
Figura 1. Panorámica de rechazo agudo y crónico.
Tinción H&E (4x): panorámica de la pieza que muestra focos de inflamación aguda
(flecha negra) e inflamación crónica con ampliación del intersticio por edema y fibrosis.
CASOS CLÍNICOS
Rechazo agudo del injerto renal no funcionante en pacientes en diálisis después de iniciar tratamiento con interferón y ribavirina
Acute rejection of non-functional renal grafts in dialysis patients after starting treatment with interferon and ribavirin
Teresa Cavero-Escribano1, Enrique Morales-Ruiz1, M. Teresa Manzano-Peña2, Raquel Muñoz-Gómez3, Eduardo Hernández-Martínez1, Eduardo Gutiérrez-Martínez 1, Manuel Praga-Terente1
1Servicio de Nefrología. Hospital Universitario 12 de Octubre. Madrid
2Servicio de Anatomía Patológica. Hospital Universitario 12 de Octubre. Madrid ]]>
3Servicio de Medicina del Aparato Digestivo. Hospital Universitario 12 de Octubre. Madrid
Dirección para correspondencia
Introducción
La infección por el virus de la hepatitis C (VHC) es relativamente frecuente en los pacientes con insuficiencia renal crónica (IRC) en tratamiento renal sustitutivo con diálisis. Aunque existen diferencias geográficas en la prevalencia, generalmente superior al 20% en los países mediterráneos, siempre es mayor que en la población general1,2. Existe una buena evidencia de que los receptores de trasplante renal con infección crónica por el VHC tienen peor supervivencia tanto del paciente como del injerto en comparación con los receptores VHC negativo3-5. El incremento de la mortalidad se ha atribuido tanto a la progresión de la enfermedad hepática, hasta un 40% presentan progresión de la fibrosis6, como a las complicaciones extrahepáticas postrasplante, diabetes de nueva aparición, microangiopatía trombótica y glomerulonefritis de novo o recidiva.
La insistencia de tratar a los pacientes en diálisis que están infectados por el VHC y esperar a que sean incluidos en la lista de trasplante renal se basa en el elevado riesgo de rechazo agudo del injerto renal inducido por el tratamiento con interferón (IFN). El IFN tiene efectos inmunomoduladores, que incluyen el incremento de expresión de genes de citoquinas y antígenos leucocitarios humanos, que favorecen la producción de aloanticuerpos donante específico que inducirían un rechazo agudo humoral7. Por todas estas consideraciones, es importante tratar la infección del VHC en los pacientes con IRC terminal mientras se encuentran en diálisis, antes del trasplante renal.
La mayoría de las publicaciones presentan resultados sobre la eficacia del IFN en monoterapia como consecuencia del rechazo histórico al uso de ribavirina (RBV) en pacientes con IRC debido a que su aclaramiento renal produce en ellos un aumento de la toxicidad que podría desencadenar una anemia hemolítica, además de empeorar la propia anemia de la enfermedad renal crónica. No obstante, debido a la eficacia de IFN y RBV en los pacientes sin IRC, se decidió asociar este último al tratamiento frente al VHC8-10, y se comprobó que, al igual que sucedía en la población general, la tasa de respuesta viral sostenida (RVS) era mayor con la doble terapia (43-50% frente a 55-66%)10,11.
En la última década, como consecuencia de los efectos deletéreos de la infección del VHC sobre la supervivencia del injerto renal y del paciente, se han planteado políticas activas de tratamiento del virus en las unidades de diálisis en aquellos pacientes que pierden la función del injerto. Sin embargo, existe experiencia en la literatura de la aparición de rechazo agudo en pacientes en diálisis con injertos no funcionantes después de iniciar el tratamiento con IFN. Es necesario conocer y diagnosticar precozmente la presencia de rechazo agudo sobre injerto no funcionante en los pacientes en diálisis que vayan a recibir estos tratamientos y que nos obliga a tomar una actitud terapéutica previa (embolización o trasplantectomía del injerto). Por este motivo, presentamos nuestra experiencia con diferentes casos con un manejo terapéutico diferente.
]]> Caso 1
Un varón de 48 años, de raza caucásica, con IRC secundaria a hipoplasia renal, inició hemodiálisis en 1984. Ese mismo año recibió su primer trasplante renal de donante vivo, su padre, que mantuvo funcionante hasta 1997, cuando retornó a hemodiálisis por nefropatía crónica del injerto y se realizó trasplantectomía. En 1999, recibió su segundo trasplante renal de donante cadáver, retornando a hemodiálisis en noviembre de 2002 tras el desarrollo de una glomerulonefritis membranoproliferativa secundaria al VHC sobre el injerto renal. Una hepatitis «no-A, no-B» se diagnosticó en 1984 y una biopsia hepática en el año 2000 mostró una hepatitis crónica periportal (P3L3F2) con RNA de VHC positivo (genotipo 3). Tras el retorno del paciente a hemodiálisis para ser incluido nuevamente en la lista de trasplante renal, se inició en marzo de 2003 tratamiento con IFN-α, 3 millones de unidades tres veces por semana. En abril de 2003 comenzó con dolor a nivel del injerto renal, hematuria y fiebre, por lo que se suspendió el INF-α y se realizó una trasplantectomía programada, observándose en la histología intensas lesiones parenquimatosas de rechazo agudo y crónico (figura 1, figura 2 y figura 3). En agosto de ese mismo año, se confirmó la negativización del RNA-VHC a pesar de haber recibido un mes de tratamiento antiviral. Sin embargo, en enero de 2004 presentó una recidiva, por lo que se reintrodujo el tratamiento antiviral, que se mantuvo durante 12 meses, consiguiéndose una RVS sin nueva recidiva. En febrero de 2008 recibió su tercer trasplante renal de donante cadáver. En la actualidad presenta una función renal normal y mantiene carga viral indetectable cinco años después de la finalización del tratamiento.

Figura 1. Panorámica de rechazo agudo y crónico.
Tinción H&E (4x): panorámica de la pieza que muestra focos de inflamación aguda
(flecha negra) e inflamación crónica con ampliación del intersticio por edema y fibrosis.

Figura 2. Rechazo agudo. ]]>
A) Tinción H&E (20x): arteritis aguda con infiltración de linfocitos en la pared. B) Tinción PAS (20x): tubulitis
aguda con permeación de linfocitos entre las células epiteliales que produce un despegamiento de la membrana basal tubular.

Figura 3. Rechazo crónico.
A) Tinción H&E (40x): arteritis crónica con engrosamiento de la íntima por proliferación de miofibroblastos con
marcada disminución de la luz. B) Tinción plata (40x): doble contorno de la membrana basal glomerular.
Caso 2
Una mujer de 50 años, de raza caucásica, con IRC secundaria a poliquistosis renal, inició hemodiálisis en 1987, recibiendo su primer trasplante renal de donante cadáver en 1988. Como complicaciones del trasplante presentó un rechazo agudo tratado con choques de esteroides, globulina antitimocítica (ATG) y anticuerpo monoclonal anti CD3 (OKT3), retornando a hemodiálisis en junio de 2009 tras pérdida del injerto renal por nefropatía crónica. Se diagnosticó una hepatitis «no-A, no-B» en 1987 en relación con politransfusión de hemoderivados, confirmándose posteriormente RNA-VHC positivo (genotipo 1a). En noviembre de 2009, cinco meses después del retorno a diálisis, se inició tratamiento con IFN pegilado α2a, 135 μg semanales, y RBV 200 mg cada 48 horas, con soporte de eritropoyetina oscilante durante todo el tratamiento. En febrero de 2010, comenzó con fiebre y hematuria, por lo que se disminuyó la dosis del tratamiento antiviral y se realizó embolización del injerto renal ante la sospecha de rechazo agudo del injerto no funcionante. Se reanudó el tratamiento con IFN y RBV a la dosis inicial, que hubo de ser suspendido en la semana 40 por la aparición de un eritema exudativo multiforme sin respuesta a tratamiento corticoideo. La paciente presentó una respuesta viral rápida con carga indetectable en la cuarta semana de tratamiento y RVS posterior. En julio de 2011, recibió su segundo trasplante renal de donante cadáver. Actualmente mantiene función renal normal y carga viral negativa.
]]>Caso 3
Varón de 48 años, de raza caucásica, con IRC secundaria a nefropatía intersticial crónica en el seno de un reflujo vesicoureteral, inició hemodiálisis en 1990. Recibió su primer trasplante renal de donante fallecido en 1991, con retorno a diálisis en 1997 por nefropatía crónica del injerto. En 1999 recibió su segundo trasplante renal con trasplantectomía urgente cinco meses después por rotura renal por rechazo agudo. En 2005 recibió su tercer trasplante renal de donante fallecido, con retorno a diálisis en enero de 2010 tras pérdida de función del injerto renal por nefropatía crónica. De nuevo, como consecuencia de las múltiples transfusiones recibidas, se diagnosticó una hepatitis «no-A, no-B» en el año 1990, confirmándose posteriormente la positividad del RNA-VHC (genotipo 1a). Seis meses después de su retorno a diálisis se realizó embolización del tercer injerto renal, dado el riesgo inmunológico de este paciente por antecedentes de rechazos agudos, hiperinmunización y tres trasplantes previos. En septiembre de 2012, tras la determinación del polimorfismo IL28B C/C (genotipo respondedor), inició tratamiento antiviral de una hepatitis viral crónica con fibrosis leve en el fibroscan con IFN pegilado α2a, 135 μg semanales, RBV 200 mg cada 48 horas y aumento de la dosis de eritropoyetina durante todo el tratamiento, observándose negativización de la carga viral en el tercer mes (respuesta viral temprana). Un año después del inicio del tratamiento, persiste indetectable y no ha presentado rechazo agudo del injerto renal no funcionante.
Discusión
En los pacientes con PCR (Polymerasa Chain Reaction) positiva para el VHC y un injerto no funcionante, no existen datos fehacientes acerca de la eficacia del IFN-α. Sin embargo, la mayoría de ellos no tienen ya tratamiento inmunosupresor, o como mucho reciben bajas dosis de corticoides, por lo que su respuesta al tratamiento antiviral, IFN en monoterapia o IFN y RBV, no debería ser diferente a la presentada por los pacientes en hemodiálisis que nunca han recibido un trasplante renal. Sin embargo, en cuanto a los efectos adversos habituales de este tratamiento en los pacientes con IRC terminal, pancitopenia, síndrome pseudogripal, anorexia, infecciones, habría que incluir el rechazo agudo del injerto no funcionante, pues debido a su efecto inmunomodulador favorece la formación de aloanticuerpos.
Hanrotel et al.12 publicaron en 2001 un estudio sobre la respuesta a IFN-α en 12 pacientes en hemodiálisis con infección crónica por el VHC. De este grupo, 2 eran portadores de trasplantes renales no funcionantes y otros 8 habían recibido un trasplante del que se realizó trasplantectomía antes del inicio del tratamiento antiviral. Estos pacientes estuvieron en diálisis 24 meses, con suspensión del tratamiento inmunosupresor al menos 6 meses antes del inicio del tratamiento erradicador del VHC. Los dos pacientes que alojaban los injertos no funcionantes presentaron un rechazo agudo del injerto. Rivera et al.11 analizaron en 2005 los datos de 27 pacientes en diálisis a los que se trató el VHC para entrar en la lista de trasplante renal, tras una estancia media en dicha terapia renal sustitutiva de 161±93 meses. Dos de ellos presentaron un rechazo agudo sobre un injerto no funcionante que todavía tenían alojado. No aportan más datos sobre tiempo de inmunosupresión, tratamiento que recibieron tras dicho diagnóstico ni si presentaron RVS. Carbognin et al.13, en 2006, presentaron un paciente con infección crónica por VHC, que tras 6 meses del inicio de diálisis y 5 desde que suspendió la inmunosupresión inició el tratamiento antiviral, presentando también un rechazo agudo del injerto. Weclawiak et al.14, en 2008, comunicaron 4 casos de pacientes en diálisis que tras la pérdida de función de su injerto mantuvieron bajas dosis de prednisona durante 6 meses e iniciaron tratamiento antiviral frente al VHC, 2, 9, 15 y 23 meses después de la entrada en hemodiálisis, presentando un cuadro clínico compatible con rechazo agudo del injerto no funcionante, que se confirmó en la pieza de trasplantectomía. Sperl et al.15, en 2008, comunicaron 2 nuevos casos de rechazo agudo del injerto no funcionante en 2 pacientes que tras 4 y 8 meses del inicio de hemodiálisis por pérdida de función del injerto iniciaron tratamiento con INF pegilado α2a. Otros 4 pacientes de este estudio que también eran portadores de trasplantes renales no funcionantes no presentaron rechazo agudo, aunque no se especifica el momento del inicio de la terapia antiviral (tabla 1).
Tabla 1. Experiencia previa. 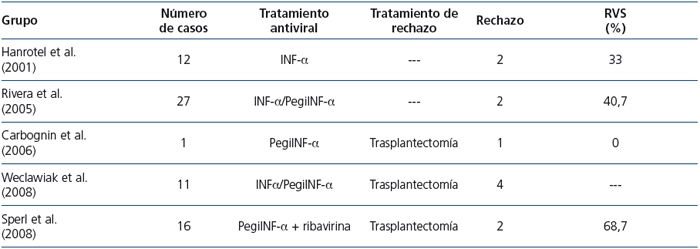 ]]>
IFN: interferón; PegiIFN: interferón pegilado; RVS: respuesta viral sostenida (definida como la
]]>
IFN: interferón; PegiIFN: interferón pegilado; RVS: respuesta viral sostenida (definida como la
negativización de la viremia mantenida al menos 24 meses después de finalizado el tratamiento).
En todos los casos anteriormente expuestos, el tratamiento de elección del rechazo agudo fue la trasplantectomía. En nuestro caso 2, la embolización del injerto fue suficiente, evitando de este modo los riesgos de la exposición a una anestesia general, una cirugía abierta y un posoperatorio. En el caso 3, debido a la experiencia previa de los casos anteriores, se decidió la embolización del injerto renal antes del inicio de la terapia antiviral. La realización de la embolizacion en un paciente de alto riesgo inmunológico ha sido suficiente para evitar la aparición de un rechazo agudo sobre el injerto no funcionante, que con alta probabilidad habría presentado después del inicio de la terapia antiviral. Además del riesgo inmunológico, probablemente el tiempo de espera desde la entrada en hemodiálisis y la suspensión de la inmunosupresión hasta el inicio de la terapia antiviral tiene un papel importante en el desarrollo de esta entidad; sin embargo, no se ha logrado demostrar por falta de estudios en este sentido. No obstante, a pesar de llevar más de 12 meses estables en diálisis, Rivera et al., Hanrotel et al. y Weclawiak et al. han publicado casos de rechazo agudo sobre injerto renal no funcionante tras el inicio de tratamiento con IFN.
En resumen, el nefrólogo debe conocer los efectos adversos del tratamiento con IFN en los pacientes con infección por VHC con injerto no funcionante para poder diagnosticar el rechazo agudo y actuar con premura, puesto que existe riesgo de rotura del injerto, con el consiguiente riesgo para la vida del paciente. Recomendamos la realización de una embolización preventiva del injerto en aquellos pacientes de alto riesgo inmunológico (antecedentes de rechazo agudo sobre el injerto, hiperinmunizados, varios trasplantes previos), puesto que, a pesar de tratarse de una técnica invasiva, los riesgos en manos de un equipo experto son mínimos.
Conflictos de interés
Los autores declaran que no tienen conflictos de interés potenciales relacionados con los contenidos de este artículo.
Referencias Bibliográficas
]]>1. Morales JM, Campistol JM. Transplantation in the patient with hepatitis C. J Am Soc Nephrol 2000;11:1343-53. [ Links ]
2. Fabrizi F, Bunnapradist S, Lunghi G, Aucella F, Martin P. Epidemiology and clinical significance of hepatotropic infections in dialysis patient. Recent evidence. Minerva Urol Nefrol 2004;56:249-57. [ Links ]
3. Pereira GJ, Natov SN, Bouthot BA, Murthy BV, Ruthazer R, Schmid CH, et al. Effects of hepatitis C infection and renal transplantation on survival in end-stage renal disease. Kidney Int 1998;53:1374-81. [ Links ]
4. Bruchefeld A, Wilczek H, Elinder CG. Hepatitis C infection, time in renal-replacement therapy, and outcome after kidney transplantation. Transplantation 2004;78:745-50. [ Links ]
5. Baid-Agrawal S, Farris AB, Pascual M, Mauiyyedi S, Farrell ML, Tolkoff-Rubin N, et al. Overlapping pathways to transplant glomerulopathy: chronic humoral rejection, hepatitis C infection and thrombotic microangiopathy. Kidney Int 2011;80:879-85. [ Links ]
]]>6. Kamar N, Rostaing K, Selves J, Sandres-Saune K, Alric L, Durand D, et al. Natural history of hepatitis C virus-related liver fibrosis after renal transplantation. Am J Transplant 2005;5:1704-12. [ Links ]
7. Terrault NA, Adey DB. The kidney transplant recipient with hepatitis C infection: pre- and posttransplantation treatment. Clin J Am Soc Nephrol 2007;2:563-75. [ Links ]
8. Tan AC, Brouwer JT, Glue P, van LR, Kauffmann RH, Schalm SW, et al. Safety of interferon and ribavirin therapy in haemodialysis patients with chronic hepatitis C: Results of a pilot study. Nephrol Dial Transplant 2001;16:193-5. [ Links ]
9. Bruchfeld A, Stahle L, Andersson J, Schvarz R. Interferon and ribavirin therapy in dialysis patients with chronic hepatitis C. Nephrol Dial Transplant 2001;16:1729. [ Links ]
10. Mousa DH, Abdalla AH, Al-Shoail G, Al-Sulaiman MH, Al-Hawas FA, Al-Khader AA. Alpha-interferon with ribavirin in the treatment of hemodialysis patients with hepatitis C. Transplant Proc 2004;36:1831-4. [ Links ]
]]>11. Rivera M, Gentil MA, Sayago M, González RF, Trigo C, Algarra G, et al. Treatment of hepatitis C virus with interferon in hemodialysis patients awaiting kidney transplant. Transplant Proc 2005;37:1424-5. [ Links ]
12. Hanrotel C, Toupance O, Lavand S, Thiefin G, Brodard V, Ingrand D, et al. Virological and histological responses to one year alpha-interferon-2a in hemodialyzed patients with chronic hepatitis C. Nephron 2001;88:120-6. [ Links ]
13. Carbognin SJ, Solomon NM, Yeo FE, Swanson SJ, Bohen EM, Koff JM, et al. Acute renal allograft rejection following pegylated IFN-a treatment for chronic HCV in a repeat allograft recipient on hemodialysis: a case report. Am J Transplant 2006;6:1746-51. [ Links ]
14. Wéclawiak H, Kamar N, Mehrenberger M, Guilbeau-Frugier C, Modesto A, Izopet J, et al. Alpha-interferon therapy for chronic hepatitis C may induce acute allograft rejection in kidney transplant patients with failed allografts. Nephrol Dial Transplant 2008;23:1043-7. [ Links ]
15. Sperl J, Petrasek J, Spicak J. Acute rejection of non-functional allograft in kidney transplant recipients with hepatitis C treated with peginterferon-a2a. J Hepatol 2008;49:461-5. [ Links ]
]]>
![]() Dirección para correspondencia:
Dirección para correspondencia:
Teresa Cavero-Escribano,
Servicio de Nefrología,
Hospital Universitario 12 de Octubre,
Av. Córdoba, s/n, 28041, Madrid
E-mail: tcaveroescribano@gmail.com
E-mail: emoralesr@senefro.org
Enviado a Revisar: 11 Oct. 2013 ]]> Aceptado el: 11 Dic. 2013
]]>