Análisis de la Resistencia Inmune en un Modelo Murino Experimental
Alimentado con Dietas Lipídicas e Infectado con Listeria monocytogenes
M.ª A. Puertollano, M.ª T. Pérez-Toscano, L. Cruz-Chamorro, E. Puertollano, G. Álvarez de Cienfuegos y M. A. de Pablo*
Área de Microbiología. Departamento de Ciencias de la Salud. Facultad de Ciencias Experimentales. Universidad de Jaén.
| Resumen Algunas dietas lipídicas están implicadas en la reducción de ciertas funciones inmunes. Sin embargo, la acción inmunosupresora de estas dietas puede tener efectos adversos sobre la resistencia inmune del individuo frente a enfermedades de naturaleza infecciosa. En el presente estudio tratamos de valorar el estado inmune de ratones alimentados con dietas lipídicas e infectados experimentalmente con una cepa virulenta de Listeria monocytogenes. (Nutr Hosp 2004, 19:333-340) Palabras clave: Aceite de oliva. Aceite de pescado. Aceite de coco. Inmunonutrición. Listeria monocytogenes. | ANALYSIS OF THE IMMUNE RESISTANCE IN AN EXPERIMENTAL MURINE MODEL FED DIETARY LIPIDS AND INFECTED WITH LISTERIA MONOCYTOGENES Abstract Several dietary lipids are capable of exerting an immunosupressor effect. This action may have undiserable effects on the host immune resistance to infectious diseases. The purpose of the present study was to determinate the immune status of mice fed dietary lipids and experimentally infected with a virulent strain of Listeria monocytogenes. (Nutr Hosp 2004, 19:333-340) ]]> Key words: Olive oil. Fish oil. Hydrogenated coconut oil. Immunonutrition. Listeria monocytogenes. |
Correspondencia: Manuel Antonio de Pablo Martínez.
Universidad de Jaén. Facultad de Ciencias Experimentales.
Departamento de Ciencias de la Salud. Área de Microbiología.
23071 Jaén.
E-mail: mapablo@ujaen.es
Recibido: 11-II-2004.
Aceptado: 26-IV-2004.
Introducción
]]> La interacción existente entre los nutrientes y el sistema inmune de animales y humanos es de gran relevancia y por consiguiente las consecuencias derivadas de la administración de ciertos componentes de la dieta deben de ser analizadas desde un punto de vista epidemiológico, clínico y experimental. Los estudios epidemiológicos llevados a cabo en los años 70 y 80 contribuyeron considerablemente a la demostración de los efectos inmunosupresores que el aceite de pescado ejerce en Esquimales de Groenlandia (población caracterizada por consumir una gran cantidad de pescado en su dieta), de manera que en esta población la incidencia de enfermedades inflamatorias es muy reducida1. Posteriormente otros estudios han destacado el papel del aceite de pescado (compuesto principal-mente por ácidos grasos poliinsaturados de la serie n-3) y del aceite de oliva (compuesto principalmente por ácidos grasos monoinsaturados de la serie n-9) en la reducción de la actividad inflamatoria característica de enfermedades de naturaleza inflamatoria como por ejemplo la artritis reumatoide2,3. Por lo tanto, la administración de ácidos grasos con actividad inmunosupresora podría tener efectos beneficiosos para la salud, dirigidos fundamentalmente a la prevención de desórdenes de tipo inflamatorio. Sin embargo, investigaciones paralelas a las mencionadas con anterioridad indicaron que en los Esquimales de Groenlandia la tasa de enfermos afectados por tuberculosis era significativamente alta4,5. Así, este hecho revela que los procesos de inmunosupresión tras la administración de dietas ricas en ácidos grasos poliinsaturados de la serie n-3 reducen la resistencia inmune frente a agentes infecciosos.Posteriormente diferentes estudios experimentales mostraron los mecanismos de acción de diferentes dietas lipídicas (fundamentalmente aquellas que contienen ácidos grasos poliinsaturados de la serie n-3) que conducen a un proceso de inmunosupresión. Igualmente otras investigaciones de carácter experimental se han centrado en el estudio de las diferentes funciones inmunes moduladas por estos ácidos grasos. Así, a lo largo de los últimos años numerosas investigaciones han puesto de manifiesto las consecuencias derivadas del consumo de una dieta rica en ácidos grasos de la serie n-3 en animales sometidos a una infección experimental con bacterias, virus o parásitos. Generalmente estas consecuencias se basan en una reducción de las funciones inmunes que conduce a un incremento de la susceptibilidad del animal frente al agente patógeno6-8.
Sin embargo, en nuestro estudio nos centramos particularmente en los efectos que una dieta rica en aceite de oliva puede provocar en la modulación de las funciones inmunes y por lo tanto es de gran importancia la determinación de las consecuencias que la administración de una dieta que contiene aceite de oliva puede inducir sobre la alteración de las funciones inmunes y especialmente sobre la resistencia a enfermedades de naturaleza infecciosa. Así, ratones de la raza Balb/c fueron divididos en cuatro grupos y alimentados cada uno con una dieta que contenía baja proporción de grasas (control), aceite de oliva (AO), aceite de pescado (AP) o aceite de coco (AC), respectivamente. Una vez finalizado el período de administración de las dietas, los ratones fueron sometidos a una infección experimental con Listeria monocytogenes, un patógeno intracelular muy utilizado para establecer los mecanismos inmunes desencadenados frente a bacterias que se desarrollan en el interior de ciertos tipos celulares.
Material y métodos
Animales y dietas
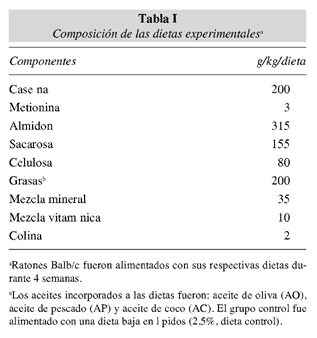
Ratones Balb/c, (8-10 semanas de edad) obtenidos de la Universidad de Jaén fueron mantenidos en jaulas a 24° C y ciclos luz/oscuridad de 12 h. Los ratones se escogieron aleatoriamente y fueron divididos en cuatro grupos experimentales. Cada grupo tuvo acceso a agua y a sus respectivas dietas experimentales ad libitum. Las dietas eran idénticas en composición a excepción del tipo de grasa. Así, el primer grupo fue alimentado con una dieta que contenía una baja proporción de lípidos (dieta control 2,5%), el segundo grupo con una que contenía aceite de oliva (AO, 20%), el tercer grupo con una que contenía aceite de pescado (AP, 20%) y finalmente el cuarto grupo con una que contenía aceite de coco (AC, 20%). Las dietas fueron administradas durante cuatro semanas antes de la infección experimental con L. monocytogenes. La composición de las dietas experimentales es mostrada en la tabla 1.
Infección experimental con Listeria monocytogenes
Una cepa virulenta de L. monocytogenes fue sembrada en agar sangre (medio agar triptona-soja (TSA) suplementado con 7% de sangre) a 37° C durante 24 h. Posteriormente para los ensayos de supervivencia, 107 unidades formadoras de colonias (UFC)/ml fueron recogidas en tampón fosfato salino (PBS) y 100 µl de esta suspensión (106 UFC) fueron inyectadas a través de la vena de la cola. Cada grupo estaba compuesto por 10 ratones y la muerte fue registrada cada 8 h. Los datos son expresados como porcentaje de supervivencia.
]]> Recuperación y cuantificación de bacterias viables a partir del bazoLos ratones fueron infectados a través de la vena de la cola (104 UFC por ratón). Los bazos de los ratones infectados fueron homogenizados asépticamente y las células lavadas tres veces en agua destilada para producir un choque osmótico y liberar a las bacterias que crecen en el interior. Seis diluciones seriadas fueron llevadas a cabo en solución salina mediante la transferencia de 10 µl en placas de agar TSA-sangre. Las placas fueron incubadas a 37° C durante 24 h y el número de colonas bacterianas fue contado. Los resultados son expresados como log10 de bacterias viables.
Medición de proliferación de linfocitos
La proliferación de linfocitos aislados del bazo de ratones alimentados con las dietas experimentales fue cuantificado mediante la técnica colorimétrica con (3-[4,5-dimethyithiazol-2 yl]-2,5-diphenyltetrazolium bromide) (MTT)9. Los esplenocitos fueron cultivados en placas de 96 pocillos a una concentración de 105 células/pocillo e incubados en una atmósfera humidificada a 37° C y 5% de CO2 durante 24 h y en presencia de concanavalin A (Con A) a 5 µg/ml. Posterior-mente se añadió 150 µl de HCI 0.04N en isopropanol para disolver los precipitados de formazan. La densidad óptica de cada muestra en triplicado se cuantificó en un lector de microplacas a 550 nm (longitud de onda de medida) y 620 nm (longitud de onda de referencia). los resultados son expresados como índice de estimulación que fue calculado como densidad óptica (DO) en presencia del mitógeno dividido por la DO en ausencia del nitógeno.
Actividad de células natural killer (NK)
La actividad de las células NK fue determinada mediante la medición de la liberación de la enzima lactato deshidrogenasa (LDH) producida por las células esplénicas en sobrenadantes de los cultivos celulares. La citotoxicidad fue medida mediante un kit (Promega, Madison, WI, USA) siguiendo las instrucciones del fabricante, Las células esplénicas (células efectoras) fueron ajustadas a una concentración de 2 x l06 células/pocillo en triplicado, mientras que las células YAC-1 (células diana) fueron ajustadas a una concentración de 104 células/pocillo en una placa de microtiter de 96 pocillos y a un ratio efectoras:diana de 100:1, 50:1 y 25:1. La liberación máxima de LDH fue determinada al incubar las células diana con Triton X-100 al 0,8%. En cambio, la liberación de LDH espontánea fue cuantificada mediante el cultivo de las células diana en RPMI 1.640 suplementado con suero bovino fetal (SBF) al 5%. La placa fue centrifugada durante 5 min a 700 rpm y posteriormente las células se incubaron durante 5 h a 37° C y en una atmósfera humidificada con 5% de CO2. El tampón de liberación máxima fue añadido 45 min antes de que finalizara el periodo de incubación. El substrato fue añadido a cada pocillo, incubando las células durante 30 min a temperatura ambiente y protegidas de la luz. Finalmente la reacción fue detenida al añadir la solución stop y la placa fue leída en un lector de microplacas a una longitud de onda de 492 nm, Los valores son expresados como porcentaje de liberación de LDH y calculados según la siguiente ecuación:
Citotoxicidad= [(DOexperimental-DOespontáneaefectoras-
DOespontánea diana)/(Dmáximo diana-DOespontánea diana)] x 100
Análisis de la actividad bactericida
Determinación de adhesión e invasión de L. monocytogenes
Para este ensayo las células esplénicas ajustadas a una concentración de 3 x 105 por pocillo fueron dispuestas en placas de 24 pocillos. Para los ensayos de adhesión, las células fueron infectadas con 0,1 ml de suspensión bacteriana (20 bacterias por célula, índice de multiplicidad 2001) durante 2 h de incubación a 37° C y 5% C02. Posteriormente las células fueron lavadas tres veces y lisadas con 1 ml de Triton X-100 al 1% durante 5 min a 37° C, seguido por 10 diluciones seriadas en TSA-sangre. Las UFC fueron contadas después de 24 h de incubación de las placas a 37° C. Para los ensayos de invasión 50 µg/ml de gentamicina fueron añadidos al cultivo celular infectado para matar las bacterias extracelulares; seguido de 2 h de incubación a 37° C. Finalmente, las células fueron lavadas dos veces y lisadas con Triton X-100 al 1% durante 5 min a 37° C. Los resultados fueron expresados como log10 de bacterias viables.
Análisis estadístico
Los datos son presentados como media ± error estándar de la media, Los resultados fueron determinados por análisis de varianza (ANOVA) para comparar los efectos de las dietas experimentales y el grupo control. Cuando ANOVA indicó diferencias significativas, se utilizó el test LSD. Las diferencias estadísticamente significativas fueron consideradas a P < 0,05.
Resultados
1. Análisis in vivo
Peso de ratón y bazo
Los pesos de ratón y bazo no mostraron diferencias estadísticamente significativas en todos los grupos analizados, con excepción del grupo alimentado con AP en el cual una reducción significativa en el peso de ratón y bazo fue observada después de la administración de la dieta (tabla II).
]]>La figura 1 muestra los valores de supervivencia de ratones alimentados con dietas lipídicas a una infección experimental con L. monocytogenes. Los animales alimentados con la dieta que contiene AP mueren antes que aquellos alimentados con los otros tipos de dieta analizados. De hecho, a las 48 h de la infección experimental con L. monocytogenes sólo sobrevivieron el 20% de los animales, mientras que a las 96 h murieron el 100% de todos los animales que integraban este grupo. Sin embargo, en los grupos alimentados con AO o AC los animales sobrevivieron durante más tiempo especialmente en los animales alimentados con esta última dieta, donde los porcentajes de supervivencia fueron superiores al resto de los grupos.
Fig. 1.-Porcentaje de supervivencia de ratones alimentados con dietas lipídicas
(n=10 en cada grupo experimental) después de la infección con Listeria monocytogenes.
Recuentos de bacterias viables a partir del bazo
El recuento de bacterias viables obtenidas a partir del bazo de ratones alimentados con dietas lipídicas ha mostrado un incremento estadísticamente significativo en los grupos alimentados con AO, AP o AC con respecto al grupo alimentado con una dieta baja en lípidos (control) (P < 0,05). Sin embargo, es destacable mencionar el elevado número de bacterias aisladas en bazos de ratones alimentados con la dieta que contiene AP, mayor que en el resto de los grupos analizados (fig. 2).
]]> Fig. 2.-Recuentos de Listeria monocytogenes aislada a
2. Análisis ex vivo
Proliferación de linfocitos estimulados con concanavalin A (Con A)
La figura 3 muestra la proliferación de linfocitos estimulados con el mitógeno Con A. La proliferación de linfocitos procedentes de ratones alimentados con AP mostró una reducción estadísticamente significativa con respecto a los valores de linfoproliferación en animales alimentados con una dieta control (P < 0,05). En el resto de los grupos no encontramos alteraciones estadísticamente significativas con respecto a la proliferación de linfocitos, aunque podemos observar un ligero incremento en la proliferación de linfocitos en el grupo alimentado con la dieta que contiene AO.
]]> Fig. 3.-Medición de la proliferación de linfocitos estimulados
Actividad de células natural killer (NK)
La tabla III muestra la actividad de células NK en animales alimentados con dietas lipídicas. La administración de las diferentes dietas lipídicas no modifican la actividad de células NK medida como porcentaje de citotoxicidad.
]]>
Actividad bactericidaLa actividad bactericida determina la capacidad de las células fagociticas para eliminar un determinado patógeno. La tabla IV muestra la medición de la actividad bactericida de células peritoneales procedentes de animales alimentados con dietas lipídicas. En el grupo alimentado con AP podemos observar una reducción significativa de la capacidad de estas células para eliminar a L. monocytogenes (P < 0,05), mientras que en el grupo alimentado con AO el porcentaje de la actividad bactericida es mayor que el del grupo control.
Adhesión e invasión
En este estudio tratamos de determinar también la capacidad de adhesión e invasión de L. monocytogenes en esplenocitos procedentes de animales alimentados con dietas lipídicas. Los valores de adhesión fueron reducidos significativamente en esplenocitos de animales alimentados con AP, mientras que los mayores valores de invasión fueron observados en el grupo alimentado con AO (fig. 4).
Fig. 4.-Medición de la adhesión e invasión de Listeria
monocytogenes en esplenocitos procedentes de animales
alimentados con dietas lipídicas e incubadas durante 2 h. ]]>
Adhesión (barras abiertas), invasión (barras cerradas).
*P < 0,05 comparado con el grupo control es considerado
como estadísticamente significativo (n = 5 en cada grupo
experimental).
Discusión
Los estudios experimentales y epidemiológicos llevados a cabo hasta el momento han revelado las propiedades inmunomoduladoras de algunas dietas lipídicas y la importancia que han adquirido algunos ácidos grasos en inmunonutrición11,12. Sin embargo, la acción que ejercen las mencionadas dietas lipídicas depende fundamentalmente del tipo de ácidos grasos contenidos en ellas. Tal y como hemos indicado con anterioridad, el aceite de pescado compuesto principalmente por ácidos grasos de la serie n-3 es el más inmunosupresor ejerciendo su efecto sobre diferentes funciones del sistema inmune como es la proliferación de linfocitos13, producción de diferentes citoquinas14, actividad de células NK15, o moléculas de adhesión16. Esta propiedad inmunosupresora se ha revelado muy importante en la reducción de los síntomas inflamatorios característicos de enfermedades autoinmunes como por ejemplo la artritis reumatoide2,3. Sin embargo un efecto inmunosupresor también puede ser perjudicial, puesto que reduce la resistencia inmune del individuo frente a agentes patógenos6,7. Muchos son los estudios que han indicado que la administración de dietas que contiene ácidos grasos de la serie n-3 reducen la resistencia inmune frente a patógenos tan importantes como Mycobacterium tuberculosis17, Salmonella typhimurium18 Pseudomonas aeruginosa19 o L. monocyto-genes20-22. Por el contrario es necesario mencionar que otros estudios han demostrado un incremento de la resistencia inmune en animales alimentados con dietas enriquecidas con aceite de pescado e infectados experimentalmente con Klebsiella pneumoniae23-24, 0 bien una ausencia de efecto en ratones alimentados con diferentes dietas lipídicas en infectados con Pseudomonas aeruginosa o Salmonella typhimurium25. Sin embargo, a nuestro juicio estas discrepancias se pueden deber a los diferentes mecanismos de patogenia que utilizan las diferentes bacterias expuestas con anterioridad, si bien los estudios llevados a cabo con el virus influenza en animales alimentados con aceite de pescado han demostrado también una reducción de la resistencia inmune frente a este agente26,27.
Estas propiedades inmunosupresoras asociadas a la administración de dietas que contienen aceite de pescado no se ven tan agudizadas con la administración de dietas que contienen AO, puesto que esta grasa no ejerce un efecto inmunosupresor tan relevante como el AP28. Así, los ensayos in vivo han demostrado como los índices de supervivencia de los animales alimentados con ácidos grasos saturados son mayores y consecuentemente sobreviven a la infección con una dosis letal de L. monocytogenes durante un periodo de tiempo ligeramente superior que el grupo alimentado con AP22. Paralelamente este estudio ha demostrado como a partir del bazo de los animales experimentalmente infectados con L. monocytogenes y alimentados con una dieta que contiene ácidos grasos saturados se produce una reducción en el recuento de bacterias viables en comparación con el grupo alimentado con la dieta que contiene AP, esto indica que el sistema inmune del grupo alimentado con ácidos grasos saturados posee una mayor capacidad para eliminar a L. monocytogenes que el grupo alimentado con una dieta que contiene AP22. En nuestro estudio hemos podido comprobar como se reduce la supervivencia en el grupo alimentado con AP, mientras que la recuperación de bacterias viables aisladas a partir de bazo es mayor, lo cual indica una ineficiente capacidad de eliminación de L. monocytogenes en el grupo alimentado con esta dieta. Por el contrario, en el resto de los grupos el porcentaje de supervivencia fue ligeramente superior y la recuperación de bacterias viables a partir de bazo fue menor que en el grupo alimentado con la dieta que contiene AP.
Las propiedades inmunosupresoras asociadas al AO se deben exclusivamente a la acción del ácido oleico y por lo tanto, otros componentes menores que forman parte de este aceite no están implicados en estas acciones29. Además, la administración de N-acetil-L-cisteína, agente con función antioxidante, no produjo ningún efecto en la supervivencia o en el recuento de bacterias viables obtenidas a partir del bazo de animales alimentados con una dieta que contenía AO o AP, lo que demuestra que el posible papel de la oxidación causada por la administración de dietas que contienen ácidos grasos poliinsaturados o monoinsaturados, no adquiere ninguna importancia en la supresión del sistema inmune y por lo tanto, otras causas diferentes a los procesos de oxidación son responsables de la modulación del sistema inmune por los ácidos grasos de la dieta30.
Uno de los posibles mecanismos implicados en un mejor estado del sistema inmune en animales alimentados con AO puede estar relacionado con una mejor respuesta linfoproliferativa. En esplenocitos procedentes de ratones alimentados con AO y estimulados con un mitógeno de células T como es Con A pudimos observar un incremento de esta actividad, mientras que una reducción significativa del índice de estimulación fue cuantificado en esplenocitos de animales alimentados con AP. Este dato indica la capacidad supresora de esta dieta, tal y como algunos estudios sugieren13. Por otra parte, en nuestro estudio no comprobamos ninguna alteración de la actividad de células NK después de la administración de dietas lipídicas, mientras que otras investigaciones han encontrado una reducción de la actividad de estas células15. Aquí, también determinamos la capacidad de adhesión e invasión de L. monocytogenes en esplenocitos de animales alimentados con dietas lipídicas. Como podemos apreciar, los valores de invasión son superiores en el grupo alimentado con la dieta que contiene AO, mientras que la capacidad bactericida en este grupo fue mayor. Estos resultados indican que uno de los factores implicados en la eliminación de L. monocytogenes en el grupo alimentado con AO está relacionado con la capacidad de las células procedentes de estos ratones para posibilitar la entrada de L. monocytogenes, mientras que simultáneamente un incremento de la actividad bactericida frente a este patógeno ha sido evidenciado, lo cual facilita considerablemente la eliminación de este patógeno10.
]]> De estos estudios se deduce principalmente que si bien el AO ejerce un proceso inmunosupresor, éste no es tan relevante como el derivado de la administración de dietas que contienen AP y esto provoca un mayor incremento de la resistencia inmune del individuo frente a enfermedades de naturaleza infecciosa. Por consiguiente, a raíz de estas investigaciones se desprende la secuencia de los ácidos grasos más inmunosupresores; así ácidos grasos poliinsaturados > ácidos grasos monoinsaturados ≥ ácidos grasos saturados.Sin embargo, a pesar de los descubrimientos dentro de este campo, en los últimos años se han generado una serie de discrepancias lo cual hace necesario una mayor investigación con el objeto de despejar las actuales controversias y determinar las razones por las cuales en algunos casos las dietas enriquecidas con ácidos grasos poliinsaturados de la serie n-3 incrementan la resistencia inmune, mientras que en otros casos la reducen. Este hecho podría estar relacionado con la necesidad de definir de forma precisa los componentes del sistema inmune requeridos para la defensa frente a un patógeno específico, el modo de administración del patógeno, las especies animales objeto del estudio o la cantidad de ácidos grasos administrados en la dieta.
Conclusiones
Las dietas lipídicas constituidas por ácidos grasos poliinsaturados de la serie n-3 (contenidos fundamentalmente en el aceite de pescado) producen una supresión de las funciones inmunes, lo cual conduce a una reducción de la resistencia inmune del individuo frente a agentes patógenos (bacterias o virus). Sin embargo, las dietas constituidas por ácidos grasos monoinsaturados (contenidos particularmente en el aceite de oliva) no ocasionan una inmunosupresión tan agudizada como los ácidos grasos poliinsaturados de la serie n-3 y no inducen un incremento tan severo de la susceptibilidad del individuo a enfermedades de naturaleza infecciosa.
Agradecimientos
M. A. Puertollano recibe una beca del Plan de Formación de Personal Docente e Investigador de la Junta de Andalucía. E. Puertollano recibe una beca del Plan de Formación de Profesorado Universitario del Minis-terio de Educación, Cultura y Deporte.
Referencias
1 . Kromann N y Green A: Epidemiological studies in the Upernavik district, Greenland incidence of some chronic diseases 1950-1974. Acta Med Scand 1980, 208:401-406. [ Links ]2. Kremer JM, Lawrence DA, Jubiz W y cols.: Dietary fish oil and olive oil supplementation in patients with rheumatoid arthritis. Clinical and immunologic effects. Arthritis Rheum 1990, 33:810-820. [ Links ]
3. Linos A, Kaklamanis E, Kontomerkos A y cols.: The effect of olive oil and fish consumption on rheumatoid arthritis-case control study. Scand J Rheumatol 1991, 20:419-426. [ Links ]
4. Kaplan, GJ, Fraser, RI, Comstock GW: Tuberculosis in Alaska 1970. Am Rev Respir Dis 1971, 105:920-926. [ Links ]
5. Stevenson M: Tuberculosis in the north - a lifestyle issue. Can Nurse 1984, 80:41-43. [ Links ]
6. Anderson M, Fritsche KL: (n-3) fatty acids and infectious disease resistance. J Nutr 2002, 132:3566-3576. [ Links ]
7. De Pablo MA, Puertollano MA, Álvarez de Cienfuegos G: Biological and clinical significance of lipids as modulators of immune system functions. Clin Diagn Lab Immunnol 2002, 9:945-950. [ Links ]
8. De Pablo MA, Puertollano MA y Álvarez de Cienfuegos G: Immune cell functions, lipids and host natural resistance. FEMS Immunol Med Microbiol 2000, 29:323-328. [ Links ]
9. Mosmann T: Rapid colormetric, assay for cellular growth and survival: application to proliferation and cytotoxicity assays. J Immunol Methods 1983, 65:55-63. [ Links ]
10. Palombo JD, DeMichele SJ, Boyce PJ y cols.: Effect of short-term enteral feeding with eicosapentaenoic and gamma-linolenic acids on alveolar macrophage eicosanoid synthesis and bactericidal function in rats. Crit Care Med 1999, 27:1908-1915. [ Links ]
11. Calder PC: Fat chance of immunomodulation. Immunol Today 1998, 19:244-247. [ Links ]
12. De Pablo MA, Álvarez de Cienfuegos: G: Modulatory effects of dietary lipids on immune system functions. Immunol Cell Biol 2000, 78:31-39. [ Links ]
13. Yaqoob P, Newsholme EA, Calder PC: The effect of dietary lipid manipulation on rat lymphocyte subsets and proliferation. Immunology 1994, 82:603-610. [ Links ]
14. Calder PC: N-3 polyunsaturated fatty acids and cytokine production in health and disease. Ann Nutr Metab 1997, 41:203-234. [ Links ]
15. Yaqoob P, Newsholme EA, Calder PC: Inhibition of natural killer cell activity by dietary lipids. Immunol Lett 1994, 41:241-247. [ Links ]
16. Sanderson P, Calder PC: Dietary fish oil diminishes lymphocyte adhesion to macrophage and endothelial cell monolayers. Immunology 1998, 94:79-87. [ Links ]
17. Paul KP, Leischsenring M, Pfisterer M y cols.: Influence of n-6 and n-3 polyunsaturated fatty acids on the resistance to experimental tuberculosis. Metabolism 1997, 46:619-624. [ Links ]
18. Chang HR, Dullo AG, Vladoianu IR y cols.: Fish oil decreases natural resistance of mice to infection with Salmonella typhimurium. Metabolism 1992, 41:1-2. [ Links ]
19. Peck MD, Alexander JW, Ogle CK y Babcock GF: The effect of dietary fatty acids on response to Pseudomonas infection in burned mice. J Trauma 1990, 30:445-452. [ Links ]
20 De Pablo MA, Puertollano MA, Gálvez A, Ortega E, Gaforio JJ y Álvarez de Cienfuegos G: Determination of natural resistance of mice fed dietary lipide to experimental infection induced by Listeria monocytogenes. FEMS Immunol Med Micro-biol 2000; 27:127-133. [ Links ]
21. Puertollano, MA, De Pablo MA y Álvarez de Cienfuegos G: Relevance of dietary lipids as modulators of immune functions in cells infected with Listeria monocytogenes. Clin Diagn Lab Immunol 2002,9:352-357. [ Links ]
22. Fritsche KL, Shahbazian LM, Feng C, Berg JN: Dietary fish oil reduces survival and impairs bacterial clearance in C3H/Hen mice challenged with Listeria monocytogenes. Clin Sci 1997, 92:95-101. [ Links ]
23. Bjornsson S, Hardardottir 1, Gunnarson E, Haraldsson A: Dietary fish oil supplementation increases survival in mice following Klebsiella pneumoniae infection. Scand J Infect Dis 1997, 29:491-493. [ Links ]
24. Blok WL, Vogels MT, Curfs JH, Eling WM, Buumnan WA, Van der Meer JW: Dietary fish-oil supplementation in experimental gram-negative infection and in cerebral malaria in mice. J Infect Dis 1992,165:898-903. [ Links ]
25. Clouva-Molyvdas P, Peck MD, Alexander JW: Short-term dietary lipid manipulation does not affect survival in two models of murine sepsis. J Parenter Enteral Nutr 1992, 16:343-347. [ Links ]
26. Byleveld PM, Pang GT, Clancy RL, Roberts DCK: Fish oil feeding enhances lymphocyte proliferation but impairs virus-specific T lymphocyte cytotoxicity in mice following challenge with influenza virus. Clin Exp Immunol 2000, 119:287-292. [ Links ]
27. Byleveld PM, Pang GT, Clancy RL, Roberts DC: Fish oil feeding delays influenza virus clearance and impairs production of interferon-gamma and virus-specific, immunoglobulin A in the lungs of mice. J Nutr 1999, 129:328-335. [ Links ]
28. Yaqoob P, Knapper JA, Webb DH, Williams CM, Newsholme EA, Calder PC: Effect of olive oil on immune function in middle-aged men. Am J Clin Nutr 1998, 67:129-135. [ Links ]
29. Jeffery NM, Yaqoob P, Newsholme EA, Calder PC: The effects of olive oil upon rat serum lipid levels and lymphocyte functions appear to be due to oleic acid. Ann Nutr Metab 1996, 40:71-80. [ Links ]
30. Puertollano MA, De Pablo MA, Álvarez de Cienfuegos G: Anti-oxidant properties of N-acetyl-L-cysteine do not improve the immune resistance of mice fed dietary lipids to Listeria monocytogenes infection. Clin Nutr 2003, 22:313-319. [ Links ] ]]>