La expresión de IL-10 interviene en la regulación de la respuesta inflamatoria por los ácidos grasos omega 3
S. Sierra, F. Lara-Villoslada, M. Olivares, J. Jiménez, J. Boza y J. Xaus
Departamento de Inmunología y Estudios Preclínicos. Puleva Biotech. Granada.
| Resumen Objetivo o antecedente: Los ácidos grasos poliinsaturados son importantes para el organismo humano debido a su implicación en numerosas funciones biológicas. Las dietas occidentales se caracterizan por ser excesivamente ricas en ácidos grasos w-6 y pobres en ácidos grasos w-3. (Nutr Hosp 2004, 19:376-382) Palabras clave: Ácidos grasos poliinsaturados. Inflamación. Organismo. | IL-10 EXPRESSION IS INVOLVED IN THE REGULATION OF THE IMMUNE RESPONSE BY OMEGA 3 FATTY ACIDS Abstract Introduction: Polyunsaturated fatty acids play a key role in a huge number of biological functions. Western diets are highly rich in w-6 fatty acids. However the content of w-3 fatty acids is not suitable in those diets, despite of their importance in normal development of the human body and regulation of immune response. (Nutr Hosp 2004, 19:376-382) Key words: Polyunsaturated fatty acids. Antiinflammatory. Organism.
|
Correspondencia: J. Xaus.
Departamento de Inmunología y Estudios Preclínicos.
Puleva Biotech.
Camino de Purchil, 66. 18004 Granada.
E-mail: jxaus@pulevabiotech.es
Recibido: 21-I-2004. ]]> Aceptado: 13-II-2004.
Introducción
El sistema inmunológico está involucrado en la defensa del organismo frente a agentes extraños, células tumorales y agresiones externas. Un elevado número de órganos, células, tejidos y moléculas interactúan para llevar a cabo esta misión.
El desarrollo, mantenimiento y óptimo funcionamiento del sistema inmunológico depende de la dieta entre otros factores. Entre los nutrientes que más afectan al sistema inmunológico destaca la grasa cuya deficiencia o desequilibrada aportación así como la calidad de la misma comprometen la estabilidad del sistema inmunológico1.
La relación entre ácidos grasas e inflamación se debe principalmente al componente fosfolipídico de las células del sistema inmunológico. Los ácidos grasos incorporados en la membrana de las mismas pueden afectar a las funciones de ésta y por tanto al funcionamiento celular. Los fosfolípidos de membrana son responsables de la fluidez de la misma, que afectará a los diferentes componentes anclados en ella. Diversas señales intracelulares parten de estos fosfolípidos y su composición, por tanto, afecta diferentes vías de transducción de señales. Además, los ácidos grasos sintetizados a partir de los fosfolípidos, son sustratos para la síntesis de un grupo de mediadores, los eicosanoides, de marcada importancia biológica2.
Actualmente, el interés por el estudio de los ácidos grasos es creciente, y cobra importancia la influencia de ellos sobre la respuesta inmunológica. Dicho interés se ha centrado en el estudio de los ácidos grasos poliinsaturados de cadena larga (AGPI-CL), procedentes de las familias w-6 y w-3, cuyos precursores, ácidos linoléico y α-linolénico, son esenciales, debiendo ser ingeridos con la dieta, así como se recomienda también incluir en ella algunos de sus derivados, como el ácido eicosapentaenoico (EPA), docosahexaenoico (DHA) y araquidónico (AA), ya que a través de las vías metabólicas, por elongación de sus precursores, no se alcanzan los niveles adecuados3.
En individuos que consumen dietas occidentales, las células inflamatorias contienen elevadas proporciones de AGPI-CL de la serie w-6, especialmente de AA y bajas proporciones, sin embargo, del EPA de la serie w-34. El principal papel de AA es actuar como sustrato para la síntesis de mediadores bioactivos del tipo eicosanoides. Estos están implicados en modular la duración y la intensidad de la respuesta inflamatoria. Los derivados del AA, como TXA2 y LTB4, son potentes agentes con un marcado efecto infamatorio. El TXA2, tiene efecto vasoconstrictor y proagregante mientras que el LTB4 es un potente agente quimiotáctico5. Además, la PGE2 induce fiebre, aumenta la permeabilidad vascular y la vasodilatación, al tiempo que la producción de IgE por células B.
El aumento del consumo de los ácidos grasos w-3 conlleva una disminución del AA en las membranas de las células inflamatorias disminuyéndose así su capacidad para sintetizar a partir de la COX y la LOX eicosanoides derivados del AA. Además de inhibir el metabolismo del AA, el EPA inhibe la oxigenación del AA por la COX, y suprime la inducción de ciertas citocinas que actúan sobre la expresión génica de la COX-2 y la 5-LOX. También es capaz de actuar como sustrato de la COX y la 5-LOX, dando lugar a eicosanoides considerados biológicamente menos activos5.
Todo esto lleva a la idea de que el aceite de pescado tiene propiedades antiinflamatorias. El consumo en individuos sanos de una proporción adecuada de los ácidos grasos w-6 y w-3 llevaría a una mejor regulación de la respuesta inmunológica, y el consiguiente incremento de la proporción de los ácidos grasos w-3 resultaría beneficioso para sujetos que padezcan enfermedades autoinmunes o inflamatorias por el efecto antiinflamatorio de los mismos1.
]]> No solo estos mecanismos están involucrados en el efecto antiinflamatorio sino que actualmente se está conociendo su implicación a nivel de vías de señalización como NFkB, MAPK o PPAR y LXR6. La actuación a través de estos dos últimos receptores abre un nuevo campo de investigación y una mayor gama de aplicaciones de los ácidos grasos w-3 debido a la localización y función de los mismos.El presente estudio trata de poner de manifiesto el efecto antiinflamatorio de los ácidos grasos w-3 y los mecanismos implicados, midiendo parámetros inmunológicos que permitan comprobar su efecto a nivel sistémico, y analizando el curso de una inflamación inducida para determinar su actuación a nivel local.
Material y métodos
Reactivos y anficuerpos
La concanavalina A (Con A) y el lipopolisacárido (LPS) fueron proporcionados por Sigma Chemical Co (St Louis, Mo). Para medir inmunoglobulinas se utilizaron anticuerpos proporcionados por Bethyl (Montgomery TX) y en el caso de las citocinas por Biosource (Camarillo, CA). La peroxidasa de rábano, el bromuro de hexadeciltrimetilamonio, el clorhidrato de o-dianisidina y el peróxido de hidrógeno para la medida de actividad miloperoxidasa así como el ácido tricloroacético, el ß-NADPA, el 5,5-ditio-bis (2-ácido nitrobenzoico) y el glutatión fueron también adquiridos en Sigma. La glutatión reductasa fue suministrada por Roche. Se empleó agua desionizada purificada con un sistema Millipore Milli-Q (Bedford, MA).
Animales y dietas
Ratones macho Balb/c al destete de tres semanas de edad fueron proporcionados por la Universidad de Granada. Se les mantuvo durante todo el experimento a una temperatura controlada de 22° C y bajo un ciclo de luz de 12 horas. El experimento global fue llevado a cabo 3 veces con resultados similares.
Todos los estudios animales que se realizaron se llevaron a cabo según las Normas de Ética Animal fijadas en los Criterios de Helsinki.
El experimento consta de 2 grupos de ratones (n = 10) alimentados durante 28 días con dietas base iguales y cuya diferencia radica en el tipo de grasa incluida. Ambas contienen el 5% de grasa del total de la dieta. Este 5% de grasa está constituido por aceite de girasol en el caso del grupo usado como control. En el caso de la dieta w-3, el 12% del contenido total de grasa es aceite de pescado refinado, mientras que el resto de la grasa es el mismo aceite de girasol del grupo anterior. Ambas dietas fueron elaboradas de mane-ra específica siguiendo las recomendaciones de la Academia Americana de Veterinaria para Nutrición Animal. De este modo se prepararon dietas semisintéticas incluyendo en las mismas el 5% de grasa, 21,3% de proteína, 67,5% de hidratos de carbono, 5,2% de fibra y el 1% restante de una mezcla de vitaminas y minerales.
Las dietas fueron conservadas en atmósfera de argón y administradas diariamente a los ratones para evitar la oxidación de los AGPI-CL. A lo largo del estudio se llevó a cabo un control del peso y aspecto.
]]> Doce horas antes del sacrificio se indujo una dermatitis de contacto en una de las orejas de cada ratón. El agente irritante usado fue el 2,4-dinitro-1-fluorobenzeno al 0,5% en una solución de acetona: aceite de oliva 4:1. Se utilizaron de esta solución 80 µl que se pusieron en cada oreja7.El sacrificio se realizó por medio de una inyección intraperitoneal de pentotal sódico (50 mg/kg) y seguidamente la sangre fue extraída por punción cardiaca en tubos que contenían EDTA (60 mg/ml). La sangre se centrifugó (3.500 rpm) 10 minutos a 4° C y las alícuotas de suero fueron recogidas y almacenadas a -80° C.
Procesamiento de las orejas
Ambas orejas de cada ratón fueron pesadas en balanza de precisión. La mitad de ellas fueron introducidas durante 24 horas en una estufa a 60° C y posterior-mente se analizó su peso seco y su consiguiente contenido de agua. La mitad restante, se homogeneizó independientemente en tampón HITAB (Bromuro de hexadeciltrimetilamonio) a la proporción de 1/20 para proceder a la medida de glutatión total y de actividad mieloperoxidasa. Dichas medidas se realizaron según lo descrito anteriormente8,9.
Cultivo de células
Los bazos de cada ratón se extrajeron y cultivaron como se ha descrito anteriormente10. La médula ósea de los fémur y las tibias de cada ratón fueron extraídos por inyección de medio y cultivadas, previa diferenciación, según se ha descrito con anterioridad1l.
Ensayo de proliferación
Los linfocitos derivados de bazo fueron cultivados en placas de 24 pozos (2 x 106, células/pozo) con 500 ul de medio e incubados en presencia o ausencia de Con A (5 µg/ml) o LPS (50 µg/ml). Timidita tritiada (Amersbam Biosciences, Arlington Heights, IL) a la concentración de 1 µCi/ml fue añadida a cada pozo. La incorporación de timidina tras 48 horas fue analizada como se ha descrito anteriormente1l. Las medidas se realizaron por duplicado y fueron representadas como la media ± SD.
Producción de citocinas
Los linfocitos de bazo fueron cultivados en placas de 6 pozos (5 x 106 células/ml) con 5 ml de medio y fueron estimulados con Con A y LPS a las mismas concentraciones usadas en el ensayo de proliferación. Tras 48 horas se recogieron los sobrenadantes. El sedimento fue lisado con 1 ml de trizol para posterior extracción de RNA. En el caso de los macrófagos, estos fueron cultivados en placas de 6 pozos (3 x l06 células/pozo) y estimulados con LPS (100 ng/ml). Tras 24 horas se recogió el sobrenadante y se lisaron los sedimentos celulares.
]]> Los niveles de IgA, IgE, e IgG1, fueron determinados en suero. La concentración de IL-10, TNFα, e IL-2 fue medida en sobrenadante de bazo y de macrófiagos por ELISA siguiendo las instrucciones del fabricante.Análisis estadístico
El grado de significación estadística entre los grupos fue determinado por el test de la t-Student a dos colas y con varianzas iguales entre las muestras (p < 0,05). Los resultados han sido expresados como la media ± SD.
Resultados
Los animales fueron controlados durante el mes que duró el experimento observándose una conducta y aspecto normales. Se comprobó que la evolución en el crecimiento era la adecuada y que no existían diferencias entre los dos grupos. No existió tampoco ningún tipo de anomalías con respecto a la cantidad, consistencia y aspecto de las heces, siendo el contenido de agua de las mismas similar en ambos grupos.
Con el objetivo de evaluar los efectos de los ácidos grasos w-3 en los roedores se estudiaron diversos parámetros sistémicos que pudiesen aportar información de cómo estos modulan el sistema inmunológico y por tanto, aclarar sus posibles mecanismos de acción.
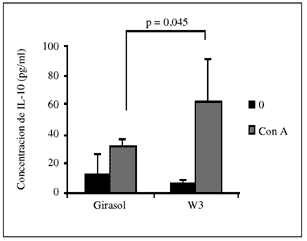
Las citocinas son un grupo muy diverso de moléculas producidas por células en respuesta a una gran variedad de estímulos y que son capaces de alterar de alguna manera el comportamiento de otras células. Es el caso de la IL-10, una interleucina de tipo regulador que media la denominada respuesta Th3. En este estudio se tomaron suero, sobrenadante de cultivo de linfocitos y sobrenadante de macrófagos y se determinó por ELISA los niveles de dicho mediador, descubrién-dose un aumento significativo en el grupo de ratones alimentados con ácidos grasos w-3 en la producción de IL-10 por parte de macrófagos (94,7 ± 57,8 vs 126,5 ± 37,6 pg/ml, p = 0,05) y linfocitos (31,56 ± 5,51 vs 61,29 ± 29,08 pg/ml p = 0,045) al ser las células estimuladas (fig. l).
Fig. 1.-El consumo de ácidos grasos w-3 induce la expresión
de IL-10. Niveles de IL-10 en sobrenadante de cultivo de bazo ]]>
sin estimular o estimulado con concanavalina A (Con A).
Como consecuencia del incremento de IL-10 se observó la disminución de citocinas de tipo Th1, como por ejemplo la IL-2 liberada por linfocitos (332,83 ± 197,86 vs 181,61 ± 137,1 pg/ml, p = 0.05) (fig. 2A). El descenso en los niveles de esta interleucina llevó a la disminución significativa de la proliferación de linfocitos B en el grupo de ratones tratados con w-3 (7.300 ± 2.873,55 vs 4.681 ± 2.243,35 cpm, p = 0,04) y a una reducción de la proliferación de los linfocitos T (7.622,6 ± 3.692,8 vs 5.048,4 ± 2.507,07 cpm, p = 0,07) señalando ya un posible efecto supresor de los ácidos grasos w-3 sobre el sistema inmunológico (fig. 2B). Este dato se correlacionó también con una tendencia a disminuir el tamaño del bazo expresado como mg bazo/g ratón (5,72 ± 1,36 vs 4,7 ± 0,54, p = 0,08).
Esta disminución en el número de linfocitos debe tener una repercusión drástica sobre el sujeto debido al papel fundamental de estas células en la defensa del organismo. Por tanto, otras citocinas liberadas por estas células podrían estar alteradas. También el efecto de la IL-10 debería haber recaído sobre los macrófagos por lo que para comprobar si se producía dicha correlación se procedió a medir algunos de estos media-dores como, por ejemplo, el TNFα (5.306 ± 0,51 vs 3.831 ± 0,82 ng/ml, p = 0,06) (fig. 2C).
Además de la disminución de la respuesta tipo Th1, también observamos que la dieta rica en w-3 ejercía un efecto inhibidor de la respuesta Th2 como se observa por la disminución de los niveles plasmáticos de IgE (291,7± 53,06 vs 176,04 ± 71,4 ng/ml, p = 0,06) e IgG (802,31 ± 228,1 vs 392,01 ± 191,3 µg/ml, p = 0,05) (fig. 3A,B) o de IL-4 e histamina (datos no mostrados).
A pesar de la disminución generalizada de la respuesta inmunológica, los ratones alimentados con w-3 no experimentaron síntomas de debilidad ni predisposición a la infección. Esto puede ser debido al incremento en estos animales de parámetros relacionados con la defensa natural del organismo como pueden ser los niveles de IgA séricos (208,23 ± 100,3 -vs 572,26 ± 135,01 µg/ml, p = 0,04) (fig. 3C), expresión de iNOS y la producción de NO por los macrófagos (datos no mostrados).
Tras la inducción de la dermatitis de contacto, las orejas fueron cortadas y rápidamente se analizaron sus pesos, observándose un mayor incremento de peso debido a la formación del edema, con respecto a la sana, en los ratones cuyas dietas contenían aceite de girasol solamente (168,041 ± 20,16 vs 113,024 ± 11,9 expresado en %, p = 0,0003) (fig. 4A); su peso seco se determinó viéndose que en ambos grupos se adquirían valores semejantes y que, por tanto, el incremento de peso experimentado, es exclusivamente debido a la extravasación de líquidos y a la migración de células hacia el foco inflamatorio. Se evaluó el contenido de líquido de las orejas, comprobándose que también era muy superior en el grupo de ratones alimentados con ácidos grasos w-6 (19,4± 4,5 vs 3,94 ± 2,92 mg, p = 0,002) (fig. 4B).
Se determinaron otros parámetros que aportasen más datos sobre el concurso del proceso inflamatorio, En este sentido, el glutatión de las orejas de los ratones que consumieron dietas ricas en ácidos grasos w-3, era significativamente superior al del grupo control (61,04 ± 4,5 vs 123,69 ± 24,2 expresado en %, p = 0,02) (fig. 4C).
La mayor gravedad de la inflamación también fue corroborada con la medida de la actividad mieloperoxidasa. Esta enzima está presente en los gránulos de los neutrófilos y cataliza la producción de HClO, constituyendo un marcador sensible de infiltración de neutrófilos y de inflamación. Se observó una mayor infiltración leucocilaria en las orejas inflamadas de ratones que habían consumido aceite de girasol (163,19 ± 52,9 vs 1.009,74 ± 404,69 expresado en %, p = 0,014) (fig. 4D).
Todos estos resultados indican que la incorporación a la dieta de los ácidos grasos w-3 produce una regulación del sistema inmunológico que hace que el individuo esté menos predispuesto a padecer procesos inflamatorios. La modificación de un gran número de parámetros sistémicos entre los que destaca el incremento de la IL-10, podrían ser los responsables de la protección ejercida por los ácidos grasos w-3 de la dieta.
Discusión
Entre los ácidos grasos, los de la serie w-3 parecen ser los de mayor actividad inmunomoduladora y dentro de los w-3, son los derivados del pescado, EPA y DHA, los biológicamente más activos4. Numerosos experimentos en animales y estudios de intervención clínica indican que los ácidos grasos w-3 poseen propiedades antiinflamatorias y que por tanto podrían ser útiles en el tratamiento de enfermedades inflamatorias, y autoinmunes.
La primera evidencia de la importancia de incluir ácidos grasos w-3 en la dieta a nivel de inflamación, surgió por observaciones epidemiológicas de la baja incidencia de enfermedades autoinmunes e inflamatorias en los esquimales de Groenlandia. Poco más tarde se producía un periodo de expansión en el conocimiento de los PUFA en general, y de los w-3 en particular4.
]]> Actualmente se sabe que los ácidos grasos w-3 son esenciales para el normal crecimiento y desarrollo del individuo y que juegan un papel clave en la prevención y tratamiento de enfermedades cardiovasculares, hipertensión o artritis entre otros4.Desafortunadamente, en las dietas occidentales predomina el consumo en exceso de ácidos grasos w-6, metabólicamente distintos a los w-3 y con funciones fisiológicas generalmente opuestas. Este desequilibrio contribuye al aumento en la incidencia de problemas cardiovasculares y desórdenes inflamatorios4. Por todo ello, se convierte en un reto para numerosos científicos, el demostrar y dar explicación al efecto antiinflamatorio de los ácidos grasos w-3.
Nuestros resultados sugieren que los ácidos grasos w-3 disminuyen la proliferación de linfocitos probablemente debido al efecto que ejercen sobre la producción de IL-2 y otras citocinas implicadas en la proliferación y diferenciación linfocitaria. Estos mismos resultados han sido encontrados por numerosos estudios en animales de experimentación12,13. En estudios clínicos en humanos donde se incluyeron ácidos grasos w-3 también se han analizado estos parámetros, encontrándose disminución de proliferación de linfocitos, aunque en este caso sin afectarse los niveles de IL-214. Sin embargo, los resultados aportados por los estudios en humanos son conflictivos, encontrándose algunos trabajos, incluso del mismo grupo, donde no se modifica15 o hasta se aumenta16 la proliferación de linfocitos. Estas diferencias pueden ser debidas a: Las dosis de ácidos grasos probados en estudios humanos no se pueden comparar con las elevadas dosis administradas en animales; los preparados de aceite de pescado que se utilizan en los diferentes estudios varían sus concentraciones de EPA y DHA pudiendo variar también los efectos, y por último la mayoría de los estudios humanos no han sido lo suficientemente consistentes para tener en cuenta la gran variación en algunos parámetros de la respuesta inmunológica.
Los ácidos grasos w-3, además de disminuir la producción de la citocina IL-2, disminuye otra serie de citocinas también Th1, como son la IL-1ß y el TNFα producidas por macrófagos. En humanos sanos, los niveles de ambas citocinas también son regulados por los ácidos grasos w-317 sugiriéndose que el efecto antiinflamatorio podría estar mediado por la modulación ejercida sobre estas citocinas.
Respecto a la respuesta Th2, nuestro estudio demuestra también una disminución de la misma puesto que hemos observado una reducción de los niveles séricos de histamina, IgE e lgG1, así como de citocinas Th2 como la IL-4. Hay diversas evidencias epidemiológicas que apoyan el papel protector de los ácidos grasos w-3 en enfermedades de tipo alérgico. Sin embargo, estudios usando suplementos de pescado en asma revelan un escaso impacto clínico a pesar de los cambios bioquímicos significativos que se producen18. Aún así, se están realizando nuevos estudios en asma y otras atopias con el fin de mejorar el curso de la enfermedad.
Diversos autores defienden otro tipo de ácidos grasos diferentes a los w-3 por pensar que pudiese llegar a un estado de inmunosupresión que dejase al individuo desprotegido y comprometiese su estado de salud19. Sin embargo, nuestros resultados sugieren que los ácidos grasos w-3 son capaces de potenciar algunas defensas del organismo, como por ejemplo la inmunoglobulina A, cuyo incremento puede estar también potenciado por el aumento de IL-10 que induce el cambio de isotipo de las inmunoglobulinas. En este estudio también se observa el incremento en la expresión de iNOS en macrófagos que supondría una ayuda frente a un ataque externo.
En nuestra opinión, el resultado más relevante y novedoso de este estudio es el incremento de la citocina reguladora IL-10, la cual podría ser considerada responsable del efecto antiinflamatorio de los ácidos grasos w-3, así como del antialérgico, ya que el poder inmunosupresor de dicha citocina podría disminuir las respuestas tanto Th1 como Th2.
Diversos estudios, como los realizados en modelos de pancreatitis experimental20 donde se aplicó nutrición parenteral con aceite de pescado, coinciden en que los ácidos w-3 inducen un incremento de los niveles de IL-10. Sin embargo, otros autores no observan diferencias21 o incluso perciben una disminución de la IL-1022 en otros modelos. Sería recomendable profundizar en este hecho para tratar de concretar el papel de la IL-10 en el mecanismo de acción de los ácidos grasos w-3 por lo que estudios con Knock-out para IL-10 están previstos realizarse en nuestros laboratorios.
El modelo de dermatitis de contacto empleado en este estudio, permite la observación a simple vista del efecto antiinflamatorio de la dieta enriquecida en ácidos grasos w-3. Los valores del peso de las orejas y del contenido de agua de las mismas ya refleja el claro efecto amiinflamatorio del aceite de pescado. Que el peso y el contenido de agua de las orejas inflamadas de ratones alimentados con w-3 fuese menor era indicativo de que en dicho grupo la vasodilatación había sido menos drástica y por tanto el edema más leve. Estudios japoneses confirman estos efectos en un mode-lo similar, atribuyendo en ese caso el efecto al mayor poder del DHA7. Un estudio semejante, usando esteres de phorbol (TPA) como agente irritante, también señala el poder antiinflamatorio, en este caso por igual, de DHA y EPA23.
La medida de MPO pone de manifiesto una menor infiltración leucocitaria con el tratamiento de ácidos grasos w-3. La migración de leucocitos desde la microvasculatura hasta el foco de la lesión donde se acumulan, es un paso clave característico de la inflamación aguda23,7. Los ácidos grasos w-3 parecen poseer un importante papel a este nivel ya que en dicho grupo apenas se percibe el fenómeno.
]]> Los radicales libres asociados a la inflamación llevan a estrés oxidativo, involucrado en el agravamiento de numerosas enfermedades. El glutatión es un tripéptido de elevada capacidad antioxidante al que recurre el organismo para la neutralización de los radicales libres. En las orejas de ratones donde se indujo la dermatitis de contacto los niveles de glutatión disminuyen significativamente al hacer frente al estrés oxidativo generado. Sin embargo, en el grupo w-3 esta disminución está reducida o compensada ya que al ser el daño menor, su efecto antioxidante no es tan requerido. Estos resultados podrían sugerir que los ácidos grasos w-3 aumenten los niveles de glutatión, pero, al analizarse el contenido de glutatión en el hígado de todos los roedores no se observaron diferencias. Sin embargo, sí que existen estudios que relacionan el consumo de ácidos grasos w-3 con un incremento en las defensas antioxidantes24,25.Podemos concluir atribuyéndoles a los ácidos grasos w-3 un potente papel antiinflamatorio donde el aumento de la IL-10 parece ser el factor desencadenante de una serie de modificaciones en la respuesta inmunológica que llevan a dicho efecto. La disminución de la proliferación de linfocitos y de las respuesta de tipo Th1 y Th2 son algunas de estas modificaciones. El estudio del efecto de los ácidos w-3 a nivel de vías de transducción de señales se hace imprescindible para terminar de dar explicación a la gran actividad de estos compuestos, no solo a nivel de inflamación sino también a nivel de alergia.
Referencias
1. Kelley D: Modulation of human immune and inflammatory responses by dietary fatty acids. Nutrition 2001, 17(7/8):669-673. [ Links ]
2. Calder PC: n-3 Polyunsaturated fatty acids and inflammation: from molecular biology to the clinic. Lipids 2003, 38:323-352. [ Links ]
3. Harbige LS: Fatty acids, the immune response, and autoimmunity: a question of n-6 essentiality and the balance between n-6 and n-3. Lipids 2003, 38:323-341. [ Links ]
4. Simopoulos AP: Omega-3 fatty acids in inflammation and autoinnumme diseases. J Am Coll Nutr 2002,21 no.6:495-505. [ Links ]
5. Calder PC: Fat chance of immunomodulation. Trends immunol today 1996, 19, no 6:244-247. [ Links ]
6. Yaqoob P: Lipids and the immune response: from molecular mechanism to clinical applications. Curr Opin Nutr Metab Care 2003, 6:133-150. [ Links ]
7. Tomobe YI, Morizawa K, Tsuchida M, Hibino H, Nakano Y, Tanaka Y: Dietary docosahexaenoic acid suppresses inflammation and immunoresponses in contact hypersensitivity reaction in mice. Lipids 2000, 35, no. 1:61-69. [ Links ]
8. Anderson ME: determination of glutathione and glutathione disulfide in biological samples. Meth Enzymol 1985, 113:548-555. [ Links ]
9. Krawisz YE, Sharon P, Stenson WF: Quantitative assay for acute intestinal inflammation based on myeloperoxidase activity. Assessment of inflammation in rat and hamster models. Gastroenterology 1984, 87:1344-1350. [ Links ]
10. Kelley DS, Warren JM, Simon VA, Bartolini G, Mackey BE, Erickson KL: Similar effects of c9,t11-CLA and t10,cl2CLA on immune cell functions in mice. Lipids 2002, 37:725-728. [ Links ]
11. Xaus J, Cardó M, Vellador AF, Soler C. Lloveras J, Celada A: Interferon gamma induces the expression of p21waf1 and arrests macrophage cell cycle preventing induction of apoptosis. Immunity 1990, 2:103-113. [ Links ]
12. Peterson LD, Thies F, Sanderson P, Newsholme EA, Calder PC: Low levels of eicosapentaenoic and docosahexaenoic acids mimic the effect of fish oil upon rat lymphocytes. Life Sci 1998, 62(24):2209-2017. [ Links ]
13. Peterson LD, Jeffery NM, Thies F, Sanderson P, Newsholme EA y Calder PC: Eicosapentaenoic and docosahexaenoic acids alter rat spleen leukocyte fatty acids composition and prostaglandin E2 production but have different effects on lymphocyte function and cell-cell mediated immunity. Lipids 1998, 33(2):171-180. [ Links ]
14. Thies F, Neve-von-Caron G, Powell JR, Yaqoob, P, Newsholme EA, Calder PC: Dietary supplementation with gamma-linolenic acid or fish oil decreases T lymphocyte proliferation in healthy older human. J Nutr 2001, 131(7):1918-1927. [ Links ]
15. Kew S, Benerjee T, Minihane AM, Finnegan YE, Muggli R, Albers R, Williams CM, Calder PC. Lack of effect of foods enriched with plant-ormarine-derived n-3 fatty acids on human immune functions. Am J Clin Nutr 2003, 77(5):1287-1295. [ Links ]
16. Trebble TM y cols.: Prostaglandin E2 production and T cell function after fish oil supplementation: response to antioxidant cosupplementation. Am J Clin Nutr 2003, 78(3):376-382. [ Links ]
17. Endres S y cols.: The effect of dietary supplementation with n-3 fatty acids on the synthesis of interleukin-1 and tumor necrosis factor by mononuclear cells. N Engl J Med 1989, 320(5):265-271. [ Links ]
18. Calder PC, Yaqoob P, Thies F, Wallace FA y Miles EA: Fatty acids and lymphocyte functions. Brit J Nutr 2002, 87 Suppl. 1, S31-S48. [ Links ]
19. Puertollano MA, De Pablo M, Álvarez de Cienfuegos G: Anti-oxidant properties of N-acetyl-cystcine do not improve the immune resistance of mice fed dietary lipids to Listeria monocytogenes infection. Clin Nutr, 2003, 22(3):313-319. [ Links ]
20. Foitzik T, Eibl G, Schneider P, Wenger FA, Jacobi CA, Buhr HJ: Omega-3 fatty acids supplementation increases anti-inflammatory cytokines and attenuates systemic disease sequelae in experimental pancreatitis. Parenter Enteral Nutr, 2002, 26(6):351-356. [ Links ]
21. Wallace FA, Miles EA, Calder PC: Comparison of the effects of linseed oil and different doses of fish oil on mononuclear cell function in healthy human subjets. Br J Nutr 2003, 89(5):679-681. [ Links ]
22. Hayashi y cols.: Effects of intravenous omega-3 and omega-6 fat emulsion on cytokine production and delayed type hiper-sensitivity in burned rats receiving total parenteral nutrition. J Parenter Enteral Nutr 1998, 22(6):363-367. [ Links ]
23. Raerlerstorff D, Pantze M, Bachmann H, Moser U: Anti-inflammatory properties of docosahexaenoic and eicosupentaenoic acids in Phorbol-ester-induced mouse ear inflammation. Int Arch Allergy Immunol 1996, 111(3):284-290. [ Links ]
24. Jolly CA, Muthukumar A, Avula CP, Troyer D, Fernandes G: Life span is progonged in food-restricted autoimmune-prone (NZBxNZW)F(l) mice fed a diet enriched with (n-3) fatty acids. J Nutr 2001, 131(10):2753-60. [ Links ]
25. Demoz A, Willumsen N y Berge RK: Eicosapentaenoic acid at hypotriglyceridemic dose enhances hepatic antioxidant defense in mice. Lipids 1992, 27(12):968-971. [ Links ] ]]>