Consecuencias clínicas de las alteraciones neuromusculares en el paciente crítico
Clinical consequences of neuromuscular impairments in critically ill patients
A. Mesejo, E. Pérez-Sancho y E. Moreno
Servicio de Medicina Intensiva. Hospital Clínico Universitario de Valencia.
Dirección para correspondencia
]]>
RESUMEN
La patología neuromuscular en el paciente crítico se desarrolla en dos contextos: enfermedades neurológicas primarias que requieren su ingreso en Medicina Intensiva por necesitar vigilancia estricta o ventilación mecánica y manifestaciones del sistema nervioso periférico secundarias a enfermedades sistémicas críticas. En el primer grupo son las más frecuentes el Síndrome de Guillain-Barré y la Miastenia Gravis y en el segundo la Polineuropatía y la Miopatía del paciente crítico.
El patrón clínico común más frecuente consiste en el desarrollo de un cuadro de acusada debilidad y cuadriparesia cuya manifestación más típica es la necesidad de respiración asistida o la dificultad/imposibilidad para su retirada. Se consideran factores desencadenantes el fracaso multiorgánico y la sepsis en la polineuropatía y los esteroides y bloqueantes neuromusculares en la miopatía, actuando como coadyuvantes en ambos casos la malnutrición, particularmente la hipoalbimunemia, y la hiperglucemia. Considerando que la afectación neuropática y miopática coexisten con frecuencia, se ha acuñado el término polineuromiopatía del paciente crítico.
Tanto el Síndrome de Guillain-Barré como la polineuropatía del paciente crítico se localizan a nivel del nervio periférico, por lo que debe efectuarse un diagnóstico diferencial entre ambos. La forma de presentación es diferente ya que el primero es una patología aguda que motiva su ingreso en UCI, mientras que la polineuropatía se adquiere durante la hospitalización. En el primero es frecuente la afectación del sistema nervioso autónomo y la disociación albúmino-citológica en el LCR, lo que no se da en la polineuropatía. Los estudios electrofisiológicos muestran signos de desmelinización con disminución de la velocidad de conducción y normalidad en la amplitud de potenciales motores en el Síndrome de Guillain- Barré frente a velocidad de conducción normal y amplitud reducida de potenciales motores en la polineuropatía axonal.
La crisis miasténica afecta a la unión neuromuscular y su diagnóstico suele ser más fácil al tener en la mayoría de los casos un diagnóstico previo de miastenia gravis.La debilidad muscular aumenta durante la actividad repetida (fatiga muscular) y mejora con el reposo. Su confirmación diagnóstica se realiza con el test del edofronio y con la estimulación nerviosa repetitiva, que provoca una rápida disminución del 10-15% en la amplitud de las respuestas provocadas.
La miopatía del paciente crítico se localiza en el músculo y provoca una debilidad generalizada con cuadriparesia, muy similar a la de la polineuropatía, que impide o retrasa la desconexión de la ventilación mecánica y que en sus grados avanzados puede provocar un aumento de CPK y mioglobina, junto con alteraciones en la exploración neurofisiológica. Esta última es difícil de discernir de la encontrada en la polineuropatía, aunque la normalidad en los potenciales de acción sensitiva y la redución en el potencial de ación motora con estimulación muscular directa, puede ayudar a diferenciarlos.
El pronóstico funcional de las alteraciones musculares primarias suele ser bastante bueno, pero tanto la polineuropatía como la miopatía evolucionan lentamente a lo largo de semanas o meses, pudiendo quedar un importante déficit residual a los dos años en los casos más graves.
Palabras clave: Polineuropatía. Miopatía. Nutrición. Patología neuromuscular.
ABSTRACT
]]> Neuromuscular pathology in the critically ill patient develops within two settings: primary neurological diseases that require admission in the Intensive Care Medicine Unit for close monitoring or mechanical ventilation, and peripheral nervous system manifestations secondary to critical systemic diseases. The most frequent conditions in the first group are Guillain-Barré syndrome and Myasthenia Gravis, and in the second group, polyneuropathy and myopathy of the critically ill patient.Key words: Polyneuropathy. Myopathy. Nutrition. Neuromuscular Pathology.
Introducción
La patología neuromuscular puede ser causa de ingreso de un paciente en Medicina Intensiva o puede desarrollarse como consecuencia de la evolución y tratamiento de otra enfermedad crítica. De esta forma nos encontramos con dos contextos: enfermedades neurológicas primarias que requieren ingreso en Cuidados Intensivos por necesidad de vigilancia estricta y/o ventilación mecánica y manifestaciones del sistema nervioso periférico (SNP) secundarias a enfermedades sistémicas críticas que con frecuencia suelen asociarse a un fracaso multiorgánico (FMO).
]]> De esta forma las subdividimos en:- Enfermedades neuromusculares, agudas o crónicas, que precipitan la enfermedad crítica.
- Enfermedades neuromusculares que se desarrollan de forma secundaria a la enfermedad crítica y a su tratamiento.
En la tabla I se presenta un listado con todas ellas, algunas absolutamente anecdóticas. Nos centraremos en las que tienen más trascendencia, tanto por su frecuencia como desde el punto de vista clínico y/o de diagnóstico diferencial. En el primer grupo, el Síndrome de Guillain-Barré (SGB) y la Miastenia Gravis (MG) y en el segundo grupo la Polineuropatía del paciente crítico (PPC) y la Miopatía del paciente crítico (MPC).
La patología del primer grupo es conocida desde tiempo atrás. No sucede igual, sin embargo, con la del segundo grupo ya que con los nuevos tratamientos aplicados a los pacientes críticos y las posibilidades de recuperación que antes no existían, con cierta frecuencia se encuentran disfunciones de órganos o sistemas no relacionados con el inicialmente afecto. Este es el caso de las alteraciones neuromusculares adquiridas que pueden afectar, de forma aislada o conjunta, al nervio, unión neuromuscular o músculo.
Antiguamente se pensaba que la debilidad muscular secundaria era consecuencia exclusiva de la inmovilidad prolongada y el catabolismo asociado con una enfermedad postrante. Hoy sabemos que el paciente grave puede padecer fenómenos como la polineuropatía o la miopatía asociada con el paciente crítico, que exacerba la debilidad muscular en este grupo de riesgo.Su frecuencia subraya la importancia de las medidas para preservar la función muscular en estos pacientes.
El patrón clínico más frecuente consiste en el desarrollo de un cuadro de acusada debilidad cuya manifestación más típica es la necesidad de respiración asistida o la dificultad/imposibilidad para la desconexión del respirador1. Teniendo en cuenta el estado clínico general del paciente y su presumible poca colaboración, existen dificultades para la valoración mediante tests que miden la fuerza muscular. En ausencia de enfermedad pulmonar o esquelética, una disminución de la capacidad vital forzada (CVF) por debajo del 50% (valor normal 65-75 ml/kg) sugiere marcada debilidad de la musculatura respiratoria y, por tanto, posibilidad de fracaso ante la desventilación.
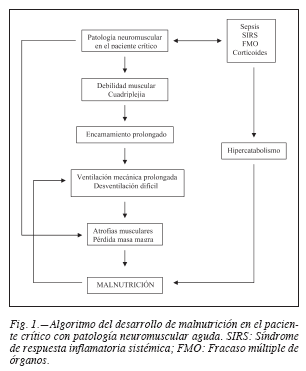
Entre los factores desencadenantes más comunes se encuentran el fracaso multiorgánico (FMO) y la sepsis en la polineuropatía2-4 y los esteroides y bloqueantes euromusculares en la miopatía5,6. Los agentes bloqueadores de la unión neuromuscular, que se utilizan para controlar la insuficiencia respiratoria grave y el Síndrome del Distress Respiratorio Agudo (SDRA), se asocian con la inducción de debilidad muscular y parálisis prolongada, bien por una prolongación de sus efectos o como factor desencadenante de una miopatía7,8. Actúan como coadyuvantes en ambos la malnutrición en general y la hipoalbuminemia en particular, así como la hiperglucemia9.10. Aunque se considera que la malnutrición puede ayudar en su desarrollo, es vidente que también es una consecuencia directa de estas alteraciones y de la patología acompañante (fig. 1), por lo que deberá ser uno de los pilares importantes en el tratamiento. Hay que recordar que la respuesta al estrés en el paciente crítico se caracteriza, entre otros hallazgos, por un exacerbado hipercatabolismo proteico con aumento en la eliminación de nitrógeno. Mediante biopsias musculares en pacientes críticos, se ha constatado un marcado descenso de la concentración total de aminoácidos y particularmente de glutamina, que puede llegar a ser hasta de un 72%11, con un aumento paralelo de los aminoácidos de cadena ramificada, por lo que la concentración muscular de glutamina parece un excelente marcador del catabolismo proteico en el músculo y puede ser aplicado a los pacientes con patología neuromuscular, no solo desde el punto de vista diagnóstico sino también evolutivo.
La incidencia de PPC y MPC es superior al 70% en los casos de pacientes críticos graves, aunque la afectación es con frecuencia subclínica o poco relevante. Sin embargo, en los últimos años está ganando adeptos, dentro del confuso marco de la terminología, el término polineuromiopatía del paciente crítico (PNMPC) como concepto de enfermedad neuromuscular adquirida en Medicina Intensiva, debido a que ambas entidades con frecuencia se dan de forma simultánea, las manifestaciones clínicas son casi superponibles y la exploración neurofisiológica denota cambios similares en muchos aspectos en ambas.
]]> Vamos a analizar las consecuencias clínicas en las cuatro entidades responsables, en mayor grado, de las alteraciones neuromusculares en el paciente crítico
Síndrome de Guillain-Barré
Es una polirradiculoneuropatía desmielinizante inflamatoria aguda de carácter periférico, predominantemente motor, con un comienzo subagudo-agudo,una evolución monofásica y un máximo dentro de las 4 semanas, aunque en ocasiones adquiere un carácter grave e incluso fulminante. Su frecuencia es de 1.3 casos/100.00 habitantes/año12. Más del 90% sufren una neuropatía desmielinizante y un 5% una axonopatía primaria. El 75% de los casos está precedido en 1-3 semanas de un proceso infeccioso agudo, respiratorio o gastrointestinal (Campylobacter jejuni, herpes, citomegalovirus, mycoplasma pneumoniae). Esta frecuente asociación de infecciones precedentes sugiere que se puede producir una respuesta inmunológica con anticuerpos que reaccionan en forma cruzada con los gangliósidos de los nervios periféricos.
Los primeros hallazgos consisten en debilidad aguda rápidamente progresiva, generalmente de inicio en las piernas, con o sin alteraciones sensitivas asociadas13. El patrón más habitual es una parálisis ascendente que el paciente nota inicialmente como un acorchamiento de las piernas. La debilidad evoluciona en horas o días, acompañada de disestesias, con mayor afectación de miembros inferiores que superiores y en un 50% con parálisis facial. Cuando hay afectación de los pares craneales a nivel bulbar, manifestado por disfonía, dificultad en la deglución o protusión lingual, se produce un mal manejo de secreciones e insuficiencia respiratoria aguda que requiere ventilación mecánica en un 30% de los casos14. Al inicio, en las formas puras, no existe fiebre ni otra sintomatología general. Los reflejos osteotendinosos a menudo están marcadamente reducidos o ausentes en el momento de la presentación, pero con frecuencia este hallazgo puede tardar varios días en producirse. La sensibilidad superficial suele estar solo ligeramente afectada. Una vez estabilizado el proceso, sin nuevos signos de progresión, la recuperación suele ser relativamente rápida.
Se ha intentado establecer parámetros de evaluación prospectivos que nos orienten respecto de aquellos pacientes que necesitarán ventilación mecánica (VM). En ese sentido, se ha comprobado15 que los pacientes que precisaron ventilación mecánica fueron los que presentaron una disminución de la capacidad vital (CV) en las 48 horas precedentes, mientras que ésta permaneció estable en aquellos que no la precisaron. Los que necesitaron VM tenían una CV media de 15,2 ml/kg mientras que en los que no fue necesaria era superior a 40 ml/kg. La medida de la frecuencia respiratoria, sin embargo, no es un buen parámetro predictivo ya que las fluctuaciones que presenta, en ambos grupos, reduce su valor pronóstico. La aparición de clínica de afectación bulbar, sin embargo, si que es indicativa de probable necesidad de ventilación mecánica.
En los casos graves se afecta con frecuencia el sistema nervioso autónomo16, con una disfunción que se manifiesta como un estado hipersimpático que provoca una taquicardia sinusal mantenida y poco explicable por otras causas. En raras ocasiones pueden aparecer episodios de bradicardia, incluso con necesidad de marcapasos transitorio y síndrome bradicardia-taquicardia que obliga a un estrecho control. La tensión arterial puede fluctuar ampliamente. Es característica la presencia de dolor, bien en la musculatura afecta con disestesias en extremidades o en la columna vertebral. Todo ello mejora paralelamente al cuadro general.
Una complicación frecuente es la trombosis venosa profunda, lo que debe tenerse en cuenta a la hora de planificar el tratamiento. Precisamente, con independencia de las complicaciones inherentes a la posible ventilación mecánica prolongada, actualmente se considera que la disfunción autonómica, junto con el tromboembolismo pulmonar son las causas principales de mortalidad en este Síndrome.
El encamamiento prolongado, además, puede desencadenar importantes atrofias musculares, por lo que debe planificarse desde el principio un soporte nutricional adecuado y un tratamiento rehabilitador precoz. Dado que no existe afectación de la conciencia, en ocasiones es precisa una sedación suave, sobre todo en los casos más graves con necesidad de ventilación mecánica prolongada. Debe tenerse en cuenta este hecho a la hora de evaluar evolutivamente la exploración neurológica, que puede encontrarse total o parcialmente enmascarada.
En los casos típicos, los hallazgos del líquido cefalorraquídeo (LCR) muestra una disociación albúminocitológica con hiperproteinorraquia (100-1.000 mg/dl) sin pleocitosis, aunque en las primeras 48-72 h puede ser normal o incluso no evolucionar hasta la segunda semana de la enfermedad16. El examen del LCR puede excluir o confirmar otros diagnósticos y la pleocitosis linfocítica (20-50 cel/mm3) puede indicar una infección aguda por el virus de la inmunodeficiencia humana (VIH), no conocida.
]]> Los estudios electrodiagnósticos (conducción nerviosa motora y sensitiva y electromiografía con aguja) (tabla II), ponen de manifiesto unas alteraciones que son leves o inexistentes en las fases iniciales y quevan por detrás de la evolución clínica. A menudo reflejan desmielinización nerviosa segmentaria con latencias distales prolongadas y bloqueos multifocales de la conducción, amplitudes dispersas del potencial de acción muscular compuesto (PAMC), disminución de la velocidad de conducción y prolongación o ausencia de las ondas F. En un 5% de los casos se observa una afectación axonal primaria, apreciándose una disminución de los potenciales de acción compuestos, sin retraso de la conducción ni prolongación de las latencias distales17,18, lo que puede confundirlo con una PPC, debiendo hacerse hincapié en las manifestaciones clínicas y forma de presentación para su diagnóstico diferencial.El diagnóstico global se establece por un patrón de parálisis de rápida evolución con arreflexia, ausencia de fiebre y otros síntoma generales (tabla III). El diagnóstico diferencial debe realizarse con las patologías enumeradas en el apartado "nervio periférico" de la tabla I. Considerando que en la primera semana las pruebas complementarias pueden ser anodinas (analítica, EMG, LCR), en el caso de sospecharse un SGB debe iniciarse el tratamiento de inmediato ya que la evolución clínica a corto plazo puede depender de ello.
Miastenia Gravis
La Miastenia Gravis es consecuencia de un reacción autoinmne sobre el complejo del receptor de acetilcolina en la membrana postsináptica de la unión neuromuscular. No es una patología infrecuente y su prevalencia es de 14,2 casos/100.000 habitantes, mas en mujeres en tercera y cuarta década de la vida y varones en sexta y séptima19, constatándose en un 10% de los casos la existencia de un tumor tímico (timoma), e hiperplasia tímica en la mayoría de los demás. Hasta el 20% de los pacientes afectados tienen crisis miasténicas con insuficiencia respiratoria que exige ventilación mecánica20. El precipitante más común de la crisis miasténica es la infección broncopulmonar.
La clínica característica de la MG es debilidad muscular con fatigabilidad progresiva. La debilidad presenta un patrón fluctuante, aumentando durante la actividad repetida (fatiga) y mejorando tras el reposo o el sueño. En los casos típicos, los músculos craneales, faciales y extraoculares, se afectan precozmente con diplopia, ptosis, facies inexpresiva, dificultad masticatoria y voz pastosa o disártrica. Puede conducir a dificultades en la deglución con fenómenos de regurgitación o aspiración. En el 85% de los pacientes la debilidad se generaliza y afecta a los miembros, con frecuencia de forma proximal y asimétrica, con reflejos tendinosos y sensibilidad conservados.
Cuando se afecta la musculatura respiratoria y la deglución se habla de crisis miasténica severa que puede precisar soporte ventilatorio. A diferencia de lo que acontece en el SGB, se ha comprobado que en la miastenia la CV no tiene valor predictivo para una probable necesidad de ventilación mecánica, incluso en pacientes con valores inferiores a 10-15 ml/kg, dada la posible reversibilidad farmacológica del episodio agudo21. A este respecto, hay que considerar que en la crisis miasténica la dosificación excesiva con inhibidores de la colinesterasa puede superponer al cuadro clínico una crisis colinérgica, lo que produce de forma paradójica un aumento de la debilidad muscular. Una vez estabilizado el proceso se ha comprobado que la CV, al igual que en el SGB15, es útil para valorar el inicio del progresivo despegue del respirador, pudiendo comenzarse cuando se encuentra entre 7-15 ml/kg.
La evolución es variable con remisiones, raramente completas, y exacerbaciones, a menudo por procesos intercurrentes, que pueden conducir a una crisis miasténica severa.
El diagnóstico clínico de sospecha debe confirmarse para establecer un diagnóstico definitivo, normalmente con el test del edofronio (prueba de la anticolinesterasa) o con la presencia de anticuerpos anti-AChR en el suero (80% de los casos)22. Ante la aparición de insuficiencia respiratoria, debe establecerse el diagnóstico diferencial con el botulismo19, aunque la mayoría de los pacientes con miastenia ya tienen un diagnóstico previo establecido.
]]> Asimismo, el estudio electrofisiológico mediante la estimulación nerviosa repetitiva suele confirmar el diagnóstico20 (tabla II): la aplicación de descargas con una frecuencia de 2-3/seg en grupos musculares proximales de personas sanas no modifican la amplitud de los potenciales de acción de los músculos, mientras que en los pacientes miasténicos se produce una disminución rápida del 10-15% en la amplitud de las respuestas provocadas.
Polineuropatía del paciente crítico
Es una neuropatía periférica axonal difusa que fue reconocida y descrita en gran parte por Bolton y cols.23,24. Se desarrolla, sobre todo, en el contexto de enfermedades críticas de estancia prolongada con fracaso multiorgánico y sepsis. El daño axonal está relacionado con el Síndrome de Respuesta Inflamatoria Sistémica (SIRS), FMO y sepsis, al parecer a través dela liberación de citokinas, radicales libres y factores neurotóxicos que actúan directamente sobre la microcirculación25. No parece existir correlación entre la intensidad de la PPC medida por la intensidad de los cambios neurofisiológicos y la gravedad del FMO, la estancia o el tiempo de ventilación mecánica26,27. Se ha constatado en un grupo de pacientes con dificultades para la desconexión del respirador que la presencia de PPC afectaba a un 62% de ellos28. En un estudio que analizaba 43 pacientes con sepsis grave y fallo multiorgánico de forma prospectiva29, se ha llegado a documentar en un 70% de ellos algún grado de PPC con indicios electrofisiológicos de neuropatía axonal sensitivo- motora y en un 35% hubo dificultades para la desventilación, aunque sin duda son muchos menos los que tienen un síndrome lo suficientemente intenso como para necesitar ventilación mecánica y/o prolongar la desconexión del respirador. Asimismo, el tiempo total de ventilación mecánica es superior en pacientes con PPC30,31. Probablemente sea la causa neuromuscular más frecuente de dependencia prolongada del respirador en los pacientes sin enfermedad neuromuscular conocida previa32 y debe sospecharse en todo paciente que tras 2-3 semanas de estancia en Medicina Intensiva se recupera de un FMO previo, sepsis y patología de base y sin embargo presenta dificultades para la desconexión del respirador.
Dadas las limitaciones del examen neurológico motor y sensitivo en el contexto de la enfermedad crítica, con pacientes frecuentemente sedados, analgesiados y con frecuencia miorrelajados, es posible que no se valoren adecuadamente las características clínicas de esta polineuropatía, que cursa fundamentalmente con pérdida de fuerza generalizada, debilidad y atrofias musculares de las extremidades, hipoestesia distal y parestesias, con preservación de pares craneales. En general, los reflejos osteotendinosos están disminuidos o ausentes, aunque en el frecuente contexto de una patología superpuesta del sistema nervioso central (SNC) con disfunción del tracto piramidal, pueden ser normales o incluso exaltados33.
Ante la dificultad para calibrar la naturaleza de los hallazgos clínicos de esta entidad patológica, los estudios neurofisiológicos son importantes para su diagnóstico34 (tabla II). En ellos se demuestra la presencia de una neuropatía axonal sensitivo-motora difusa y simétrica. Los hallazgos de la conducción nerviosa incluyen valores de velocidad y de latencia de conducción normales o casi normales y amplitudes del PAMC y del potencial de acción de los nervios sensitivos (PANS) muy reducidos que traducen una lesión primaria axonal. El examen con electrodos de aguja pone en evidencia cambios denervatorios, que son más pronunciados en los músculos distales, y que se manifiestan por potenciales de fibrilación, ondas agudas positivas y una reducción del reclutamiento de potenciales de unidad motora35 (fig. 2-b). En conjunto, la PPC más frecuente es de predominio motor y ocasionalmente tieneun componente sensitivo27,36. Con la recuperación, la actividad espontánea cede y los potenciales de unidad motora se tornan polifásicos y grandes.
La histopatología de los nervios periféricos ha puesto en evidencia una degeneración axonal primaria difusa en las fibras motoras y sensitivas distales con poca o ninguna desmielinización, observándose así mismo un agrupamiento por tipo de fibras en el músculo esquelético24, ya que con frecuencia se asocia a una afectación muscular dando lugar a un cuadro mixto de polineuromiopatía.
En ocasiones, el diagnóstico diferencial clínico en un paciente con debilidad de las extremidades e incapacidad para ser separado de la ventilación mecánica entre dos trastornos neuropáticos periféricos como son el SGB y la PPC es complicado, si no está claramente diferenciada la forma de inicio. Si bien en algunos casosgraves de PPC se ha asociado con debilidad facial37, es sobre todo en el SGB donde es frecuente la debilidad facial y orofaríngea, así como disautonomía y ocasionalmente oftalmoplejía externa. Los hallazgos electrofisiológicos son también útiles para su diagnóstico diferencial. En el SGB, el número total de fibras está normal pero la mayoría tienen una disminución de su vaina de mielina. Sin embargo, en la PPC el número de fibras está reducido pero preserva su mielina (fig. 3). El estudio de la conducción nerviosa en el SGB tiene pues características de desmielinización (reducción de la velocidad de conducción, latencias distales y de onda F prolongadas, bloqueo de la conducción y dispersión temporal de los PAMC) con amplitud normal, lo que no aparece en la PPC y mediante electromiografía (EMG) de aguja, en el SGB se observa menos actividad espontánea que en la PPC, en los músculos clínicamente débiles, los primeros días.
La proteinorraquia media en los pacientes con PPC es significativamente más baja que en aquellos con SGB35. En la histopatología del nervio periférico, la PPC nopresenta la desmielinización y cambios inflamatorios segmentarios que se observan en el SGB24.
]]> Aunque el pronóstico global de la PPC depende de la patología subyacente, la mayoría de los pacientes que sobreviven experimentan una recuperación funcional en varios meses24, aunque los pacientes que han presentado una PPC grave permanecen a los dos años con graves secuelas y deterioro de la calidad de vida, siendo la mayor duración de la sepsis, la estancia prolongada en UCI y la disminución de masa magra los parámetros que se asocian con peor recuperación funcional38,39. La PPC prolonga la dependencia del respirador pero no empeora per se el pronóstico a largo plazo. Se ha constatado un aumento de la estancia hospitalaria en estos pacientes30 pero no está claro que exista un aumento de mortalidad en los pacientes con PPC respecto de los que no la tienen31.
Miopatía del paciente crítico
Este síndrome fue descrito en 1977 en una mujer joven que experimentó una miopatía grave tras el tratamiento de un estatus asmático con corticosteroides a dosis elevadas y pancuronio40. Tras ella se ha descrito en muchos pacientes con patología crítica sin enfermedad neuromuscular preexistente. Se ha desarrollado con mayor frecuencia en los casos de insuficiencia respiratoria aguda grave y/o SDRA en donde se ha utilizado miorelajantes para facilitar la ventilación mecánica y administrado simultáneamente corticosteroides a altas dosis.
Sin embargo, la terminología sigue estando confusa encontrándose distintos tipos y/o grados de dicha miopatía41,42. Así, se sabe que un elevado porcentaje de pacientes críticos experimentan con frecuencia una marcada atrofia muscular, incluso con un aporte nutricional adecuado. Se ha supuesto que esta atrofia y la consiguiente pérdida de fuerza representa una miopatía catabólica, consecuencia de múltiples factores, como el aumento de la liberación de cortisol, catecolaminas y otros mediadores inducidos por el síndrome de respuesta inflamatoria sistémica (SIRS). Se le denomina miopatía caquéctica y en ella la CPK y el EMG son normales.
En el contexto de un agravamiento del paciente o por el mantenimiento del estado hipercatabólico, puede combinarse con un grado más avanzado, la denominada miopatía de filamentos gruesos, con un selectivo descenso de los filamentos de miosina y que se caracteriza por una pérdida de fuerza que progresa hasta un grado muy intenso en varios días. Puede asociarse un aumento de CPK y mioglobina, aunque tanto el EMG como la biopsia muscular pueden ser normales al principio.
El grado más avanzado es la llamada miopatía aguda necrotizante, considerada por algunos como la miopatía del paciente crítico propiamente dicha, que describe un síndrome clínico de intensa pérdida de fuerza que aparece en el contexto de tratamiento con corticoides y miorrelajantes. No se trata de una acción prolongada de los bloqueantes en la unión neuromuscular sino de una auténtica miopatía con lesión muscular. También se ha descrito en los pacientes que reciben, además de corticoides a altas dosis, propofol y benzodiacepinas en dosis hipnóticas43, remarcándose a importancia de la administración de corticoides en el desarrollo de esta entidad, como se ha visto también en el desarrollo de esta miopatía tras el trasplante de órganos en los que se administran altas dosis para evitar el rechazo44. Aunque la mayoría de los casos se dan con la asociación de enfermedad crítica, corticoides y miorrelajantes, ocasionalmente puede aparecer con solo alguno de esos factores aislado.
Se ha propuesto45 que el término miopatía del paciente crítico sea un término amplio que describa tanto aquellas miopatías con afectación funcional pura e histología normal como aquellas con atrofia y necrosis, con unos criterios que abarquen la clínica, electrofisiología, histopatología y bioquímica46.
Puede aparecer aislada o asociada a PPC, habiendo estado durante mucho tiempo infradiagnosticada por su similitud clínica con la neuropatía. En realidad, con frecuencia resulta imposible la diferenciación entre ambas entidades, tanto por la clínica como por las exploraciones neurofisiológicas.
Clínicamente suele reconocerse cuando un paciente no puede abandonar la ventilación mecánica aún habiendo superado la causa subyacente. La presentación clínica más frecuente consiste en debilidad y flacidez que tiende a ser difusa, afectando a músculos de extremidades, flexores del cuello, musculatura facial y diafragmática, muy similar a la clínica de la PPC. En los casos típicos se desarrolla una cuadriparesia difusa y flácida con compromiso de los músculos respiratorios y atrofia muscular tras varios días. En raras ocasiones se ha observado una oftalmoparesia externa. La sensibilidad permanece intacta pero los reflejos osteotendinosos están reducidos o ausentes. Habitualmente la CPK está elevada pero fundamentalmente en la fase inicial, siendo sus niveles normales en el 50% por lo que no es útil para diferenciarlos.
]]> Estos pacientes suelen ser incapaces de realizar movimientos voluntarios, por lo que es complicado registrar potenciales de unidad motora en el EMG lo que hace que en el estudio neurofisiológico con frecuencia solo se evidencien las alteraciones de la conducción nerviosa, siendo diagnosticados de PPC, cuando con frecuencia se trata de una entidad mixta. Los hallazgos electrofisiológicos incluyen PAMC reducidos con velocidades de conducción nerviosa normales, al igual que en la PPC (tabla II). Sin embargo, los PANS pueden ser normales, lo que puede ayudar a diferenciarlos. La recuperación clínica se acompaña de una mejoría en la amplitud de la onda M47. Los estudios de estimulación nerviosa repetitiva pueden dar respuestas decrementales mientras persistan los efectos de los miorrelajantes. Los potenciales de denervación igual pueden estar ausentes como ser muy evidentes48 aunque en general la EMG con aguja a menudo muestra potenciales de unidad motora polifásicos de baja amplitud que exhiben reclutamiento rápido, junto con ondas agudas positivas y potenciales de fibrilación (fig. 2-c).Se ha propuesto la combinación de la estimulación muscular directa con el registro estándar para un mejor diagnóstico. Un paciente con neuropatía presenta un potencial de acción reducido o ausente con la estimulación convencional, pero normal cuando se usa la estimulación muscular directa. Un paciente con miopatía presenta un potencial de acción motora reducido o ausente por ambos sistemas (fig. 4).
El hallazgo histológico biópsico característico, que puede verse mediante técnica inmunohistoquímica o microscopia electrónica, es una pérdida extensa de filamentos gruesos que corresponde a la pérdida de miosina y que revela atrofia de fibras musculares con cambios vacuolares, grados variables de necrosis y regeneración, ausencia de inflamación linfocítica, reducción parcheada o completa de la reactividad de la miosín-ATPasa en las fibras no necróticas y ausencia de mRNA de miosina49. La pérdida de miosina y la necrosis de fibras contribuyen sustancialmente al mantenimiento de la debilidad.
La cuantificación del cociente miosina/actina mediante electroforesis50 muestra que el valor medio en pacientes control es de 1,37 ± 0,21 y en pacientes con miopatía de 0,37 ± 0,17, lo que puede ayudar en el diagnóstico diferencial.
Tiene un buen pronóstico funcional per se, pero prolongado a lo largo de semanas o meses aunque, al igual que en la PPC, las formas graves pueden dejar secuelas irreversibles e invalidantes tras 2-3 años del proceso, con marcada disminución de la calida de vida51.
Referencias
1. Green DM. Weakness in the ICU: Guillain-Barre syndrome, myasthenia gravis and critical illness polyneuropathy/myopathy. Neurologist 2005; 11:338-47. [ Links ]
2. Witt NJ, Zochodne DW, Bolton CF, Grand F, Wells G, Young B: Peripheral nerve function in sepsis and multiple organ failure. Chest 1991; 99:176-184. [ Links ]
3. Leijten FS, De Weerd AW: Critical illness polyneuropathy. Areview of literature, definition and pathophysiology. Clin Neurol Neurosurg 1994; 96:10-19. [ Links ]
4. Bolton CF, Young B, Zochodne DW: The neurological complications of sepsis. Ann Neurol 1993; 33:94-100. [ Links ]
5. Zochodne DW, Ramsay DA, Saly V, Shelley S, Moffat S: Acute necrotizing myopathy of intensive care electrophysiological studies. Muscle Nerve 1994; 17:285-292. [ Links ]
6. Segredo V, Caldwell J, Matthay M, Sharma M, Grunke L, Miller : Persistent paralysis in critically ill patients after long term administration of vecuronium. N Engl J Med 1992; 327:524-528. [ Links ]
7. Gooch JL, Suchyta MR, Balbierz JM: Prolonged paralysis after treatment with neuromuscular junction blocking agents. Crit Care Med 1991; 19:1125-31. [ Links ]
8. Bercker S, Weber S, Deja M y cols.: Critical illness polyneuropathy and myopathy in patients with acute respiratory distress syndrome. Crit Care Med 2005; 33:711-15. [ Links ]
9. Bolton CF. Neuromuscular complications of sepsis. Intensive Care Med 1993; 19:S58-63. [ Links ]
10. Hirano M, Ott BR, Raps EC y cols.: Acute quadriplegic myopathy: a complication of treatment with steroids, non depolarizing blocking agents, or both? Neurology 1992; 42:2082- 2087. [ Links ]
11. Gamrin L, Andersson K, Hultman E, Nilsson E, Essen P, Wemerman J: Longitudinal changes of biochemical parameters in muscle during critical illness. Metabolism 1997; 46:756-762. [ Links ]
12. Kuwabara S: Guillain-Barré syndrome: epidemiology, pathophisiologyand management. Drugs 2004 ; 64 :597-610. [ Links ]
13. Hughes RA: The spectrum of aquired demyelinating polyradiculoneuropathy.Acta Neurol Belg 1994; 94:128-132. [ Links ]
14. Sharshar T, Chevret S, Bourdain F, Raphael JC: Early predictors of mechanical ventilation in Guillen-Barré syndrome. Crit Care Med 2003; 31:278-283. [ Links ]
15. Chevrolet JC, Deléamont P: Repeated vital capacity measurements as predictive parameters for mechanical ventilation need and weaning success in the Guillain-Barré syndrome. Am Rev Respir Dis 1991; 144:814-818. [ Links ]
16. Hughes RA, Cornblath DR: Guillain-Barré syndrome. Lancet 2005; 366:1653-1666. [ Links ]
17. Albers JW, Kelly JJ: Acquired inflammatory demyelinating polyneuropathies: clinical and electrodiagnostic features. Muscle Nerve 1989; 12:435-451. [ Links ]
18. Van der Meche FG, Van Doorn PA, Meulstee J, Jennekens FG: Diagnostic and classification criteria for the Guillain-Barré syndrome. Eur Neurol 2001; 45:133-139. [ Links ]
19. Phillips LH: The epidemiology of myasthenia gravis. Semin Neurol 2004; 24:17-20. [ Links ]
20. Thomas CE, Mayer SA, Gungor Y y cols.: Myastenic crisis. Clinical features, mortality, complications and risk factors for prolonged intubation. Neurology 1997; 48:1253-60. [ Links ]
21. Rieder P, Louis M, Jolliet P, Chevrolet JC: The repeated measurement of vital capacity is a poor predictor of the need for mechanical ventilation in myasthenia gravis. Intensive Care Med 1995; 21:663-68. [ Links ]
22. Lacomis D: Myasthenic crisis. Neurocrit Care 2005; 3:189-94. [ Links ]
23. Bolton CF, Gilber JJ, Hahn AF, Sibbald WJ: Polyneuropathy in critically ill patients. J Neurol Neurosurg Psychiatry 1984; 47:1223-1231. [ Links ]
24. Zochodne DW, Bolton CF, Wells GA y cols.: Critical illness polyneuropathy. A complication of sepsis and multiple organ failure. Brain 1987; 110:819-841. [ Links ]
25. Hund E: Neurological complications of sepsis: critical illness polyneuropathy and myopathy. J Neurol 2001; 248:929-34. [ Links ]
26. Latronico N, Fenzi F, Recupero D y cols.: Critical illness myopathy and neuropathy. Lancet 1996; 347:1579-1582. [ Links ]
27. Zifko UA, Zifko HT, Bolton CF: Clinical and electrophysiological findings in critical illness polyneuropathy. J Neurol Sci 1998; 159:186-93. [ Links ]
28. Maher J, Rutleedge F, Remtulla H, Parkes A, Bernardi L, Bolton CF: Neuromuscular disorders associated with failure to wean from the ventilator. Intensive Care Med 1995; 21:737-43. [ Links ]
29. Witt NJ, Zochodne DW, Bolton CF y cols.: Peripheral nerve function in sepsis and multiple organ failure. Chest 1991; 99:176-184. [ Links ]
30. Garnacho J, Madrazo J, García JL y cols.: Critical illness polyneuropathy: risk factors and clinical consequences. A cohort study in septic patients. Intensive Care Med 2001; 27:1288-96. [ Links ]
31. De Jonghe B, Sharshar T, Lefaucheur JP y cols.: Paresis acquired in the intensive care unit. A prospective multicenter study. JAMA 2002; 288:2859-67. [ Links ]
32. Leijten FSS, Harink JE, Poortvliet DCJ, De Weerd AW: The role of polyneuropathy in motor convalescence after prolonged mechanical ventilation. JAMA 1995; 274:1221-25. [ Links ]
33. Hund EF, Fogel W, Krieger D, DeGeorgia M, Hacke W: Critical illness polineuropathy: clinical findings and outcomes of a frequent cause of neuromuscular weaning failure. Crit Care Med 1996; 24:1328-33. [ Links ]
34. Albers JW: Clinical neurophysiology of generalized polineuropathy. J Clin Neurophysiol 1993; 10:149-166. [ Links ]
35. Bolton CF, Laverty DA, Brown JD, Witt NJ, Hahn AF, Sibbald WJ: Critically ill polineuropathy. Electrophysiological studies and differentiation from Guillain-Barré syndrome. J Neurol Neurosurg Psychiatry 1986; 49:563-73. [ Links ]
36. Gurtubay IG, Morales G, Navajas D, Carrera B, Iragui M: Alteraciones neuromusculares del paciente crítico. Rev Neurol 1998; 26:53-57. [ Links ]
37. Leijten FS, De Weerd AW: Critical illness polineuropathy:a review of the literature, definition and pathophysiology. Clin Neurol Neurosurg 1994; 96:10-19. [ Links ]
38. Zifko UA: Long-term outcome of critical illness polyneuropathy.Muscle Nerve 2000; 9:S49-52. [ Links ]
39. De Seze M, Petit H, Wiart L y cols.: Critical illness polyneuropathy.A 2-year folow-up study in 19 severe cases. Eur Neurol 2000; 43:61-9. [ Links ]
40. MacFarlane IA, Rosenthal FD: Severe myopathy after status asthmaticus. Lancet 1977; 2:615. [ Links ]
41. Bolton CF: Neuromuscular manifestations of critical illness.Muscle Nerve 2005; 32:140-63. [ Links ]
42. Hund E: Myopathy in critically ill patients. Crit Care Med 1999; 27:2544-47. [ Links ]
43. Hanson P, Dive A, Brucher JM, Bisteau M, Dangoisse M,Deltombe T: Acute corticosteroid myopathy in intensive care patients. Muscle Nerve 1997; 20:1371-80. [ Links ]
44. Campellone JV, Lacomis D, Kramer DJ, Van Cott AC, Giuliani MJ: Acute myopathy after liver transplantation. Neurology 1998; 50:46-53. [ Links ]
45. Latronico N, Peli E, Botteri M: Critical illness myopathy and neuropathy. Curr Opin Crit Care 2005; 11:126-132. [ Links ]
46. Lacomis D, Zochodne DW, Bird SJ: Critical illness myopathy.Muscle Nerve 2000; 23:1785-88. [ Links ]
47. Zochodne DW, Ramsay DA, Saly V, Shelley S, Moffatt S:Acute necrotizing myopathy of intensive care: electrophysiological studies. Muscle Nerve 1994; 17:285-92. [ Links ]
48. Gutmann L: Critical illness neuropathy and myopathy. Arch Neurol 1999; 56:527-28. [ Links ]
49. Lacomis D, Giuliani MJ, Van Cott AC, Kramer DJ: Acute myopathy of intensive care. clinical EMG and pathologic aspects.Ann Neurol 1996; 40:645-54. [ Links ]
50. Stibler H, Edstrom L, Ahlbeck K: Electrophoretic determination of the myosin/actin ratio in the diagnosis of critical illness myopathy. Intensive Care Med 2003; 29:1515-27. [ Links ]
51. Gooch JL: Prolonged paralysis after neuromuscular blockade. Muscle Nerve 1995; 18:937-42. [ Links ]
]]>
![]() Dirección para correspondencia:
Dirección para correspondencia:
Alfonso Mesejo
Servicio de Medicina Intensiva
Hospital Clínico Universitario
Avda. Blasco Ibáñez, 17
46010-Valencia
E-mail: mesejo_alf@gva.es