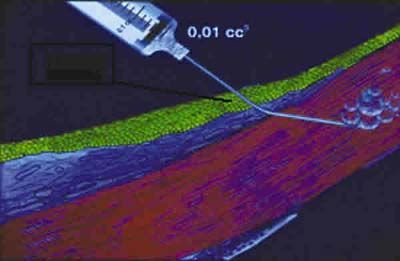
Fig. 1a. Figura en el que se observa la aguja de insulina con angulación de
30 que se requiere para inyectar el corticoide en el limbo penetrando el
epitelio y por debajo de la capa de Bowman dentro del estroma.
APLICACIÓN DE CORTICOSTEROIDES
INTRACORNEANOS DE DEPÓSITO EN EL TRATAMIENTO
DE RECHAZO DE QUERATOPLASTIA
INTRACORNEAL DEPOT STEROIDS FOR THE TREATMENT OF
CORNEAL REJECTION AFTER KERATOPLASTY
ARENAS E1, NAVARRO M2, MIETH MA3
| RESUMEN Objetivo: Presentación de una nueva forma de terapia ocular al tratamiento de rechazo de queratoplastia mediante microinyecciones intracorneanas. Palabras clave: Inyección intraestromal, queratoplastia penetrante queratoplastia lamelar, queratoplastia homoplástica, rechazo corneano, cortisona de depósito. | SUMMARY Purpose: To introduce a new type of therapy for corneal rejection after keratoplasty with the microinjection of intrastromal depot cortisone in single or multiple doses. Key words: Intrastromal injection, penetrating keratoplasty, lamellar keratoplasty, homoplastic keratoplasty, graft rejection, depot cortisone. |
Correspondencia:
Eduardo Arenas
Transv 21 No 100-20, Bogotá ]]>
Colombia
E-mail: earenas@cable.net.co
INTRODUCCIÓN
La administración tópica de corticoides ha sido usada durante mucho tiempo en el tratamiento de enfermedades inflamatorias del globo ocular (1). Una de las indicaciones más específicas es en el manejo del síndrome de rechazo en los transplantes corneanos, los cuales pueden presentarse en forma temprana o tardía en un 10 a 65% de los transplantes, según varios autores y dependiendo del tipo de huésped (2-4). Dado que la penetración de una gota dentro del estroma puede ser de solo un 1,5 a 3% cuando se aplica en forma de colirio (5), para que el corticoide actúe en estos casos, es indispensable aplicar dosis intensas y frecuentes aumentando el riesgo de producir catarata o glaucoma secundario, entre otras (6).
El tratamiento de los injertos rechazados consiste actualmente en altas dosis de cortisona local, subconjuntival o sistémica (7). Algunos autores prefieren el uso de la ciclosporina menos específica y con menos efectos locales secundarios pero más riesgos cuando se usa sistémicamente (8).
El epitelio corneano proporciona una barrera inicial a la penetración de fármacos y electrolitos hidrosolubles por su naturaleza lipofílica y sus estrechas uniones a base de desmosomas intercelulares, lo que limita la absorción de sustancias ionizadas hidrófilas. El estroma corneano con su naturaleza hidrófila actúa como barrera para fármacos en solventes lipídicos, que son los que mejor penetran el epitelio (9). En esta forma vemos que existe cierta dificultad para que un medicamento actúe en forma completa en el estroma profundo, ya que si es hidrofílico no penetra el epitelio y si es liposoluble no se difunde en el estroma. Si le agregamos a lo anterior la falta de vascularización de la córnea que impide que substancias usadas por vía parenteral o subconjuntival circulen libremente dentro del estroma. La otra vía de penetración sería por la circulación perilimbar vía cámara anterior a través de inyecciones subconjuntivales, aunque por esta ruta el medicamento puede pasar a cámara anterior, su efecto decrece rápidamente por absorción perdiendo asi su efecto terapéutico (10). De nuestra experiencia con la inyección de aire en el estroma corneano para facilitar la disección en las queratoplastias lamelares, aprendimos que substancias inyectadas intraestromalmente se difunden fácilmente, y tienden a desaparecer (11).
En este estudio presentamos nuestra experiencia con la aplicación de corticoides inyectados directamente en el estroma de la córnea a dosis mínimas, pero con cristales de depósito en el tratamiento del rechazo al trasplante corneano. Este tipo de terapia no ha sido descrito antes en la literatura.
MATERIAL Y MÉTODOS
El presente estudio retrospectivo-descriptivo, analiza información de 33 pacientes, observados entre el 23 de abril de 1998 y el 23 de setiembre del 2000. Se incluyeron ojos sometidos a queratoplastia penetrante, lamelar u homoplástica que presentaron cuadro clínico de rechazo al injerto.
Fueron excluidos los pacientes con diagnóstico de otras enfermedades concomitantes con patología inflamatoria de la córnea como por ejemplo ojos con enfermedad herpética. Las historias clínicas fueron obtenidas del Archivo de uno de los investigadores (EA). Se codificaron los datos con relación a edad, sexo, ojo implicado, tipo de cirugía, duración de síntomas de rechazo, tipo y duración del tratamiento preinyección, tipo de inyección intracorneana y número de dosis, tratamiento postinyección, mejoría sintomática y clínica. Se definió como queratoplastia homoplástica aquellos ojos en los cuales a causa de un daño no muy profundo de la córnea a consecuencia de Cirugías refractivas complicadas se reemplazo mediante un microquerátomo únicamente la parte superficial de acuerdo a técnicas descritas (12).
]]> El rechazo fue clasificado en epitelial, endotelial, estromal y mixto de acuerdo a la capa predominantemente afectada y en leve, moderado, grave y severo según su cuadro clínico en precoz y tardío según el tiempo de aparición, según lo establecido por Polack (13).Se inyectó el medicamento en la fase aguda del rechazo, directamente en el estroma corneal inmediatamente por debajo de la Capa de Bowman, con una aguja número 30 a la cual se le realizó un doblez de 30 grados en la cara del bisel mirando hacia el cirujano (fig. 1). Es indispensable utilizar una jeringa de tuberculina que tiene la aguja más delgada y además viene soldada a la jeringa. En el momento de inyectar debe ejercerse una fuerte presión que con otros tipos de jeringa se corre el riesgo de que ésta se suelte en la maniobra. La aguja con el bisel mirando hacia delante se introduce en la córnea periférica comenzando en las arcadas vasculares perilimbares y una vez desaparece el bisel dentro del estroma se inyecta hasta que aparece una zona blanquecina de aproximadamente 0,2 mm de diámetro. Esto según medidas que hicimos con una videocámara corresponde a una dosis de 0,1 mm del material inyectado. Se escogió el área más inflamada aplicando la droga en el lecho receptor. Inmediatamente después de aplicada la dosis se observa un pequeño depósito que desaparece totalmente aproximadamente 10 días después (fig. 2). La dosis inyectada fue de 10 microlitros (0,07 miligramos) de una preparación comercial de 1 mililitro la cual contiene 5 miligramos de Dipropionato de Betametasona y 2 miligramos de Fosfato Disódico de Betametasona para uso Intramuscular, Intralesional o Intraarticular. Hasta donde fue posible se trató de no utilizar ningún otro tipo de medicamento local o sistémico adicional para controlar el rechazo.

Fig. 1a. Figura en el que se observa la aguja de insulina con angulación de
30 que se requiere para inyectar el corticoide en el limbo penetrando el
epitelio y por debajo de la capa de Bowman dentro del estroma.

Fig. 1b. Jeringa de Tuberculina a 30º. Aguja calibre 30. Incurvar la aguja.
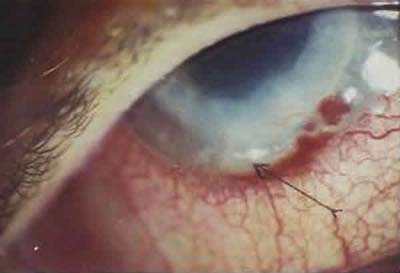
Fig. 2. Rechazo epitelio estromal al que se le aplicó en la parte inferior la ]]>
primera dosis de cortisona de depósito. Obsérvese la mancha blanca
correspondiente (flecha).
RESULTADOS
La edad promedio de los pacientes fue 48,09 (rango, 11 años a 83 años), siendo la edad promedio para el sexo masculino de 50,38, y para el sexo femenino de 44,08. Se estudiaron más rechazos del masculino con 21 casos (63,63%, tabla I). El ojo más afectado fue el ojo derecho con 19 casos (57,57%), el ojo izquierdo tuvo 14 casos (42,42%).
El tipo de cirugía practicada se distribuyó en la siguiente forma: Queratoplastia penetrante en 26 casos (78,78%), lamelar en 5 casos (15,15%) y homoplástica en 2 casos (6,06%) (tabla II). En cuanto al tipo de rechazo en 20 pacientes (60,60%) rechazo predominantemente epitelial, 2 pacientes (6,06%) presentaron rechazo de predominio endotelial y 11 pacientes (33,3%) presentaron rechazo mixto (tabla III).
Con respecto a la severidad 4 casos (12,12%) fueron leves, 20 casos (60,60%) moderados, 2 casos (6,06%) graves y 7 casos (21,21%) severos. El 39,39% de los rechazos (13 casos) fue clasificado como precoz y el 60,60% (20 casos) tardío. La duración de síntomas fue de una semana o menos en 19 casos (57,57%) y de más de una semana en el resto (42,42%).
]]> En 18 de los 33 casos (54,54%) no usamos ningún tratamiento tópico asociado, mientras que en los otros 15 (45,45%) agregamos a la terapia alguna de las preparaciones comerciales de corticoides disponible durante la primera semana, a causa de ansiedad del paciente.Se midió la eficacia del tratamiento con parámetros clínicos y subjetivos. De los 33 casos 5 mejoraron una línea de visión en el control efectuado 10 días después de aplicada la primera inyección; 10 mejoraron dos líneas; dos casos mejoraron tres líneas de visión en la escala de Snellen; un caso cuatro líneas; tres cinco líneas; siete la visión quedó igual; tres empeoraron y en cuatro no se determinó la agudeza visual.
Con relación a los síntomas subjetivos: 27 pacientes (81,81%) presentaron mejoría subjetiva del dolor, molestias y agudeza visual. Todos los ojos mostraron algún tipo de mejoría clínica, evaluada por disminución en la intensidad de los signos de rechazo en el examen con Lámpara de Hendidura, hiperemia conjuntival e inyección ciliar, edema corneal, precipitados queráticos y subepiteliales, línea endotelial de rechazo y reacción en la cámara anterior. En más de la mitad de los casos la mejoría fue total o casi total (tabla IV).
Cuando el rechazo fue considerado activo se repitió la dosis cada 10 días aproximadamente hasta la desaparición total del proceso. En tres casos detectados precozmente bastó una sola dosis para controlar el rechazo; en cinco dos dosis fueron suficientes 9 casos recibieron hasta 5 inyecciones antes de estar seguros de que no había signos y síntomas. ( 54% de los casos). El resto de los casos recibieron más de cinco sesiones muchos de ellos por presentar recurrencia de las recidivas meses más tarde.
Un total de 31 casos (93,93%) han sido seguidos por un tiempo mayor de 6 meses, sin presentar catarata ni glaucoma secundario hasta el momento.
DISCUSIÓN
El tratamiento del rechazo de injerto es ampliamente conocido por los cirujanos corneanos y consiste principalmente en altas dosis de cortisona local, subconjuntival o sistémica. La cortisona generalmente controla el rechazo cuando es iniciada tempranamente después de los primeros signos y síntomas, pero frecuentemente da origen a efectos indeseables como catarata o elevación seria de la presión intraocular. Algunos autores prefieren el uso de ciclosporina con menos efectos secundarios, pero cuando es usada sistémicamente puede desarrollar complicaciones.
Comprobamos en nuestro estudio la eficacia de la aplicación intraestromal y la ausencia de efectos secundarios oculares. En todos los casos se observó una mejoría clínica, mucho más evidente a la que solíamos observar cuando usábamos el tratamiento tradicional local o sistémico. En ninguno de los casos hubo que recurrir a dosis sistémicas. La inyección intracorneana no presentó ningún efecto negativo en el tejido, ni en otras estructuras del globo comprobado a corto y largo plazo, contrario a lo que anteriormente observamos en otra serie de casos (14). En ningún caso se presentó aumento de la presión intraocular atribuible al medicamento inyectado. Los cristales de depósito se intercalan entre las fibras estromales y desde allí liberan lentamente su acción farmacológica.
Con esta nueva vía de administración de medicamentos estamos creando una pauta en el tratamiento de diferentes enfermedades oculares que creemos va a ser ampliamente aceptada por su facilidad de administración, bajo costo, pequeñas dosis, eficacia terapéutica y ausencia de efectos secundarios. La rapidez de respuesta a una sola inyección en casos de rechazo epitelial que en ocasiones pueden ser repetitivos, nos evita el riesgo de usar en forma crónica cortisona que en muchas ocasiones conlleva al desarrollo de cataratas subcapsulares posteriores. En la actualidad estamos trabajando con el mismo procedimiento en casos de queratitis de diversas causas, incluyendo la de etiología viral en la cual inyectamos acyclovir; uveítis anteriores que tratamos con corticoides; patologías infecciosas con antibióticos y procesos inmunológicos y vascularización corneal de diferentes causas que tratamos con 5-Fluorouracilo, obteniendo resultados igualmente satisfactorios.
]]>BIBLIOGRAFÍA
1. Arentsen J. Treatment of corneal transplant allograft reactions in The Cornea. Transaction of the World Congress on the Cornea III. edited by Cavanagh HD. New York: Raven Press. 1967; 403-404. [ Links ]
2. Epstein RJ, Seedor JA, Dreizen NG, Stulting RD, Waring GO 3rd; Wilson LA et al. Penetrating keratoplasty for herpes simplex keratitis and keratoconus. Allograft rejection and survival. Ophthalmology 1987; 94: 935-944. [ Links ]
3. Sharif KW, Casey TA. Penetrating keratoplasty for keratoconus: complications and long-term success. Br J Ophthalmol 1991; 75: 142-146. [ Links ]
4. Girard LJ, Esnaola N, Rao R, Barnett L, el Maghraby A, Canizales R. Allograft rejection after penetrating keratoplasty for keratoconus. Ophthalmic Surg 1993; 24: 40-43. [ Links ]
5. Janes RG, Stiles FJ. The penetretation of cortisol into normal and pathological rabbit eyes. Am J Ophthalmol 1963; 56: 84-88. [ Links ]
6. Martin TP, Reed JW, Legault C, Oberfeld SM, Jacoby BG, Yu DD et al. Cataract formation and cataract extraction after penetrating keratoplasty. Ophthalmology 1994; 101: 113-119. [ Links ]
7. Hill JC, Ivey A. Corticosteroids in corneal graft rejection: double versus single pulse therapy. Cornea 1994; 13: 383-388. [ Links ]
8. Newton C, Gebhardt BM, Kaufman HE. Topically applied cyclosporine in azone prolongs corneal allograft survival. Invest Ophthalmol Vis Sci 1988; 29: 208-215. [ Links ]
9. Havener WH. Ocular Pharmacology. Saint Louis: The CV Mosby Co. 1974; 18-20. [ Links ]
10. Hyndiuk RA. Radioactive depot-corticosteroid penetration into monkey ocular tissue. II. subconjunctival administration. Arch Ophthalmol 1969; 82: 259-263. [ Links ]
11. Archila EA. Deep lamellar keratoplasty dissection of host tissue with intrastromal air injection. Cornea 1984; 3: 217-218. [ Links ]
12. Burillon C, Durand L, Gourraud A. Combined epikeratoplasty and homoplastic keratophakia for correction of aphakia: double curve effect. Refract Corneal Surg 1993; 9: 214-218. [ Links ]
13. Polack FM. Corneal Transplantation. New York: Grune Stratton. 1977; 201-234. [ Links ]
14. Muñoz-Negrete FJ, Arenas-Archila E. Producción de Catarata Subcapsular Posterior tras Corticoterapia Tópica. Relación Dosis Efecto. Arch Soc Esp Oftalmol 1989; 57: 481-488. [ Links ] ]]>