
TRATAMIENTO DE DEFECTOS EPITELIALES
PERSISTENTES MEDIANTE SUERO AUTÓLOGO
TREATMENT OF PERSISTENT EPITHELIAL DEFECTS USING
AUTOLOGOUS SERUM APPLICATION
ALVARADO VALERO MC1, MARTÍNEZ TOLDOS JJ1, BORRAS BLASCO J3,
ALMIÑANA ALMIÑANA A2, PÉREZ RAMOS JM2
| RESUMEN ]]> Objetivo: Estudiar la influencia del tratamiento tópico con suero autólogo en la evolución clínica de los defectos epiteliales persistentes (DEP). Observar el efecto de este tratamiento en las variaciones histológicas de la metaplasia escamosa en 7 casos de ojo seco.Pacientes y métodos: Estudiamos un total de 17 ojos (14 pacientes). Analizamos la evolución clínica (test fluoresceína, Schirmer I y II y control fotográfico) de los DEP en estos pacientes a los que se les aplicó suero autólogo al 20% durante 28 días. Cuantificamos histológicamente con citología de impresión y mediante el método de Tseng, la regresión de la metaplasia escamosa en 7 ojos de cuatro pacientes diagnosticados de penfigoide ocular cicatricial con ojo seco severo, tratados con autosuero. Se trata de un estudio clínico prospectivo no comparativo de series de casos. En el tratamiento estadístico de los datos utilizamos el test de Wilconxon. Resultados: En el 35,2% de casos (6 ojos) los DEP cicatrizaron a las 2 semanas (grupo efectivo), en el 47% (8 ojos) entre las 2 y 4 semanas (grupo parcialmente efectivo) y en el 17,6% (3 ojos) de casos la curación fue posterior a la 4.ª semana. La duración de los DEP previo al tratamiento fue de 36 días. En 6 de los 7 ojos en los que se estudió la metaplasia escamosa, se observó una regresión de la misma a los 28 días de tratamiento. Conclusiones: El tratamiento con suero autólogo acelera la cicatrización de los DEP. En la mayoría de casos, el tratamiento con suero autólogo provoca una involución de la metaplasia escamosa. Palabras clave: Suero autólogo, defecto epitelial persistente, ojo seco, metaplasia escamosa, citología de impresión. | SUMMARY Purpose: To study the impact of topical treatment with autologous serum on the clinical evolution of persistent corneal epithelial defects (PED) and to observe its effect on squamous metaplasia in 7 cases of dry eye. The Wilconxon test was used for the statistical treatment of the data. Results: The epithelial defect healed within 2 weeks in 6 eyes (35.2%). Eight eyes (47%) healed within 2-4 weeks and 3 eyes (17.6%) did not heal after week 4. The duration of PED, before serum therapy was 36 days. Six of seven eyes treated with autologous serum presented an involution of squamous metaplasia 28 days after initiation of the serum drops. Conclusions: Autologous serum treatment accelerates PED healing. Autologous serum application causes an involution of squamous metaplasia (Arch Soc Esp Oftalmol 2004; 79: 537-542). Key words: Autologous serum, persistent epithelial defect, dry eye, squamous metaplasia, impression cytology. |
Recibido: 6/2/04. Aceptado: 12/11/04.
Hospital General Universitario de Elche. Alicante. España. ]]>
1 Doctor en Medicina.
2 Licenciado en Medicina.
3 Doctor en Farmacia.
Comunicación presentada en el LXXIX Congreso de la S.E.O. (Valencia 2003).
Correspondencia:
M.C. Alvarado Valero
C/. Catedrático Eliseo G. Serrano, 16. Residencial Budapest I. Bw 16
03011 Alicante
España
El suero autólogo (SA), ha sido utilizado por diferentes autores con éxito como sustituto de la lágrima en el tratamiento de defectos epiteliales persistentes (DEP), en el contexto de ojo seco severo (1).
En pacientes con ojo seco grave, tipo penfigoide ocular cicatricial (POC), las secreciones basal y refleja están seriamente disminuidas. Este hecho supone una deprivación importante de determinados componentes de la lágrima (tales como el factor de crecimiento epidérmico, vitamina A y factor transformador del crecimiento de fibroblastos ß) los cuales, están implicados directamente en el mantenimiento y la regulación de la proliferación, diferenciación y maduración de las células epiteliales de la superficie corneo-conjuntival (2). La deficiencia de estos componentes implica un compromiso en la integridad de la superficie ocular, resultando en la disrupción del epitelio y la formación de defectos epiteliales persistentes (DEP) y úlceras tróficas. Según esto, parece ser que el tratamiento tópico con suero autólogo podría acelerar la cicatrización de estos defectos epiteliales (1-3).
Por otra parte, en el ojo seco severo secundario a estas enfermedades mucosinequiantes, existe una deficiencia importante de mucina por la pérdida de células caliciformes (células globets) de la conjuntiva, secundario a un proceso de metaplasia escamosa. El déficit de capa mucinosa de la lágrima, hace que los sustitutos lagrimales utilizados como tratamiento sintomático en estos ojos no humecten adecuadamente la superficie ocular. En este sentido, algunos autores (1,2) han demostrado in vitro, que el SA tiene un efecto directo en el aumento de la expresión del receptor MUC-1 para la mucina en un cultivo de células conjuntivales. Se cree que la vitamina A presente en el suero es la responsable de esta diferenciación celular.
Este trabajo estudia el efecto del suero autólogo en la evolución de los DEP secundarios a ojo seco severo, así como la influencia que tiene este tratamiento en la evolución de la metaplasia escamosa en siete casos de penfigoide ocular cicatricial.
SUJETOS, MATERIAL Y MÉTODOS
Se han incluido en este estudio, realizado de forma prospectiva, un total de 17 ojos (14 pacientes entre 60 y 85 años). De estos 10 eran mujeres y 4 hombres. Todos los sujetos presentaban DEP. Definido éste como el defecto epitelial corneal cuya duración excede las dos semanas con tratamiento convencional sin observarse curación o tendencia a la misma. Los DEP eran de diferente naturaleza: cuatro pacientes presentaban queratopatía neurotrófica herpética unilateral. Estos fueron tratados previamente con pomada de aciclovir 5 veces/día, cicloplejía, corticoides tópicos, lágrimas artificiales sin conservantes y corticoides vía oral. Durante un tiempo aproximado de mes y medio. Dos pacientes presentaron úlcera de Mooren unilateral, uno de ellos se trató con bolus de ciclofosfamida iv, y ambos con ciclosporina tópica 0,5%, corticoides tópicos y lágrimas artificiales sin conservantes durante 4 y 8 semanas. Tres pacientes presentaron un defecto epitelial secundario a queratopatía por exposición por parálisis facial periférica, en dos de ellos se realizó tarsorrafia quirúrgica, en todos se aplicó un tratamiento con lubricación sin conservantes durante 4 a 6 semanas. Hubo un caso de defecto epitelial por artritis reumatoide que fue tratado con ciclosporina tópica 0,5%, corticoides tópicos y lubricación durante 8 semanas. Además se realizó tratamiento sistémico con corticoides y metrotexate. Por otra parte, cuatro pacientes (7 ojos) presentaron POC y DEP secundario, cinco de ellos diagnosticados mediante biopsia conjuntival, en los otros dos la biopsia no fue resolutiva. En tres de ellos el tratamiento fue dapsona 25 mg/12 h durante 2 semanas y 100 mg/d después de este tiempo y de manera indefinida. En el paciente restante, debido a la rápida progresión de su enfermedad se pautó ciclofosfamida intravenosa 1,5 mg/k/d y prednisona 1mg/k/d iv. como tratamiento de choque, después se rebajaron los corticoides paulatinamente manteniendo el tratamiento inmunosupresor durante 8 semanas. En todos los pacientes se instauró tratamiento lubricante, corticoides tópicos y pomada antibiótica durante 4 a 8 semanas.
La metodología de seguimiento de estos pacientes fue la siguiente:
Se elaboró una ficha para cada ojo, donde constaban los datos de filiación, la patología ocular de base, el tratamiento previo, el examen biomicroscópico previo al tratamiento: con test de fluoresceína (1 gota de fluoresceína sódica al 1%), Schirmer I y II. La medición del área del defecto epitelial antes, a los 7, 14 y 28 días del tratamiento con constatación fotográfica. Duración del DEP previo al tratamiento (semanas), tratamiento concomitante adyuvante y tiempo necesario para que cicatrice el DEP con el tratamiento (semanas). Se catalogó de tratamiento efectivo cuando la curación se presentaba a las 2 semanas o antes, de parcialmente efectivo cuando eran necesarias más de dos y menos de cuatro semanas para la curación, y de inefectivo cuando la cicatrización ocurría pasadas las 4 semanas.
En los cuatro pacientes con POC se cuantificó el grado de metaplasia escamosa mediante citología de impresión según el método desarrollado por Tseng (4), antes, a los 7, 14 y 28 días del tratamiento. La citología de impresión se realizó bajo anestesia tópica: hidrocloruro de tetracaína y oxibuprocaína (Colircusí Anestésico Doble, Alcon Cusí SA El Masnou Barcelona). A continuación, con una pinza se tomó una tirita de papel de filtro de acetato de celulosa (Millipore HAWP340 Dade-Behring Barcelona) y se colocó sobre la conjuntiva bulbar superior, inferior y córnea. Se comprimió suavemente durante unos segundos y se retiró el papel de filtro, que se envió para su procesamiento al Servicio de Anatomía Patológica de nuestro Hospital. La metaplasia escamosa se clasificó en 5 estadios, según la presencia o no de células caliciformes, cambios morfológicos del núcleo de las células epiteliales no secretoras, relación núcleo/citoplasma, cambios metacromáticos del citoplasma y queratinización (4,5).
]]> La elaboración del colirio de autosuero se realizó por el Servicio de Farmacia de nuestro Hospital según el RD 175/01 del 23 febrero (6), acerca de la elaboración de fórmulas magistrales. En un primer paso se extrajeron 30 cc de sangre mediante venopunción (6 tubos de extracción de vacío con gelosa sin anticoagulante). Posteriormente, se centrifugó ésta a 5.000 rpm durante 10 minutos dejándose sedimentar para separar el suero de los elementos formes y después se diluyó con suero fisiológico al 20% en condiciones estériles, bajo campana de flujo laminar. El suero diluido fue cuidadosamente embotellado en frascos estériles protegidos de la luz (lo que evita la degradación temprana de la vitamina A) y conservados a +4º C (1 mes) y a 20º C (3 meses).Se redactó una hoja informativa para los pacientes en la que se les instruía sobre el modo de aplicación del colirio y las condiciones de conservación. Además se redactó una hoja de consentimiento informado para el tratamiento de defectos epiteliales persistentes mediante suero autólogo según el artículo 10 de la Ley General de Sanidad.
En cuanto al tratamiento estadístico, se parte de un estudio clínico prospectivo no comparativo de serie de casos. Se cuantificó la duración de los DEP previa al tratamiento y valores del test de Schirmer I y II en este tiempo. Se midió el tiempo necesario para la curación de los DEP postratamiento, clasificando esta muestra en 3 grupos según el tiempo necesario para la curación (grupo efectivo, parcialmente efectivo e inefectivo). Se comparó mediante el test de los rangos con signo de Wilconxon la duración de los DEP previa al tratamiento, test de Schirmer I y II con la duración de los DEP postratamiento. Además se realizó un estudio estadístico descriptivo de la influencia del tratamiento en la modificación de la metaplasia escamosa en 7 casos de POC a los 7, 14 y 28 días del tratamiento.
RESULTADOS
En la tabla I se describe, para cada grupo (efectivo, parcialmente efectivo e inefectivo), la enfermedad original, la duración del DEP previo al tratamiento, el tratamiento previo aplicado y los test de Schirmer I y II.
En el 35,2% de los casos (6 ojos) de DEP tratados se observó cicatrización en 2 semanas (grupo efectivo). En el 47% (8 ojos), se obtuvo curación de los defectos a partir de la 2.ª y hasta la 4.ª semana (grupo parcialmente efectivo). En el 17,6% (3 ojos) de casos la curación se obtuvo después de la 4.ª semana.
En la mayoría de los ojos tratados con SA (14 de 17), se observa curación o tendencia a la curación, al cabo de las 2 a 4 semanas. El promedio de duración de los DEP previo al tratamiento fue de 36 días y la cicatrización total de los DEP postratamiento ocurrió a los 20 días.
Mediante la prueba de los rangos con signo de Wilconxon, se observó que existía una relación estadísticamente significativa entre la antigüedad de los DEP en los grupos efectivo y parcialmente efectivo, y el tiempo necesario para que éstos curaran después de la aplicación del autosuero (p<0,005). En el grupo inefectivo, no se obtuvieron diferencias significativas.
No se encontraron diferencias significativas entre la enfermedad original, Schimer I y II en los 3 grupos.
]]> En cuanto a la influencia de este tratamiento en la evolución de la metaplasia escamosa en los 7 casos de POC, se observó que, en el 85,7% de los casos (6 de 7 ojos), mejoraba el grado de metaplasia con respecto al previo al tratamiento. El caso que no mejoró presentaba un grado de metaplasia previo muy avanzado, con ausencia de células caliciformes y sustitución del epitelio conjuntival estratificado no queratinizado por un epitelio escamoso queratinizado (fig. 1). En el resto de casos, la metaplasia escamosa involucionó de grado 2 a grado 0 en dos casos, de grado 4 a grado 3 en otros dos casos (fig. 2), de grado 3 a grado 1 en un caso y de grado 3 a grado 0 en otro caso. Estos resultados son referentes a las 4 semanas de tratamiento.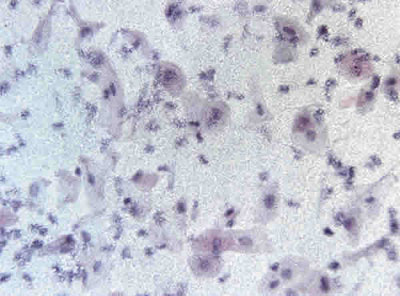
Fig. 1. Citología de impresión de un paciente con Penfigoide ocular cicatricial (POC)
grado IV y metaplasia escamosa grado 5. Las células epiteliales no secretoras son grandes,
queratinizadas y separadas, con núcleos picnóticos o ausentes.
Tinción PAS-hematoxilina. Magnificación x40.

Fig. 2. Citología de impresión de un paciente con POC grado II y metaplasia escamosa grado 3:
Las células epiteliales no secretoras son grandes y separadas.
Existen algunas células picnóticas. Tinción PAS-hematoxilina. Magnificación x40.
Se observó, según los resultados expuestos anteriormente, y teniendo constancia de que no utilizamos grupo control, que en la mayoría de ojos (14 de 17), se aprecia curación o tendencia a la curación entre las 2 a 4 semanas del tratamiento (media de 20 días). Sin embargo la antigüedad de los DEP fue de 36 días. Por otra parte, los DEP no recurrieron en ningún ojo después de haber suspendido el tratamiento.
Estos resultados hacen pensar que, efectivamente, el tratamiento con SA parece acelerar y favorecer el crecimiento y trofismo celular, y por tanto, facilitar la cicatrización de los DEP. Probablemente el factor de crecimiento epidérmico (EGF) y la vitamina A son los responsables de estas acciones (1). Aunque los mecanismos precisos de actuación del SA en la superficie ocular son desconocidos, se sabe que el EGF acelera el proceso de migración de células epiteliales conjuntivales in vitro (1,2). También se ha observado que este factor y la albúmina (otra proteína presente en el suero) tienen actividad antiapoptótica (1,7), lo cual podría facilitar también la epitelización de estas lesiones.
La concentración de EGF presente en la secreción lagrimal refleja es de 0,7 a 8,1 ng/ml y de 1,9 a 9,7 en la secreción basal (2). Estos valores son más altos que los existentes en el suero (aproximadamente 0,5 ng/ml). En contraste, la cantidad de vitamina A de la lágrima humana es de 0,4-10,6 ng/ml y la del suero de 55 mg/ml (cien veces superior a la concentración de la lágrima). Cuando la vitamina A disminuye, el epitelio tiende a la metaplasia escamosa (2).
Según esto, y con respecto a los resultados obtenidos en este trabajo acerca de la influencia del SA en la involución de la metaplasia escamosa en los 7 casos de POC, parece ser que este tratamiento influye positivamente en la diferenciación de las células conjuntivales caliciformes. Según algunos autores (1), las células conjuntivales epiteliales cultivadas con SA presentan una mayor expresividad del receptor para la mucina MUC-1 en su superficie.
Todos los pacientes excepto dos experimentaron un mayor confort y bienestar tras el tratamiento con autosuero.
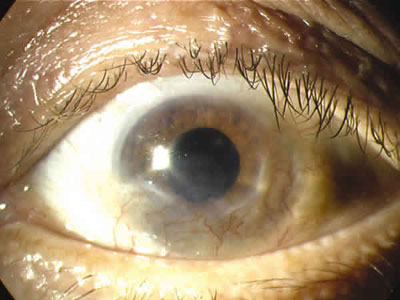
También el suero contiene antiproteasas semejantes a α2 macroglobulinas, con actividad anticolagenasa (2), lo cual pudiera tener beneficio en quemaduras por álcalis y en úlceras marginales autoinmunes tipo Mooren. A propósito de esto, se trató con éxito un caso muy avanzado de úlcera de Mooren con SA y ciclosporina tópica 0,5% (figs. 3 y 4), la úlcera epitelizó completamente, a pesar de que existía una insuficiencia limbar importante. Quizás el SA pudiera tener una actividad semejante a la de la membrana amniótica, en cuanto a capacidad de favorecer el microambiente celular limbar y facilitar así la epitelización y curación de estas lesiones.
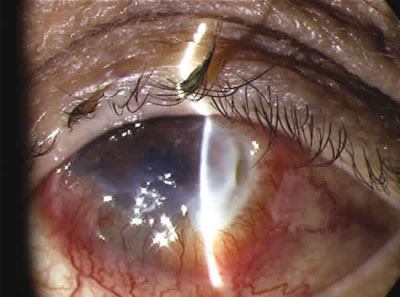
Fig. 3. Úlcera de Mooren avanzada. Obsérvese la invasión de la córnea inferior por conjuntiva.
Detalle del gran adelgazamiento y ablandamiento corneal periférico.
En cuanto a la conservación del suero autólogo, se sabe que sus componentes son estables durante 1 mes en el refrigerador (a +4º C) y 3 meses en el congelador (a -20º C) (1), a esto puede contribuir el hecho de que el SA contiene proteínas semejantes a la albúmina (2), que protege de la degradación de importantes citoquinas.
Los sustitutos lagrimales farmacológicos, proporcionan lubricación pero no nutrición (1). In vitro se confirma, según algunos autores (1), que las lágrimas artificiales tipo hidroxipropilmetilcelulosa (HPMC) al 0,3% son inapropiadas para mantener niveles intracelulares de ATP y por consiguiente la integridad de la membrana celular en células epiteliales humanas.
De cualquier forma, se debe tener una visión global e integrada en cuanto al tratamiento de este tipo de afecciones de la superficie ocular. Cuando la enfermedad primaria es conocida, el tratamiento inicial ha de enfocarse hacia el problema causante del DEP. Como pudiera ser lubricación artificial sin conservantes, tarsorrafia, lente de contacto terapéutica, transplante de limbo o de membrana amniótica, tratamiento de las malposiciones palpebrales, etc. (1,8). Si este tratamiento no es suficiente para conseguir una evolución favorable, entonces se puede recurrir al tratamiento con colirio de autosuero en conjunción con cualquiera de los tratamientos anteriores.
Con todo, podemos concluir que el tratamiento con SA es un método eficaz y coadyuvante al tratamiento estándar de los DEP. Supera a la terapia sustitutiva con lágrimas artificiales en casos de ojo seco grave, por ser una fuente de factores de crecimiento capaz de mantener la viabilidad celular del epitelio dañado.
Quizá en un futuro existan sustitutos de la lágrima fisiológica enriquecidos con citoquinas, los cuáles pudieran tener un papel preponderante en el tratamiento del ojo seco grave, defectos epiteliales persistentes de diferente origen, úlceras tróficas, etc. Y así se solventarían algunos inconvenientes de la obtención del SA, como pudieran ser las múltiples extracciones venosas.
]]> BIBLIOGRAFÍA
1. Tsubota K, Goto E, Shimmura S, Shimazaki J. Treatment of persistent corneal epithelial defect by autologous serum application. Ophthalmology 1999; 106: 1984-1989. [ Links ]
2. Tsubota K, Goto E, Fujita H, Ono M, Inove H, Saito I et al. Treatment of dry eye by autologous serum application in Sjogrens syndrome. Br J Ophthalmol 1999; 83: 390-395. [ Links ]
3. Poon AC, Geerling G, Dart JK, Fraendel GE, Daniels JT. Autologous serum eyedrops for dry eyes and epithelial defects: clinical and in vitro toxicity studies. Br J Ophthalmol 2001; 85: 1188-1197. [ Links ]
4. Murube del Castillo J, Rivas L. Ojo seco: clasificación clínica y por citología de impresión. Arch Soc Canar Oftal 2002; 13: 5-11. [ Links ]
5. Tseng SC. Staging of conjunctival squamous metaplasia by impression cytology. Ophthalmology 1985; 92: 728-733. [ Links ]
6. García Jiménez V, Veiga Villaverde B, Baamonde Arbaiza B, Cahue Carpintero I, Celemin Vinuela ML, Simo Martínez RM. Elaboración, utilización y evaluación de un colirio con suero autólogo en las lesiones corneales. Farm Hosp 2003; 27: 21-25. [ Links ]
7. Shimmura S, Ueno R, Matsumoto Y, Goto E, Higuchi A, Shimazaki J et al. Albumin as a tear supplement in the treatment of severe dry eye. Br J Ophthalmol 2003; 87: 1279-1283. [ Links ]
8. Díaz-Valle D, Benítez del Castillo Sánchez JM, Díaz Rodríguez E, Toledano Fernández M, Arteaga Sánchez A, Sayagués Gómez O. Manejo de la queratopatía neurotrófica mediante tarsorrafia con cianoacrilato y suero autólogo. Arch Soc Esp Oftalmol 2003; 78: 119-122. [ Links ] ]]>