Fig. 1. HSM pseudotumoral, de 21.800 micras de GLD,
en lesión no valorable por presentar la paciente ]]> alergia a fluoresceína. NVC mixta, secundaria
a DMAE y miopía magna. AV final, 0,005.
- 0,1 en 25% (2/8), con una pérdida media de 4 líneas de Snellen. Conclusiones: La HSM tras terapia fotodinámica es un suceso de etiología desconocida y poco frecuente. La incidencia de nuestra serie, 1,58%, está en el rango de lo publicado (0,24-9%). La mayor incidencia en DMAE y en las NVC ocultas sugiere que podrían tener un mayor riesgo de desarrollar una HSM. Se debe informar a los pacientes de la posibilidad de presentar esta complicación, que puede comprometer el resultado visual del tratamiento, y en ocasiones precisar cirugía. El bajo riesgo de HSM relacionada con el tratamiento, justifica su aplicación cuando éste está indicado.]]>
- 0.1. Patients lost 4 Snellen lines on average. Conclusions: SMH after PDT was an event of unknown etiology and low frequency. The incidence in our series (1.58%) was comparable with that described in the world literature (0.24-9.0%). The greatest incidence of AMD was in the occult group with no classic type of CNV, suggesting a possible higher risk for SMH in this type of lesion. It is mandatory to inform patients of the possibility of this complication, which can compromise the visual result of the PDT, and sometimes require surgery. The low risk of SMH related to the PDT justifies its application when it is indicated.]]>
Hemorragia submacular tras terapia fotodinámica en el tratamiento de la neovascularización coroidea
Submacular hemorrhage following photodynamic therapy in the treatment of choroidal neovascularization
Díaz-de-Durana-Santa-Coloma E.1, Fernández-Ares M.L.1, Iturralde-Errea D.1, Salazar-Díez J.L.1, Vázquez-Cruchaga E.1, López-Garrido J.A.1
Servicio de Oftalmología. Hospital de Galdakao. Vizcaya. España.
1 Licenciado en Medicina
Comunicación presentada en el LXXXI Congreso de la S.E.O. (Zaragoza 2005)
]]> Dirección para correspondencia
RESUMEN
Objetivo: Describir la incidencia, características clínicas y evolución de los pacientes que desarrollaron hemorragia submacular (HSM) tras terapia fotodinámica con verteporfino (TFD) en el tratamiento de la neovascularización coroidea (NVC).
Método: Estudio retrospectivo de los pacientes tratados mediante TFD en nuestro servicio desde julio de 2002 hasta junio de 2005.
Resultados: 8 de 504 ojos tratados con TFD (1,58%), desarrollaron HSM, de los cuales cuatro (0,79%) precisaron intervención quirúrgica. La incidencia por aplicación de TFD es de 0,65% (8/1221).
En siete de los ocho casos (87,5%) la patología de base fue la degeneración macular asociada a la edad (DMAE), y en un caso (12,5%) la miopía magna. Respecto a la composición de la lesión, cinco eran ocultas (62,5%; p=0,01), una predominantemente clásica, una mínimamente clásica, otra no valorable. La AV final media era de 0,057, siendo >– 0,1 en 25% (2/8), con una pérdida media de 4 líneas de Snellen.
Conclusiones: La HSM tras terapia fotodinámica es un suceso de etiología desconocida y poco frecuente. La incidencia de nuestra serie, 1,58%, está en el rango de lo publicado (0,24-9%). La mayor incidencia en DMAE y en las NVC ocultas sugiere que podrían tener un mayor riesgo de desarrollar una HSM. Se debe informar a los pacientes de la posibilidad de presentar esta complicación, que puede comprometer el resultado visual del tratamiento, y en ocasiones precisar cirugía. El bajo riesgo de HSM relacionada con el tratamiento, justifica su aplicación cuando éste está indicado.
Palabras clave: Hemorragia submacular, degeneración macular asociada a la edad, terapia fotodinámica, verteporfino, neovascularización coroidea.
Purpose: To describe the incidence, clinical features and evolution of submacular hemorrhage (SMH) occurring after photodynamic therapy (PDT) with verteporfin in the treatment of choroidal neovascularization (CNV).
Methods: A retrospective analysis of the patients treated with PDT in our hospital between July 2002 and May 2005 was undertaken.
Results: 8 out of 504 eyes treated with PDT (1.58%) developed SMH; 4 of them (0.79%) required surgical attack. The incidence of SMH for every application of PDT was 0.65% (8/1221).
The underlying disorder defined was age-related macular degeneration (AMD) in 7 cases (87.5%), and high myopia in one case (12.5%). Regarding the type of lesion, 5 were occult (62.5%; p=0.01), 1 predominantly classic, 1 minimally classic, and the last one was not classified. The average final visual acuity (VA) was 0.057, with 25% of patients having a VA >– 0.1. Patients lost 4 Snellen lines on average.
Conclusions: SMH after PDT was an event of unknown etiology and low frequency. The incidence in our series (1.58%) was comparable with that described in the world literature (0.24-9.0%). The greatest incidence of AMD was in the occult group with no classic type of CNV, suggesting a possible higher risk for SMH in this type of lesion. It is mandatory to inform patients of the possibility of this complication, which can compromise the visual result of the PDT, and sometimes require surgery. The low risk of SMH related to the PDT justifies its application when it is indicated. (Arch Soc Esp Oftalmol 2006; 81: 685-692).
Key words: Submacular hemorrhage, age-related macular degeneration, photodynamic therapy, verteporfin, choroidal neovascularization.
Introducción
La terapia fotodinámica con verteporfino (TFD) ha demostrado reducir de forma efectiva y segura el riesgo de pérdida visual moderada y grave en pacientes seleccionados con neovascularización coroidea (NVC) subfoveal secundaria a degeneración macular asociada a la edad (DMAE) y miopía patológica (estudios TAP y VIP) (1-4). Sin embargo, ambos estudios comunicaron casos ocasionales con pérdida de agudeza visual (AV) aguda y grave (al menos de 20 letras) dentro de los siete primeros días tras el tratamiento (TTO). Su conclusión es que este riesgo de pérdida visual grave es bajo, y atribuible a aumento del fluido sub-retiniano, retraso de la perfusión coroidea, hemorragia sub-retiniana o sub-epitelio pigmentario, o sin causa demostrable en angiofluoresceingrafía (AFG) (5). También se ha referido que algunos pacientes desarrollan hemorragia submacular (HSM), sin disminución de AV detectada por el paciente; ésta puede interferir con los re-TTOs, afectar al resultado visual, así como requerir cirugía (6).
]]> El propósito del presente estudio es describir la incidencia, características clínicas y evolución de las HSM producidas en el curso del tratamiento con TFD en nuestro medio.
Sujetos, material y métodos
El estudio incluye 504 ojos de 470 pacientes (1.221 sesiones de TFD) con diagnóstico de NVC secundaria a DMAE, y miopía magna (MM), que inician tratamiento con TFD desde julio de 2002 hasta junio de 2005 en el Servicio de Oftalmología de nuestro Centro. La TFD se aplica según los parámetros estándar [infusión intravenosa de 6 mg/m2 de verteporfino durante 10 minutos (Visudyne, Novartis, Bülach, Switzerland), y aplicación de láser de diodo de 689 nm (Zeiss, Oberkochen, Germany), 50 J/cm2 e intensidad de 600 mW/cm2, con un tiempo de exposición de 83 segundos].
Se trata de 310 mujeres (61,5%) y 194 varones (38,5%). La edad media de la serie, es de 71,52 DE 13,66 años (26,03-93,21; 77,31).
En la primera visita se realiza una exploración oftalmológica completa, que incluye: mejor AV corregida, medida de la tensión intraocular (TO), exploración del segmento anterior, valoración del segmento posterior con lámpara de hendidura (LH) y lente de 78 dioptrías o lente de contacto y AFG digitalizada.
Después de administrada la TFD, el paciente es citado en el plazo de tres meses para nueva valoración de AV, exploración de fondo de ojo y AFG, y así decidir la conveniencia de re-TTO. Asimismo, el paciente es instruido para evitar la exposición a la luz directa durante 48 horas tras la TFD, y para acudir de forma urgente si presenta pérdida de AV visual durante el período entre visitas, dolor o síntomas de fotosensibilidad cutánea.
La indicación del TTO se ha realizado según los criterios propuestos por los estudios TAP y VIP (1,3), siendo modificados a medida que aparecían nuevas publicaciones de los mismos. Según esto, las indicaciones se han ampliado con el tiempo, desde las NVC predominantemente clásicas y secundarias a miopía en un primer período, hasta las NVC ocultas y mínimamente clásicas. También se han estudiado otras indicaciones de TFD fuera de los protocolos TAP y VIP, como NVC secundarias a patología inflamatoria, coroidopatía serosa central (CSC), estrías angioides, idiopáticas, NVC polipoidea, proliferación angiomatosa retiniana. En éstas no ha habido ningún caso de HSM, por lo que no figuran en la estadística, siendo ésta referida a los casos de DMAE y MM.
Respecto al tipo de lesión, se aplicaron los criterios angiográficos de los estudios TAP y VIP, clasificándolas en predominantemente clásicas, mínimamente clásicas, y ocultas sin componente clásico.
La indicación de re-TTO se ha realizado también de acuerdo con los criterios de dichos estudios: presencia de fuga de contraste en la AFG, o signos de actividad como fluido sub-retiniano o hemorragia no presente en la visita previa.
]]> Se ha considerado HSM aquella hemorragia producida en el curso del TTO con TFD, que afectando el centro de la mácula, justifica una disminución de AV importante y/o impide valorar las características de la lesión y/o la necesidad de re-TTO.En cada visita se recogen datos tales como, mejor AV corregida, patología que motiva el TTO, tipo angiográfico de la lesión, tamaño de la misma, si recibe o no TTO, así como efectos secundarios o complicaciones derivadas del mismo. Éstos son almacenados en una base de datos (Microsoft Acces for Windows, versión 9.0.0.2719), para luego realizar el análisis estadístico con el paquete informático S.A.S. versión 8.02 (from S.A.S Institute Inc., Cary, N.C., USA).
Resultados
Han presentado HSM 8 casos de los 504 ojos tratados por NVC secundaria a DMAE o MM, lo que supone una incidencia del 1,58%; de éstos la mitad precisó vitrectomía para su desplazamiento del área macular, es decir, un 0,79%. La probabilidad de presentar HSM por cada sesión de TFD es de 0,65% (8/1221).
La edad media de los ocho casos es de 76,75 DE 8,9 años (69-93; 72), 5 casos de 194 (2,57%) eran varones y 3 de 310 (0,96%) mujeres. No hubo diferencias estadísticamente significativas en cuanto a edad ni sexo de los casos respecto del total de la serie.
De los ocho casos, siete (87,5%) se han presentado en pacientes con DMAE, lo que supone una incidencia del 2% respecto a todos los casos de DMAE (7/349). El caso restante era miope magna y presentaba signos de maculopatía asociada a la edad, por lo que se incluyó como lesión mixta, con una incidencia del 0,64% (1/155) respecto al total de lesiones miópicas tratadas (fig. 1). De los ocho casos de HSM, tres tomaban anticoagulantes orales y cinco no. Asimismo, un paciente presentaba hipercolesterolemia, tres tenían hipertensión arterial y un caso estaba en TTO por cardiopatía isquémica. Las características más reseñables de la serie se resumen en la tabla I.

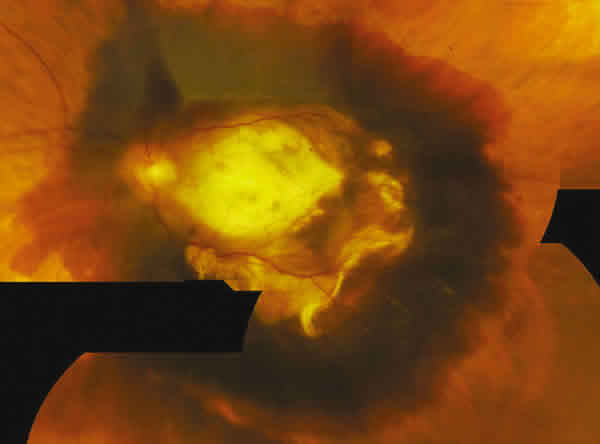
Fig. 1. HSM pseudotumoral, de 21.800 micras de GLD,
en lesión no valorable por presentar la paciente ]]>
alergia a fluoresceína. NVC mixta, secundaria
a DMAE y miopía magna. AV final, 0,005.
En cuanto a la presentación clínica de inicio, cinco de los ocho casos eran lesiones de tipo oculto, esto es, un 62,5% del total de hemorragias. El resto se presentaron en una lesión mínimamente clásica (12,5%), en otra predominantemente clásica (12,5%), y otra que no era valorable (12,5%) pues no se realizó AFG al ser la paciente alérgica a la fluoresceína (fig. 1).
La incidencia respecto a cada tipo de lesión considerado fue de 0,29% en las predominantemente clásicas (1/344), 2,8% en mínimamente clásicas (1/36), y 4,7% en ocultas (5/105). Esta diferencia resultó significativa tras el análisis estadístico, con una p=0,01, es decir, existió asociación estadísticamente significativa entre el tipo de lesión al inicio y la probabilidad de tener una HSM.
En cuatro casos la hemorragia ocurrió tras la primera sesión de TFD, en dos tras la segunda, y en otros dos tras la tercera.
Respecto al tiempo de aparición, se pueden diferenciar dos grupos: HSM precoces, antes de los 10 días tras la TFD, en dos casos, y HSM tardías, ocurridas después de 6 semanas, en cinco casos. Un paciente no refirió pérdida de visión y la hemorragia fue un hallazgo en la visita de re-tratamiento. Estos dos grupos presentan también carácterísticas diferenciales:
HSM precoces, centrales, de pequeño tamaño (figs. 2 y 3).
HSM tardías (después de 6 semanas, hasta 3 meses), periféricas a la lesión, de gran tamaño, pseudotumorales (figs. 1, 4 y 5).
]]>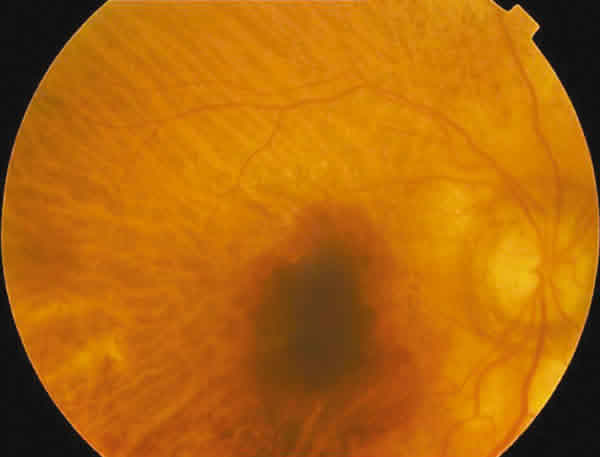
Figs. 2 y 3. Lesión oculta con hemorragia asociada,
que desarrolló una HSM central 9 días tras
la primera TFD. AV final, 0,05.
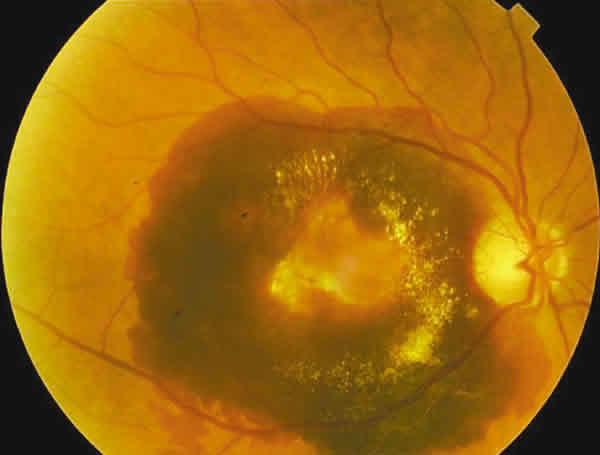
Figs. 4 y 5. NVC oculta que desarrolló una
HSM tras la tercera TFD. Se da la circunstancia
de que esta paciente tomaba sintrom. AV final, 0,02.
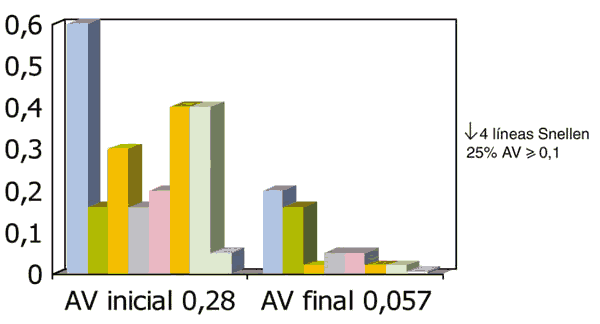
Respecto a la AV, ésta era al inicio 0,28 de media, pasando a 0,057 al final del seguimiento, lo que supuso una pérdida media de 4 líneas de Snellen (fig. 6). Únicamente un paciente mantuvo su AV y todos los demás perdieron visión. Dos pacientes (25%) tenían una AV >– 0,1 al final del seguimiento (una lesión predominantemente clásica y otra mínimamente clásica), mientras en los seis restantes (75%) la AV era < de 0,1.
]]>
La AV final media de los diferentes grupos de lesiones se ilustra en la figura 7. Se puede apreciar que la AV final media de los casos con HSM (0,05), es menor que la AV final media de DMAE (0,15), y menor que la AV final media de las lesiones ocultas (0,30).
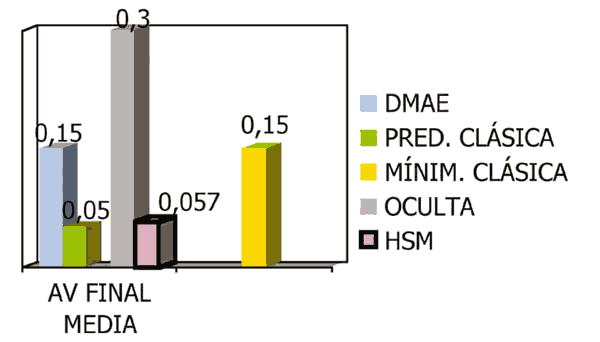
Fig. 7. Comparación de AV final media según el tipo de lesión.
En cuanto al tamaño de la lesión, pasó de 4.000 a 10.000 micras de tamaño medio (GLD), multiplicandose por 2,6 (fig. 8). Se dio la circunstancia de que las HSM precoces apenas aumentan el tamaño de la lesión, y, sin embargo, las tardías aumentan todas, llegando en algún caso a ser 6 veces mayor que GLD inicial.
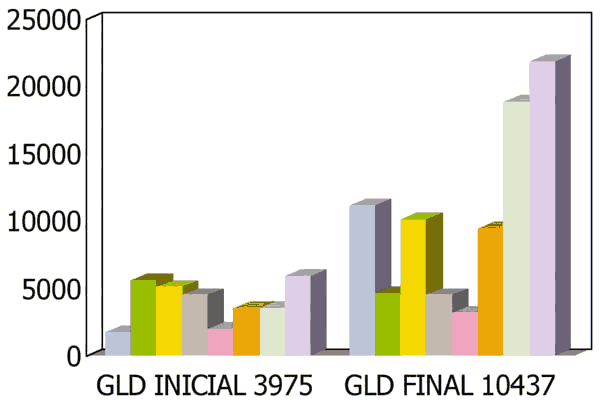
Fig. 8. Tamaño inicial y final de cada paciente ]]>
con HSM (GLD en micras; cada paciente, una barra).
Finalmente, cuatro casos necesitaron cirugía para desplazar la hemorragia, tres de los cuales se presentaron en lesiones ocultas y el cuarto en una lesión no valorable. Estos pacientes también asociaron agudezas visuales bajas (–<0,05) (tabla I).
Discusión
Los estudios TAP y VIP han demostrado que, comparada con el placebo, la TFD reduce de manera significativa el riesgo de pérdida visual en pacientes seleccionados con NVC subfoveal secundaria a DMAE y MM. En el informe n.º 3 de los estudios TAP y VIP se analizan las causas de pérdida visual aguda grave tras TFD. En un paciente (1/402) del estudio TAP y en tres (3/225) del VIP la causa de la pérdida de AV severa fue una HSM, lo que supone una incidencia de 0,24% y 1,33% respectivamente (5). La incidencia en otros trabajos es variable, y oscila entre el 1,86% y 9% (6-8).
No se pueden comparar dichas incidencias con la encontrada en este trabajo por las diferencias metodológicas. En otros estudios, se ha hecho un estudio sistemático y protocolizado de los pacientes y además, no todos los estudios coinciden en el mejor momento para detectar estas hemorragias, por lo que el momento de analizar esta incidencia es diferente para cada uno. En nuestro caso, se han analizado aquellos pacientes que han acudido a consulta refiriendo pérdida visual antes de la fecha del re-TTO, y también los que han presentado HSM en el momento del mismo. Existe la posibilidad de perder pacientes en el seguimiento, ya sea porque ellos han rehusado nuevo tratamiento, o porque no han sido remitidos desde su hospital de referencia pues consideraron que su lesión no era tratable en ese momento. Por ello pensamos que la incidencia de HSM asociada a TFD en nuestro medio probablemente sea mayor, aunque no se puede cuantificar hasta qué punto. En cualquier caso, es baja y está en el rango de lo publicado.
También se puede afirmar que casi exclusivamente han aparecido en pacientes con diagnóstico de DMAE (7 de 8, 87,5%), pues sólo en uno de los casos de HSM la paciente tenía miopía magna, aunque la lesión fue clasificada como mixta, por presentar la paciente signos asociados de DMAE. Por esta razón probablemente la edad media de los ocho casos sea algo más elevada que la de la serie, y similar a la de los pacientes con diagnóstico de DMAE (77,54DE7,22).
Por otro lado, no hay ningún estudio hasta la fecha que analice esta complicación en relación con todos los tipos de lesiones, pues en el TAP la mayoría de lesiones son predominantemente clásicas, en el VIP hay mayor porcentaje de pacientes con lesiones ocultas, y en los otros estudios analizados, salvo el de Theodossiadis (7), sólo se ha tratado un tipo concreto de lesión (6,8). Éste es el primer estudio que tengamos conocimiento en el que se analizan todos los pacientes tratados durante un largo período de tiempo (3 años), en el que se incluyen lesiones y patologías de todo tipo.
Respecto al tipo de lesión, hemos encontrado una incidencia significativamente mayor en lesiones de tipo oculto, (4,7%; p=0,01), lo que indica que estas lesiones podrían tener un mayor riesgo de presentar esta complicación que el resto. La incidencia en el resto de lesiones es anecdótica y tampoco se pueden extraer conclusiones estadísticamente significativas debido al escaso número de casos presentados en cada grupo. Los estudios publicados apuntan una mayor incidencia de HSM en lesiones de tipo oculto, aunque en ninguno de ellos se llega a la conclusión de que ésta fuera estadísticamente significativa (5,6).
Además, las lesiones ocultas aglutinan a tres de los cuatro casos que han precisado intervención quirúrgica y presentan una AV final más baja (tabla I), lo que sugiere que las HSM asociadas a este tipo de lesiones tendrían peor pronóstico visual que el resto.
]]> Comparando la AV final de los casos que presentan HSM (0,05) con la media de NVC secundaria a DMAE (0,15), es claramente más baja (fig. 7), por lo que estos pacientes pierden más AV que aquellos que no presentan esta complicación. De todas formas, la AV final de los pacientes que presentaron pérdida de AV aguda grave en los estudios TAP y VIP era similar a la del grupo placebo (5), por lo que su situación no era peor que si no se hubieran tratado.En cuanto al número de TFD administradas, no parece haber relación con esta variable: en cuatro casos, la HSM ha ocurrido tras la primera TFD, en dos tras la segunda y en otros dos tras la tercera. Tampoco hemos encontrado relación con la toma de ACO (tabla I).
Es motivo de controversia el papel etiológico de la TFD en la producción de estas hemorragias. En el artículo de Theodossiadis et al (7) las hemorragias relacionadas con la TFD aparecen dentro de las 48 horas de su aplicación y tienen un tamaño final extremadamente grande, >12.000 micras, por lo cual concluye que no son parte de la evolución natural de la NVC. No obstante, las HSM también tienen lugar durante la evolución natural de las NVC; así en el estudio TAP 1 se presentaron hemorragias intrarretinianas y subretinianas en el 46% del grupo placebo y en el 29% del grupo tratado con verteporfino (1). Estas hemorragias no se relacionaron en el tiempo con la TFD, y se postula que pueden ser debidas a desgarros del epitelio pigmentario. Por otro lado, Bressler et al, en una serie de lesiones ocultas afirma que la probabilidad de presentar una HSM es mayor tras 2-3 meses post-TFD (6).
Después de estas consideraciones, parece lógico pensar que si una HSM se presenta precozmente tras la TFD, entre 48 horas-7 días, podría ser consecuencia directa de la TFD, secundaria a la fototrombosis vascular selectiva, respuesta inflamatoria, vasculitis y disfunción de barreras vasculares provocadas por la misma. Además, si la HSM es masiva, no es probable que forme parte de la evolución natural de NVC secundaria a DMAE (1).
Sin embargo, tampoco se puede afirmar, si es tardía que no sea secundaria a la TFD, pues se conoce que la trombosis de NVC es reversible, y a partir de 1 semana hay una recuperación de la circulación coriocapilar con repercusión y crecimiento de la NVC. Además, la TFD también provoca hipoperfusión de la coroides y coriocapilar sanas circundantes a la lesión, lo cual estimula la producción de VEGF, que en algunos casos origina el crecimiento en periferia de NVC (9). Estos dos efectos inherentes a la TFD podrían explicar las HSM tardías, que como hemos visto en nuestra serie, son las de mayor tamaño y de localización periférica.
En cualquier caso, no se pueden extraer conclusiones acerca del papel etiológico de la TFD en las HSM producidas en el curso del tratamiento de la DMAE u otras patologías.
Como conclusión final, pensamos que se debe informar a los pacientes de la posibilidad de disminución de AV moderada o grave asociada a HSM en el curso del TTO con TFD, la cual puede precisar cirugía, y que este riesgo es significativamente mayor en DMAE y en lesiones ocultas. En cualquier caso, consideramos que el bajo riesgo de HSM en relación con la TFD no contraindica el TTO cuando éste está indicado. Son necesarios más estudios para establecer la incidencia real de este suceso, así como para aclarar el papel etiológico de la TFD en el mismo.
Agradecimientos
Urko Agirre, de la Unidad de Epidemiología e Investigación clínica del Hospital de Galdakao, por el análisis estadístico de los datos.
]]>Bibliografía
1. Photodynamic therapy of subfoveal choroidal neovascularization in age-related macular degeneration with verteporfin: one year results of 2 randomized clinical trials—TAP report. Treatment of age-related macular degeneration with photodynamic therapy (TAP) Study Group. Arch Ophthalmol 1999; 117: 1329-1345. [ Links ]
2.Bresslet NM; Treatment of Age-Related Macular Degeneration with Photodynamic Therapy (TAP) Study Group. Photodynamic therapy of subfoveal choroidal neovascularization in age-related macular degeneration with verteporfin: two-year results of 2 randomized clinical trials-Tap report 2. Arch Ophthalmol 2001; 119: 198-207. [ Links ]
3.Verteporfin in Photodynamic Therapy Study Group. Photodynamic therapy of subfoveal choroidal neovascularization in pathologic myopia with verteporfin. one-year results of a randomized clinical trial. VIP report no.1. Ophthalmology 2001; 108: 841-852. [ Links ]
4.Verteporfin In Photodynamic Therapy Study Group. Verteporfin therapy of subfoveal choroidal neovascularization in age-related macular degeneration: two-year results of a randomized clinical trial including lesions with occult with no classic choroidal neovascularization--verteporfin in photodynamic therapy report 2. Am J Ophthalmol 2001; 131: 541-560. [ Links ]
5.Arnold JJ, Blinker KJ, Bressler NM, Bressler SB, Burdan A, Haynes L, et al. Acute severe visual acuity decrease after photodynamic therapy wtih verteporfin: case reports from randomized clinical trials-TAP and VIP report no. 3. Am J Ophthalmol 2004; 137: 683-696. [ Links ]
6.Do DV, Bressler NM, Bressler SB. Large submacular hemorrhages after verteporfin therapy. Am J Ophthalmol 2004; 137: 558-560. [ Links ]
7.Theodossiadis GP, Panaglotidis D, Georgalas IG, Moschos M, Theodossiadis PG. Retinal hemorrhage after photodynamic therapy in patients with subfoveal choroidal neovascularization caused by age-related macular degeneration. Graefes Arch Clin Exp Ophthalmol 2003; 241: 13-18. [ Links ]
8.Gelisken F, Inhoffen W, Karim-Zoda K, Grisanti S, Partsch M, Voelker M, et al. Subfoveal hemorrhage after verteporfin photodynamic therapy in treatment of choroidal neovascularization. Graefes Arch Clin Exp Ophthalmol 2005; 243: 198-203. [ Links ]
9.Arroyo JG, Michaud N, Jacobiec FA. Choroidal neovascular membranes treated with photodynamic therapy. Arch Ophthalmol 2003; 121: 898-903. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Enrique Díaz de Durana Santa Coloma
Hospital de Galdakao
Barrio de Labeaga, s/n
48960 Galdakao (Vizcaya)
España
E-mail: lezeaga@vodafone.es