
Clasificación y caracterización biológica de los tumores neuroendocrinos del tracto gastrointestinal
A. Astudillo
Servicio de Anatomía Patológica II. Hospital Central Universitario. Asturias (Oviedo)
RESUMEN
]]> La actual Clasificación Internacional de las Neoplasias del Tracto Gastronitestinal publicada por la OMS en el año 20001, deriva de la CIEO-10 y como todas las anteriores tiene una base histogenética. Pero a diferencia de las otras ediciones, se ha ampliado para incluir datos clínicos específicos que conllevan implicaciones patogénicas moleculares de valor pronóstico. En este trabajo se resumen las principales características morfológicas e inmunohistoquímicas de estos tumores segmentándolos por localizaciones tumorales, ya que su comportamiento se relaciona parcialmente con la localización topográfica.
Fenotipo de los tumores neuroendocrinos del tracto gastrointestinal
La célula tumoral en todos ellos reproduce con mayor o menor grado de diferenciación las características de la célula neuroendocrina intraepitelial, ubicada en la mucosa, tanto en el revestimiento como en las criptas y aisladamente en la lámina propia. Cuando observamos al microscopio electrónico cualquier parte del tubo digestivo, vemos células aisladas, dispersas, justo en la porción basal de las células epiteliales, entre éstas y la membrana basal. Destacan por un carácter morfológico muy distintivo: la presencia de abundantes gránulos de neurosecreción en su citoplasma. Aunque no tienen conexiones directas con las terminaciones nerviosas de la lámina propia, están muy próximos a éstas.
Aunque durante mucho tiempo se aceptó que estas células, que forman parte del sistema neuroendocrino difuso, procedían embriológicamente de la cresta neural, como todas las células del sistema nervioso vegetativo entérico (para las que la demostración de esta evidencia vino de mano de Le Douarin en sus elegantes experimentos con células quimera), esta aseveración fue refutada y actualmente se acepta que al menos una parte de las células neuroendocrinas proceden de una diferenciación específica a partir de la célula primitiva pluripotencial del epitelio entérico, de origen endodérmico, quizás bajo la inducción del entorno y muy particularmente de los nervios vecinos. Pero esta célula neuroendocrina entérica, adscrita al obsoleto grupo clasificado como de las células APUD ("amine precursor uptake and decarboxilation"), como todo el sistema neuroendocrino difuso, tiene unas propiedades más próximas a las células nerviosas que a los epitelios.
En el páncreas, la distribución de este sistema neuroendocrino es algo diferente, ya que en vez de aparecer dispersas, las células se agrupan en islotes ricamente vascularizados.
Una de las principales propiedades de estas células radica en su extraordinaria capacidad de producir sustancias peptídicas, almacenadas en las vesículas de neurosecreción, con unas afinidades tintoriales por las que fueron denominadas "cromafines" y "argentafines". De ellas, las primeras identificadas fueron gastrina, secretina y colecistoquinina. Hoy se conoce que puede haber en estas células más de 100 diferentes péptidos bioactivos, codificados por 30 genes, además de otros mensajeros hormonales (Tabla I). Algunas de estas sustancias tienen actividad como factores de crecimiento.
]]>

Los tumores neuroendocrinos gastrointestinales tienen la capacidad de producir estas sustancias pero, al igual que en sus contrapartidas celulares normales, con diferencias de expresión peptídica en las distintas zonas del tracto gastrointestinal.
Clasificación de los tumores neuroendocrinos gastrointestinales
La actual clasificación de la OMS (Tabla II) de los tumores neuroendocrinos del tracto gastrointestinal varía según el órgano. No ha incorporado los criterios sustentados por el grupo de Solcia y Capella2 y otros autores que, al igual que sugirió Travis para los tumores neuroendocrinos pulmonares, separan los carcinoides en típicos y atípicos. Para los tumores neuroendocrinos del tracto gastrointestinal, este grupo describe tres variantes tumorales: tumor carcinoide típico, carcinoide atípico y carcinoma de célula pequeña, con subtipos relacionados con datos clínicos asociados.
La exclusión de la variante atípica de carcinoide en la clasificación de la OMS puede justificarse por no haber sido demostrado fehacientemente su valor pronóstico. El estudio holandés3 de 56 casos entre otros así lo asevera. Sin embargo, hay otras publicaciones que apoyan el criterio de Solcia y Capella.
Para que un tumor entre dentro de esta clasificación, debe demostrar su diferenciación neuroendocrina. Algo que ancilarmente se demostraba por la afinidad de la célula tumoral por la plata, directamente o con pretratamiento reductor (argirofilia o argentafinidad)4 o por la presencia de gránulos de neurosecreción en el estudio ultraestructural y que actualmente se demuestra con inmunohistoquímica positiva para dos o más marcadores neuroendocrinos (enolasa, sinaptofisina, cromogranina, Leu 7 son los más utilizados).
]]> Dado que los criterios morfológicos, inmunohistoquímicos y ultraestructurales para la definición del carácter neuroendocrino están bien establecidos (ver Tabla III), y en el supuesto de que se conozcan los datos clínicos complementarios (diagnóstico de MEN-1, gastritis atrófica) la clasificación de esos tumores no parece difícil. Si bien se debe tener en cuenta un criterio numérico: un destacable número de adenocarcinomas del tracto gastrointestinal, como sucede en tumores epiteliales de otros órganos, expresa diferenciación neuroendocrina en células aisladas, lo cual no tiene ninguna significación ni se acepta por ello su agrupación como entidad separada. Pero se ven tumores en los que este fenotipo neuroendocrino supone más del 50% de un adenocarcinoma convencional: en este caso debe clasificarse como una forma mixta. Y también se dan tumores en los que la célula proliferente expresa un doble fenotipo: de adenocarcinoma mucosecretor, comúnmente en la forma de células "en anillo de sello" y con gránulos de neurosecreción: son las denominadas formas adenocarcinoides.
Carcinoide típico
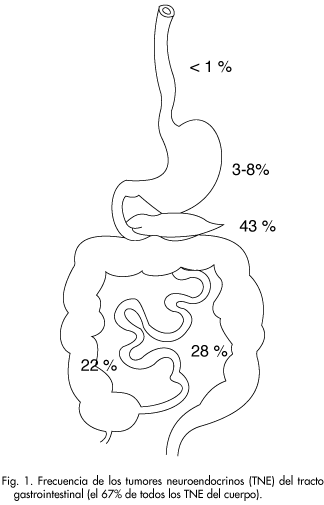
Es un tumor muy bien conocido en órganos cuyo revestimiento interno procede embriológicamente del endodermo: pulmón, tubo digestivo, hígado y otros. Su frecuencia varía a lo largo del tracto gastrointestinal, que por relación con el origen embriológico ha sido agrupado como intestino anterior, medio y posterior. En el esquema (Fig.1) pueden verse las frecuencias.
Su tamaño es muy variable, aunque suele aparecer como tumores circunscritos, ricamente vascularizados, sin necrosis.
La inclusión de un tumor dentro de este grupo es fácil para un patólogo y no suele ofrecer dudas. Los patrones de crecimiento, característicos y armoniosos, forman nidos con empalizada periférica (Tipo A), grupos de borde festoneado (Tipo B) o rosetas y glánadulas (Tipo C) con formas mixtas. Por técnicas de inmunohistoquímica o ultraestructura, se puede determinar su contenido citoplásmico.
]]> La frecuencia de síndrome carcinoide asociado a ellos varía con la localización. La misma serotonina que lo produce sirve para su detección con métodos no invasivos, que se facilita con el marcaje del octreótrido, un análogo de la serotonina descrito en 1976.Ya desde la publicación clásica de Askanazy5 y la de Hakanson6 se sabe que este tipo de tumor es más frecuente en pacientes con hipergastrinemia, por gastritis crónica atrófica tipo A (A-CGA) o por síndrome de Zollinger-Ellinson (ZES). Dado que estas formas difieren en comportamiento biológico del carcinoide esporádico sin hipergastrinemia, se propuso una clasificación separada, que es la que actualmente ha sido aceptada por la OMS y prevalece.
Carcinoide atípico
Aunque no reconocido por la clasificación de la OMS, es de uso por la convicción del grupo de Capella sobre el interés pronóstico de su demarcación separada del carcinoide típico. Su frecuencia varía según las series.
No es tan fácil incluir a un tumor dentro de este grupo, ya que se debe pensar en él: detectar en la tinción simple de Hematoxilina-Eosina los caracteres morfológicos de diferenciación neuroendocrina, por encima de otros: formación de rosetas, carácter finamente granular del citoplasma, cromatina en finos grumos, etc. Una vez sospechado, se debe confirmar con marcadores de diferenciación neuroendocrina, que deben hacerse inexcusablemente para establecer el diagnóstico.
Y ello es muy importante, porque este subtipo tumoral tiene unas características de comportamiento que difieren radicalmente de los carcinoides típicos: en particular, la extraordinaria frecuencia de diseminación linfática submucosa, particularmente en las formas yeyunales y la no respuesta a quimioterapia convencional.
Lo que lo hace distinto del carcinoide no es sólo el comportamiento: al microscopio siempre tiene áreas de necrosis y abundantes mitosis, que nunca se ven en el carcinoide.
Es, pues, uno de los muchos tumores en los que la correlación clínico-patológica es clara. El problema radica en que algunos de los carcinoides típicos tienen el mismo comportamiento agresivo que los atípicos, y ello debilita el poder de esta subclasificación de los carcinoides.
Carcinoma de célula pequeña
La OMS la admite como una forma de carcinoma neuroendocrino del tracto gastrointestinal.
]]> Es más frecuente en el esófago que en otras localizacionesSuele ser un tumor de tamaño muy variable.
Para diagnosticarlo, además de la morfología de célula pequeña difusa, debe demostrarse, como en los otros tumores de su grupo, la diferenciación neuroendocrina.
Características diferenciales de los tumores gastrointestinales neuroendocrinos según su localización
Esófago
En esta localización, los tumores neuroendocrinos carcinoides suelen ser grandes e infiltrantes, con características microscópicas típicas, por lo que cabe deducir que se detectan en estadios avanzados por carecer de síntomas neuroendocrinos y retardar la presentación de la clínica obstructiva.
Los tumores de célula pequeña son indistinguibles de su contrapartida pulmonar. Expresan marcadores neuroendocrinos y ocasionalmente tienen zonas de diferenciación escamosa o glandular.
Estómago
Relación de la hipergastrinemia con el tumor carcinoide
]]> La gastrina se ha demostrado como un potente agente trófico para las células neuroendocrinas gastrointestinales, habiéndose descrito morfológicamente una secuencia desde displasia a neoplasia como etapas hacia la malignización7 en los pacientes con hipergastrinemia. Esto tiene lugar en las personas con gastritis crónica atrófica autoinmune (A-CAG), en el síndrome de Zollinger-Ellinson (ZES), y en la Neoplasia Endocrina Múltiple tipo I (MEN-1) con ZES asociado. Pero parece que la gastrina por sí sola no es suficiente, como lo corroboran los casos de ZES esporádico. Sin embargo, la frecuencia de carcinoides se eleva notablemente en pacientes en los que el ZES se da en un contexto de MEN-1, enfermedad asociada a mutación en el gen de la menina, en el cromosoma 11q13 considerado como gen supresor.El grupo de Capella reconoce estos tres subtipos de carcinoide gástrico: Tipo I, asociado con gastritis crónica atrófica autoinmune (A-CAG); Tipo II, asociado con MEN-1 y ZES, y Tipo III, esporádico, o no asociado con hipergastrinemia o A-CAG. Esta clasificación se apoya en diferencias clinicopatológicas: los de Tipo I y II se presentan hiperplasias y displasias de las células enterocromafines y suelen ser tumores pequeños y múltiples. Los de Tipo III suelen ser grandes y no funcionantes, aunque hay casos con síndrome carcinoide atípico sin diarrea. Al microscopio, en los Tipos I y II se observa el característico aspecto "carcinoide" de ordenación regular en trabéculas o nódulos formados por células monomorfas con escasas mitosis o grado 1 de la clasificación de Rindi8. Pero en el Tipo III , las células tienen un mayor índice mitótico y necrosis, es decir, características de grado 2 de Rindi, con mayor tendencia invasora. Por ello, las formas esporádicas suelen ser más agresivas que las Tipo I y II.
Duodeno
En él se localizan la mayor parte de los tumores carcinoides de intestino delgado9 que suelen concentrarse entre la primera y segunda porción del duodeno. Suelen ser pequeños. Los secretores de gastrina tienen morfología de carcinoides típicos grado 1. Los secretores de somatostatina tiene con frecuencia cuerpos de psamoma y apariencia glandular y también son grado 1. Pero a pesar de su apariencia, pueden tener un comportamiento muy agresivo.
Pacientes con neurifibromatosis grado I tienen riesgo elevado de tumores periampulares, que suelen ser somatostatinomas.
Su comportamiento se relaciona con el nivel de invasión, particularmente si rebasan la submucosa o dan metástasis y con el tipo de hormona que producen. Son agresivos la mitad de los asociados a ZES-MEN-1 y los esporádicos con ZES. Los gastrinomas asociados a ZES tienen peor pronóstico que las formas no funcionantes.
Hígado y páncreas
La clasificación de la OMS no contempla los carcinoides primarios hepáticos, que deben ser incluidos en el capítulo de "otros". Aunque extraordinariamente infrecuentes y siempre descartando metástasis de un primario extrahepático, han sido descritos probablemente de origen en las vías biliares intrahepáticas, como se pueden ver a lo largo de todo el tracto de las vías biliares y páncreas. El origen embriológico común de estas estructuras lo justifica.
Yeyuno-ileon
Los tumores neuroendocrinos de esta zona suelen ser múltiples en el 25-30% de los casos. Forman nódulos que protruyen desde la submucosa a la mucosa y con frecuencia invaden muscular y peritoneo, causando fibrosis y cuadros obstructivos.
]]> Su patrón microscópico de crecimiento, al igual que sucede en otros carcinoides, es armonioso y puede hacer mezcla de patrones. La secreción de sus vesículas suele ser similar a su contrapartida, la célula enterocromafin de la zona: producen sustancia P y otras taquiquininas, como la neurokinina A; encefalina, somatostatina, etc. Pero su apariencia microscópica no se correlaciona con el pronóstico, que parece depender de su capacidad metastásica. Los tumores de menos de 1 cm que no invaden vasos, se localizan en mucosa y submucosa y no son funcionantes, se curan con resección completa. La agresividad está marcada por invasión más allá de la submucosa o las metástasis.Apéndice
La mayor parte de los carcinoides de apéndice son un hallazgo incidental. Suelen ser asintomáticos en el ápex y sólo en algunos casos los localizados en otras porciones del apéndice dan síntomas de apendicitis, pero rara vez dan síndrome carcinoide, que cuando está presente, suele asociarse a formas avanzadas de la enfermedad. Las formas de carcinoides de células caliciformes tienen la peculiaridad de infiltrar con células dispersas, como los carcinomas difusos gástricos, por lo que son difíciles de sospechar macroscópicamente. De forma similar, el carcinoide tubular tiene un patrón diferente del carcinoide clásico, por lo que suele ser mal diagnosticado: forma cordones y glándulas dispersas, que pueden contener mucina en su luz. Junto con los caliciformes, se agrupa como formas mixtas adeno-carcinoides.
El factor de riesgo más importante es el tamaño del tumor y la invasión del meso apéndice.
La OMS los sublcasifica según su producción hormonal, atendiendo especialmente a las formas productoras de serotonina, glucagon y péptido Y.
Colon y recto
Los tumores endocrinos de esta localización son más frecuentes en el recto (54%) seguido del ciego (20%) y sigma (7,5%). Menos del 5% presentan síndrome carcinoide10. Los tumores de recto suelen formar masas polipoideas submucosas, de pequeño tamaño y únicas, aunque hay formas mayores y adheridad a capas profundas. En el colon derecho suelen ser mayores.
En el examen microscópico, suelen adoptar el patrón carcinoide clásico, con gránulos citoplásmicos positivos para serotonina, glucagon, péptido Y, sustancia P, etc.
Una curiosidad inmunohistoquímica de los carcinoides de recto es la positividad para fosfatasa ácida prostática, menos común en carcinoides de otras zonas del tracto gastrointestinal y probablemente en relación con el origen embrionario común con el epitelio prostático11.
Los carcinomas de célula pequeña con diferenciación neuroendocrina de esta localización, corresponden al grado 3 de la clasificación de Rindi. Suelen localizarse en colon derecho y se asocian con frecuencia un adenoma o adenocarcinoma. Suelen tener metástasis hepáticas en el momento del diagnóstico.
]]> De forma muy aislada, se han descrito carcinomas neuroendocrinos de célula grande de características similares a los del pulmón12.Mecanismos moleculares que modulan la diferenciación neuroendocrina y su relación con el proceso de malignización. Hacia una clasificación molecular de las neoplasias endocrinas del tracto gastrointestinal
Los carcinoides reciben su denominación de su comportamiento de baja agresividad. Sin embargo, hay formas agresivas, no predecibles por la morfología indolente. Es del máximo interés conocer los mecanismos moleculares que subyacen, y encontrar marcadores fáciles de usar, inmunohistoquímicos, relacionados con estos mecanismos. La búsqueda puede venir a partir del proceso fisiológico evolutivo de la célula de origen. La célula neuroendocrina del tracto gastrointestinal comparte nicho topográfico con la célula de más rápida multiplicación de nuestro organismo: la célula primitiva basal del epitelio intestinal. Y sin embargo, es de muy baja actividad proliferativa, probablemente por silenciamiento de genes de proliferación. Esto podría guardar relación con la baja actividad proliferativa del carcinoide típico. Pero además, la célula neuroendocrina, como producto final de la diferenciación del neuroectodermo, o inducida fuertemente por el mismo, ha sobrevivido a la criba apoptótica y, en similitud con los elementos maduros del sistema nervioso, es altamente resistente a la muerte apoptótica. También es muy infrecuente la apoptosis en los tumores carcinoides. Esta resistencia no parece ser explicada por la sobreexpresión de bcl-2, que no es característico de ellos.
Además de la búsqueda de razones que justifiquen la baja agresividad de los carcinoides en general y quizás con mayor interés, está la búsqueda de indicadores inmunohistoquímicos o moleculares del comportamiento agresivo de algunos de ellos. En esa búsqueda hay un enlace razonable con los mecanismos de regulación del desarrollo de estos tipos celulares: tanto el TGFb 1 como otro factor de transcripción el SNAIL, están altamente regulados en el desarrollo del neuroectodermo en su fase más precoz: NOTCH, el generador de la diferenciación local neuroectodérmica en la capa del ectodermo, induce, como mecanismo fisiológico altamente regulado la expresión de SNAIL, cooperando a la vez RAS con TGFb en la embriogénesis, en la secuencia de señales de transición del epitelio a mesénquima que culminan en el silenciamiento de genes. Se sabe que SNAIL es capaz de potenciar la transición epitelio-mesénquima, promoviendo la pérdida de expresión de E-cadherina. Un mecanismo altamente regulado, en el que intervienen otras familias de inhibidores génicos. Y recientemente se ha demostrado que una de las características que diferencia los carcinoides indolentes de los agresivos, es la pérdida de E-cadherina en estos últimos13 Se sabe que en algunos tumores, las mutaciones en SNAIL inducen su sobreactivación, y este solo mecanismo hace que se sobreexprese en las zonas invasivas. Amparo Cano propone un modelo en que SNAIL mutado, como represor de cadherina E, pueda actuar en la fase inicial de la transformación neoplásica de los tumores, contribuyendo otros genes a la progresión.
Otra vía de búsqueda de genes responsables es la de las formas familiares. Se han descrito tumores carcinoides más frecuentes en pacientes con MEN-1, ZES y A-CAG. Por tanto, puede pensarse que en las formas esporádicas los mecanismos de malignización sigan unas rutas mutacionales similares a la delección del gen supresor MEN, o a la acción promotora de la proliferación de la gastrina. Pero los carcinoides esporádicos difieren de estos por razones de mecanismo molecular de la malignización y también difieren por comportamiento. Aún así, la ruta de búsqueda de mecanismos de malignización comienza por las formas conocidas antes citadas.
La gastrina es promotora de la proliferación de las células neuroendocrinas. ¿La malignización de las células "enterocromafi-like" por la gastrina tiene una secuencia molecular conocida? Parece que el efecto proliferativo de la gastrina no basta: pacientes con ZES esporádico con diez veces más gastrina no desarrollan tantos carcinoides. Pero los pacientes con MEN-1 y ZES (54%) tienen 30 veces más carcinoides. La explicación puede estar en que la pérdida de menina, la proteína deficitaria en los MEN-1, parece "downregular" el factor de transcripción SMAD 3, efector de la acción antiproliferativa del factor de crecimiento transformante TGFb1. Este último se ha hipotetizado como el secreto que justifica la baja actividad proliferativa del carcinoide, ya que estos tumores sobreexpresan receptores para el TGFb (TGFbR)
Estamos aún lejos de un modelo de mecanismo mutacional que explique la secuencia del carcinoide. Pero al menos tenemos algunas evidencias: una de ellas es que pueden actuar distintos mecanismos, dependiendo del tracto gastrointestinal afectado, ya que en los carcinoides de intestino anterior parece actuar la delección de MEN-1, en los de intestino medio, pérdidas asociadas a 18, 11q y 16q, y en los de intestino posterior, sobreepresión de EGFr y TGFa14
Bibliografía
1. Hamilton SR, Aaltonen LA. Pathology and genetics of tumours of the digestive system. World Health Organization Classification of Tumours. IARC Press, Lyon 2000. [ Links ]
2. Rindi G, Luinetti O, Cornaggia M, Capella C, Solcia E. Three subtypes of gastric argyrophil carcinoids and the gastric neuroendocrine carcinoma: a clinicopathological study. Gastroenterology 1993; 104:994-1006. [ Links ]
3. Van Eeden S, Quaedvlieg PF, Taal BG, Offerhaus GJ, Lamers CB, Van Velthuysen ML. Classification of low-grade neuroendocrine tumors of midgut and unknown origin. Hum Pathol 2002; 33:1126-32. [ Links ]
4. García del Moral R. Laboratorio de Anatomía Patológica. Ed Interamericana, Madrid 1993. [ Links ]
5. Askanazy M. Pathogenese der Magenkrebse und uber ihren gelegentlichen Ursprung angeborenen epithelialen Keimer in der Magenwand. Dtsch Med Wochennschr 1923; 49:49-51. [ Links ]
6. Hakanson R, Sundler F eds. Mechanisms for the development of gastric carcinoids (proceedings of an International Symposium, Mondal, Sweden, February 6, 1985). Digestion 1986; 35 (Suppl 1)1-152. [ Links ]
7. Creutzfeldt W. The achlorydria-carcinoid sequence: role of gastrin. Digestion 1988; 39:61-79. [ Links ]
8. Rindi G, Azzoni, C, La Rosa S, Klersy C, Palotti D, Rappel S, Solte M, Capella C, Bordi C, Solcia E. ECL cell tumor and poorly differentiated endocrine carcinoma of the stomach: prognostic evaluation by pathological analysis. Gastroenterology 1999; 116:532-42. [ Links ]
9. Rindi G, Luinetti o, Cornaggia M, Capella C, Solcia E. Three subtypes of gastric argyrophil carcinoid and the gastric neuroendocrine carcinoma: a clinicopathologic study. Gastroenterology 1993; 104:994-1006. [ Links ]
10. Rosemberg JM, Welch JP. Carcinoid tumors of the colon. A study of 72 patients. Am J Surg 1985; 149:775-9. [ Links ]
11. Federspiel BH, Burke AP, Sobin LH, Shekitka KM. Rectal and colonic carcinoids. A clinicopathologic study of 84 cases. Cancer 1990; 65:135-40. [ Links ]
12. Travis WD, Linnoliola RI, Tosokos MG, Hitchcock CL, Cutler GB, Nieman L, Chrousos G, Pass H, Doppmann J. Neuroendocrine tumors of the lung with proposed criteria for large cell neuroendocrine carcinoma. An ultrastructural, inmunohistochemical, and flow cytometric study of 35 cases. Am J Surg Pathol 1991; 15:529-53. [ Links ]
13. Kawahara M, Kammori M, Kanauchi H, Noguchi C, Kuramoto S, Kaminishi M, Endo H, Takubo K Immunohistochemical prognostic indicators of gastrointestinal carcinoid tumours.Eur J Surg Oncol 2002; 28:140-6. [ Links ]
14. Leotlela PD, Jauch A, Holtgreve-Grez H, Thakker RV. Genetics of neuroendocrine and carcinoid tumours. Endocr Relat Cancer 2003; 10:437-50. [ Links ] ]]>