Tratamiento hormonal del cáncer de mama
I. Herruzo
Servicio de Oncología Radioterápica. Hospital General Carlos Haya. Málaga
Las modalidades de tratamiento supresor de estrógenos las podemos agrupar en 1-3:
]]> 1) estándar: castración quirúrgica o RT;2) antiestrógenos: moduladores selectivos del RE (SERM)); trifeniletilenos: tamoxifen, toremifeno, clomifeno, droloxifeno; benzotiofenos: raloxifeno; antiestrógenos puros: ICI 182780 (faslodex); reguladores por disminución selectiva de receptores de estrógenos;
3) inhibidores de aromatasa (IA): según su mecanismo de acción, dos tipos:
Tipo I: derivados esteroideos de la androstendiona (provocan una unión covalente irreversible con la enzima, provocándole perdida funcional): formestano (1a generación), exemestano (2a generación) y el atamestano (3a generación).
Tipo II: inhibidores no esteroideos (inhibición reversible, con el citocromo P450 de la aromatasa): aminoglutetimida (1a generación), fadrozol (2a generación) y letrozol, anastrozol y vorazol (3ª generación).
4) Análogos de Gh-Rh.
Inhiben el efecto pulsátil de la GnRH sobre el hipotálamo, anulando así la función ovárica o testicular. Al ser polipéptidos se degradan en el intestino, de ahí su uso por vía intra muscular, subcutánea o intranasal. Aministrados agudamente: efecto agonista (flare). Administrados crónicamente: castración química. Son decapéptidos semejantes a la molécula original de GnRH pero con dos aminoácidos cambiados. Goselerin, Leuprolin, Buselerin, Triptolerin.
]]> 5) Progestágenos: Acetato de megestrol y acetato de medroxiprogesterona:
Acción antiestrogénica y antiandrogénica. Actúan sobre receptores de PR, que regula la activación del receptor de estrógenos frenándolo, e inhibe el TGF alfa y la IGF I-II. Suprimen parcialmente la secreción GnRH. Induce la creación de receptores de estrógenos anómalos.
Embarazo y cáncer de mama
Embarazo después del diagnóstico de cáncer de mama: no parece influir negativamente en su evolución.
Cáncer in situ de mama
Ensayo NSABP B244: se recomienda tamoxifeno si RE+ y tumor con riesgo intermedio o alto de recidiva.
Tratamiento hormonal primario, exclusivo, en cáncer de mama invasivo
Ensayo NSABP B215: tratamiento hormonal primario, sin RT (T1<= 1cm, N0 M0), sólo se recomienda en el contexto de ensayos clínicos, ya que el porcentaje de recidivas es alto.
Tratamiento neoadyuvante en cáncer de mama avanzado
Tamoxifeno en cáncer de mama avanzado, como tratamiento neoadyuvante, con 80% de respuestas en pacientes ER+.
]]> Quimioprevención:NSABP P-16: compara tamoxifen y placebo, beneficio pero efectos secundarios que deben ser advertidos (aumento al doble de incidencia de cáncer de endometrio, sofocos, tromboembolismo). Tras una mediana de 54 meses se mostró una reducción en el 49% de incidencia de cáncer invasivo, aunque no influyó sobre la aparición de tumores hormonorresistentes. También redujo la incidencia de cáncer lobulillar infiltrante.
El ensayo del Royal Marsden10, resultó negativo para la prevención con tamoxifeno.
Están en marcha el estudio Internacional Breast Cancer Interventio (IBIS) (en Europa y Australia), con tamoxifeno; y el estudio NSABP P-2, con tamoxifeno y raloxifeno (STAR)10que aleatorizará a 22.000 mujeres con riesgo aumentado de padecer cáncer de mama a recibir 5 años de tamoxifen o raloxifeno. Se basó en los resultados obtenidos con el ensayo MORE (Multiple Outcome of Raloxifene Evaluation)10, en el que participaban mujeres con cáncer de mama osteoporóticas con el objetivo de reducir las fracturas patológicas, en las que se detectó además una reducción de la incidencia de cáncer de mama (76% reducción frente a placebo. El estudio realizado con toremifeno no se ha asociado a aumento de cáncer de endometrio7.
Revisión de la literatura
Conclusiones del metaanálisis (EBCCG. 2000)8
La actualización del metaanálisis mundial de Tratamientos Adyuvantes del Cáncer de Mama Inicial, en septiembre del 2000 ha proporcionado varias conclusiones:
Evidencia de beneficio terapéutico de la QT, tamoxifeno, ablación ovárica y la RT, aunque la homogenización intrínseca al propio proceso limita la capacidad de estimación de la magnitud del beneficio de tratamientos concretos en grupos de pacientes definidos. Está claro que la magnitud del beneficio del tamoxifeno es máxima en pacientes con tumores que expresan receptores hormonales positivos que reciben 5 años de hormonoterapia.
En los estudios en marcha aTTOm (adjuvant Tamoxifen Treatment offer more?) y ATLAS (Adjuvant Tamoxifen-Longer Against Shorter) se definirá esta cuestión, aunque un estudio, realizado en Escocia (Scottish Adjuvant Tamoxifen Trial), demuestra ausencia de beneficio en prolongar más de 5 años el tratamiento. El estudio NSABP-14 plantea la ausencia de beneficio hasta 7 años de tratamiento y plantea el incremento de 2-3 veces la tasa de cáncer de endometrio en estas pacientes que reciben tamoxifen. Pendiente de evaluar la misma cuestión en pacientes en las que el tratamiento de elección es la QT±hormonoterapia.*
]]> Respecto al tratamiento adyuvante y los aspectos psicológicos, las mujeres aceptarían tratamiento con QT si se espera un modesto beneficio, pero exigen mayor beneficio a la hora de aceptar el tratamiento adyuvante endocrino por la toxicidad esperable.
I) Tamoxifeno
Early Breast Cancer Trialist's Collaborative Group. From The Cochrane Library, Issue 1, 2003. Oxford. Tamoxifen for early breast cancer (Cochrane Review)9.
Conclusión de los revisores:
En mujeres con tumor con RE-negativos, el uso del tamoxifen permanece como investigacional. Tratamiento con tamoxifen mejora sustancialmente la supervivencia a 10 años en mujeres con ER-positivos o desconocidos, reduciendo además las posibilidades de recurrencia. Este efecto parece ser independiente de las otras características clínicas de la paciente o el tratamiento.
Beneficios
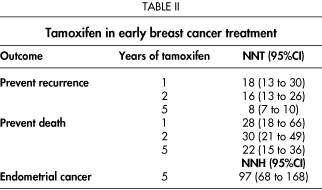
En mujeres tratadas con tamoxifen durante 1, 2 o 5 años, la reducción en la tasa de recidiva durante los 10 años siguientes es de 21, 29 y 47% respectivamente, la reducción en la aparición de tumor contralateral del 13,26 y 47% y la reducción en la mortalidad del 12, 17 y 26%. Se exponen los NNT calculados, en la Tabla II. Por cada 8 mujeres a las que se les da tamoxifen por 5 años, se previene la recidiva en una (NNT de 8).
]]>

Riesgos
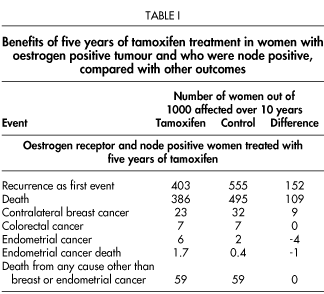
La incidencia de cáncer endometrial es mayor con tamoxifen, aproximadamente, en números absolutos, la mitad de los cánceres de mama evitados. El NNT para producir un cáncer endometrial, en pacientes tratadas durante 5 años es de 97. Hay un 45% de reducción de cáncer de mama, entre 239 casos, pero había más casos de cáncer endometrial, de embolismo pulmonar y de trombosis venosa profunda, pero no aumento de coronariopatía.
II) Bases racionales para el uso de inhibidores de la aromatasa en el tratamiento de primera línea en el cáncer de mama
]]> Beneficio sobre el tamoxifenTiempo medio hasta progresión mayor que con tamoxifen.
Reducción en la incidencia de accidentes tromboembólicos.
No es probable que produzca estimulación del crecimiento tumoral en pacientes resistentes al tamoxifeno. Es improbable que ejerza efecto proliferativo sobre el endometrio
Eficacia probada como segunda línea de tratamiento.
Bien tolerado, dosificación cómoda (una vez al día).
Recomendaciones
No se deben usar en mujeres premenopáusicas.
Tratamiento de primera línea:
• Los IA selectivos, son modestamente superiores al tamoxifen (en términos de respuestas objetivas y tiempo hasta la progresión) como tratamiento de primera línea en mujeres postmenopáusicas con estadio IV. ]]>
• El tamoxifen permanece como una alternativa idónea.• No hay datos para poder recomendar un IA sobre otro.
Tratamiento de segunda línea:
• Los IA son superiores al acetato de megestrol o la aminoglutetimida como segunda línea. No hay datos para poder recomendar un IA sobre otro.
Tratamiento de tercera línea:
• En mujeres con cáncer avanzado de mama que han sido tratadas con agentes hormonales y QT, el tratamiento con examestano es una opción recomendada.
III) Ablación ovárica
Ovarian ablation for early breast cancer (Cochrane Review)10
Resultados principales: se han descrito 1.130 mujeres y 153 recurrencias entre 2.102 mujeres de edad debajo de los 50 años cuando se randomizaron, la mayoría premenopáusicas al diagnóstico. La supervivencia a los 15 años era mejor en el grupo con ablación ovárica (52,4 vs 46,1%, 6,3 menos muertes por100 mujeres, p=0.001), así como la supervivencia libre de recurrencia (45 vs 39 %, p= 0.007).
]]> Conclusiones de los revisores: en mujeres de edad por debajo de 50 años, la ablación ovárica mejora la supervivencia, al menos en ausencia de quimioterapia. Son necesarios nuevos estudios para evaluar la relevancia de la ablación ovárica junto a otros tratamientos adyuvantes.
Resumen de los principales ensayos clínicos
I) Cáncer de mama localmente avanzado o metastático
Ensayos 0027 y 0030 con anastrozol en primera línea frente a tamoxifen en cáncer de mama avanzado o metastático, demuestra beneficio del anastrozol en el tiempo hasta la progresión en tumores hormonodependientes12, 13.
Postmenopáusica IIIB o E IV. Letrozol en primera línea. Ensayo 02514. En conjunto, letrozol era superior al tamoxifen en cuanto al tiempo hasta la progresión, respuestas objetivas y beneficio clínico.
II) Cáncer de mama precoz
Ensayo ATAC: (Arimidex, Tamoxifen, Aloneorin Combination)15.
Tratamiento en mujeres postmenopáusicas con cáncer de mama invasivo, se sometían a cirugía±RT±QT y posteriormente se randomizaban , con esquema 1:1:1, a tratamiento con : Anastrozol 1 mg/d+tamoxifeno placebo, Anastrozol placebo+tamoxifeno 20 mg/d o Anastrozol 1 mg/d+ Tamoxifeno 20 mg/d. La duración prevista del tratamiento, era de 5 años.
En el análisis actualizado en diciembre de 2002 (25 Conferencia de San Antonio) incluía 1.373 eventos, con 991 eventos en población con R Hormonales positivos y una mediana de seguimiento de 47 meses. En el análisis de supervivencia libre de enfermedad, en la población con receptores de estrógenos positivos, (incluyendo tiempo transcurrido hasta la primera recidiva local o a distancia, nuevo tumor de mama primario (contralateral) o muerte por cualquier causa), mostró a los 48 meses de seguimiento, una OR de 0.82, con IC de 0.70-0.96 y p de 0.014 entre AN frente a TAM (valores 88% frente a 85,1%). La diferencia absoluta ha sido de 2,9% (frente a 1,7% a los 36 meses). La probabilidad de recurrencia en la población con receptores de estrógenos positivos ha sido de OR de 0.78 (IC de 0.65-0.93) y p de 0.007 (11% frente a 8,4%), con una diferencia absoluta de 2,6%.
]]>
La incidencia de efectos secundarios beneficia al uso del anastrozol. Además no había beneficio de asociar Tamoxifen y anastrozol, frente a su administración individual.
En la actualización a los 54 meses16, la supervivencia libre de enfermedad en la población global es de 86,9% frente a 84,5%, mostrando una OR de 0,86 (IC 0,76-0,99) (p=0,03) con diferencia absoluta de 2,4%. La supervivencia libre de enfermedad en la población con receptores hormonales positivos, la OR es de 0,82 (IC 0,70-0,96) (p=0,014). La probabilidad de recurrencia en la población global muestra una OR de 0,83 (IC 0,71-0,96) (p=0,015) con una diferencia absoluta del 2,3%. En la población receptor estrógeno positivo, la probabilidad de recurrencia muestra una OR de 0,78 (IC 0,65-0,93) (p=0,007) con una diferencia absoluta del 2,6%.
En definitiva se mantienen las ventajas en eficacia, las diferencias absolutas se incrementan con el tiempo. El perfil de toxicidad sigue igual.
III) Ablación ovárica en premenopáusicas: cáncer avanzado
Los resultados presentados por Taylor y cols17 y por Boccado y cols18, muestran que Zoladex a dosis de 3,6 mg. es una alternativa a la ooforectomía en el cáncer de mama avanzado en mujeres premenopáusicas con RE-positivos o desconocidos.
El metaanálisis de la EORTC19, concluye que la combinación de LHRH agonistas+tamoxifen es superior a los agonistas aislados (2,9 años frente a 2,5 en supervivencia global y RO del 39% frente al 30%).
Estudio ZEBRA = zoladex 3.6 mg Early Breast Cancer Research Association 20
]]> Incluía a 1.640 pacientes de 102 centros, con 74% de las pacientes RE+. Se comparó zoladex durante 2 años, frente a CMF 6 ciclos. Las conclusiones de este estudio fueron:En pacientes con RE+, zoladex era equivalente a CMF en la supervivencia libre de enfermedad (SLE).
Zoladex era más efectivo en inducir amenorrea que el CMF y la inducción de amenorrea siguiendo a la QT se asociaba con mejor pronóstico en la SLE. La amenorrea inducida por zoladex era reversible, pero no así la de la QT. No hubo diferencias en la pérdida de densidad ósea entre los 2 grupos a los 3 años.
En la actualización del ensayo a 7,3 años, zoladex no es inferior a CMF en pacientes con receptores de estrógenos, no así en los pacientes con receptores de estrógenos negativos.
Ensayo IBCSG VIII 21, las pacientes sometidas a cirugía son randomizadas 1:1:1 a zoladex, 3,6 mg cada 28 días durante 2 años, frente a CMF x 6 ciclos, y frente a CMF x 6 ciclos seguido por zoladex 3,6 mg cada 28 días durante 18 meses, mostrando a los 5 años de seguimiento una eficacia similar con zoladex frente a CMF en mujeres per/perimenopausicas receptores de estrógenos positivos y ganglios negativos, con supervivencia libre de enfermedad del 81% en ambos brazos.
El ensayo GROCTA 0222 (Italian Adyuvant Breast Cancer Trial) , comparando zoladex 2 años+tamoxifen 5 años, frente a CMF x 6 meses, confirma la eficacia de este régimen en premenopausicas con tumores RE+. En la actualización del ensayo con una mediana de seguimiento de 7,5 años, se confirman los resultados.
El ensayo austriaco, ABCSG AC05 (Mustian Adyuvant Breast Cancer trial), de igual diseño pero administrando zoladex 3 años+tamoxifeno durante 5 años, frente a CMF x 6 ciclos, muestra beneficio de zoladex+tamoxifeno frente a CMF en la supervivencia libre de recidiva local y a distancia en pacientes premenopausicas con tumor hormonosensible.
El estudio GROCTA 4B23, consistente en cirugía±RT±QT, seguido de tamoxifen 2-3 años, randomizado a tamoxifen 2-3 años frente a anastrozol 2-3 años. El número de pacientes incluidos ha sido de 448, con un seguimiento medio de 36 meses, recaída locorregional 13% en brazo tamoxifen frente a 2% en anastrozol, metástasis a distancia 19% frente a 10% y aparición de segundo primario, 10% frente a 5%. En la actualización del estudio presentada en la reunión de San Antonio 2003, la supervivencia global actuarial a 5,5 años es de 99,2% frente a 96,4% en el grupo de anastrozol y tamoxifen respectivamente (p=0,1). La supervivencia libre de recaída es de 94,3% y 99% (p= 0,003) en el grupo de tamoxifen y de anastrozol respectivamente. Las conclusiones de este estudio es que el tratamiento con anastrozol es superior a tamoxifen en la supervivencia libre de recaída, y mejor perfil de toxicidad.
El ensayo ZIPP24 (zoladex enpacientes premenopáusicas), análisis combinado, comparando zoladex 2 o más años, tamoxifen 2 o más años, zoladex+tamoxifen 2 o más años y no tratamiento, adyuvante al tratamiento estándar (que podía incluir RT± QT±tamoxifen), mostró que el añadir zoladex al tratamiento estándar producía aumento de la supervivencia libre de enfermedad y global en el cáncer precoz de mama. El tratamiento era más efectivo en el subgrupo de pacientes con RE+ que no recibían QT. Tambien beneficiaba a las que habían recibido anterioriormente QT o tamoxifen, aunque en menor medida. Había menor incidencia de cáncer de mama contralateral.
El ensayo FASG 0625 (French adyuvant Breast Cancer Trial), compara LHRHa (triptolerina)+tamoxifen versus QT con antraciclina (FEC 50 x 6), en mujeres premenopáusicas con RE+, ganglios positivos (1-3) en cáncer de mama precoz. Después de 54 meses de seguimiento, el número de eventos es muy bajo, mostrando buena supervivencia libre de enfermedad, con ambos tratamientos (97 y 92,9% supervivencia global con ablación ovárica frente a QT).
]]> En mujeres menores de 35 años, es fundamental conseguir que queden en amenorrea por QT, debiéndose añadir ablación ovárica si ésta no se produce (23% supervivencia libre de enfermedad, frente a 38% en no amenoreicas)26.Mam-1 GOCSI Trial (GOCSI-Gruppo Oncologico Centro-Sud-Isole)27.
Los resultados de este ensayo, en pacientes premenopáusicas con ganglios positivos, añadiendo secuencialmente tratamiento hormonal al tratamiento con QT (CMF y/o adriamicina), demuestran beneficio de añadir zoladex + tamoxifen a la QT en cuanto a supervivencia libre de progresión.
Como resumen, a modo de conclusiones expondremos los algoritmos de tratamiento recomendados hay día en el cáncer de mama, definidos en la literatura consultada y en la Conferencia de Consenso de St Gallen (a la fecha de remisión de este manuscrito no estaban publicado las conclusiones de la VIII Reunión de St Gallen, de marzo del 2003 y en las que el punto clave es el nuevo papel de los inhibidores de la aromatasa (anastrozol) y del marcador Cerb-2, a la hora de condicionar el tratamiento con QT y/o hormonoterapia.
]]> tabla 3
Propuesta de tratamiento
La tasa de respuesta de las maniobras hormonales, secuenciales, en mujeres con cáncer de mama metastático van disminuyendo desde el 65% en la primera, 43% en la segunda, 30% en la tercera, 16% en la cuarta y ausencia de repuesta en la quinta maniobra.
Se iniciará tratamiento hormonal en la recidiva sistémica en los casos de:
RE+/RP+ o enfermedad sólo en hueso/tejido blando o enfermedad asintomático visceral.
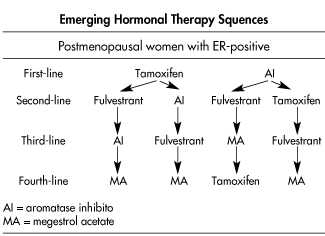
En dichos casos se administrará tamoxifeno (T) si no se usó en el año anterior o hace más de una año desde que se suspendió su uso. Si se usó el año anterior, se debe pasar a un inhibidor de la aromatasa (IA). Hoy día, a la luz de los ensayos randomizados disponibles, se puede recomendar iniciar el tratamiento en postmenopáusicas, con IA y secuencialmente con tamoxifeno. Si responde, se puede ir combinando hormonoterapia de 3a y 4a línea, tal como exponemos a continuación.
La secuencia recomendada en cáncer de mama metastásico es (Buzdar y cols.)28.
Estrategia de tratamiento endocrino para pacientes jóvenes: (resumen St Gallen 2001) 29
La QT sola es insuficiente para las pacientes jóvenes que tienen receptores hormonales positivos, posiblemente porque la QT no inhibe eficazmente la función ovárica en estas edades. El tratamiento endocrino, incluyendo la supresión ovárica con un análogo de LHRH y tamoxifeno, es como mínimo igual que la QT citotóxica convencional, según el resultado de varios ensayos clínicos aleatorizados realizados en premenopáusicas).
]]> En la enfermedad avanzada, la combinación de un análogo GHRH y tamoxifeno produce un control de la enfermedad mejor que el de cualquiera de estos tratamientos por sí solo. En un contexto adyuvante, no se ha demostrado ningún beneficio con la adición de QT a un tratamiento endocrino combinado (ablación/supresión ovárica más tamoxifeno) en un pequeño ensayo realizado en mujeres premenopáusicas con tumores con receptores positivos.Esta observación no implica que la QT deba evitarse en las pacientes premenopáusicas con tumores que expresan receptores de estrógenos y/o progesterona, sino más bien que serán necesarias nuevas investigaciones para definir el papel de la supresión de la función ovárica junto con el tamoxifeno tras el uso de la QT para la enfermedad sensible al tratamiento endocrino.
El tratamiento endocrino (tamoxifeno) no está indicado en pacientes con receptores hormonales negativos y puede, en realidad, ser nocivo si se administra concomitante con QT a estas pacientes. Se presentará las conclusiones de la VIII reunión de St Gallen 2003, en el que toma relevancia el papel del tratamiento con anastrozol como adyuvante en cáncer de mama precoz hormonosensible, principalmente si son pacientes con antecedentes tromboembólicos o si contraindicación o no tolerancia al tamoxifen y como primera línea de tratamiento en cáncer metastásico, aparte de ser una segunda línea de tratamiento eficaz, después del tamoxifeno30.
Bibliografía
1. Avery´s: Cap. 27. Malignanat diseases. Pag:1254-94. Drug Treatment. 4ª Edition. ADIS Press. 1997.
2. Herfindal & Gourdey. Textbook of therapeutics. 7ª edition. Lippincott & Williams. 2000; Cap. 88: Breast cancer. Pag.1769-86. [ Links ]
3. Coia L, Wagman L. Cap. Breast cancer. Formato electrónico. © 2000 by PRR, Inc. http://www.cancernetwork.com/framesets/default.htm [ Links ]
4. Fisher B, Dignam J, Wolmarrk y cols. Tamoxifen in treatment of intraductal breast cancer: National Surgical Adjuvant Breast and Bowel projet B-24 randomised controlled trial. Lancet 1999; 353;1993-2000. [ Links ]
5. Fisher B, Bryant J, Dignam J y cols. Tamoxifen, radiation therapy, or both for prevention of ipsilateral breast tumor recurrence after lumpectomy in women with invasive breast cancer of one centimeter or less. JCO 2002; 20:4141-9. [ Links ]
6. Fisher B, Costantino JP, Wickerham DL y cols. Tamoxifen for prevention of breast cancer: Report of the National Surgical Adjuvant Breast and Bowel projet P-1 study. J Natl Cancer Inst. 1998; 90:1371-88. [ Links ]
7. Wickerham L, Tan-Chiu E. Quimioprevención del cáncer de mama: estado actual e indicaciones futuras. Semen Oncol 2002; 1(1)35-41. [ Links ]
8. Early Breast Cancer Trialist Collaborative Group: Favourable and unfavourable effects on long-term survival of radiotherapy for early breast cancer: An overview of the randomised trials. Lancet 2000; 355:1757-70. [ Links ]
9. Early Breast Cancer Trialists' Collaborative Group. From The Cochrane Library, Issue 1, 2003. Oxford. Tamoxifen for early breast cancer (Cochrane Review). [ Links ]
10. Ovarian ablation for early breast cancer (Cochrane Review). Early Breast Cancer Trialists' Collaborative Group From The Cochrane Library, Issue 1, 2003. Oxford: Update Software Ltd. [ Links ]
11. Eisen A, Pritchard K, Johnston M, Oliver T, and the Breast Cancer Disease Site Group. The Role of Aromatase Inhibitors in the Treatment of Postmenopausal Women with Metastatic Breast Cancer (Practice Guideline Report No. 1-5). September 2002. [ Links ]
12. Bonneterre J, et al. J Clin Oncol 2000; 18:3748-57. [ Links ]
13. Nabholtz JM, et al. J Clin Oncol 2000; 18:3758-67. [ Links ]
14. Mouridsen H, et al. J Clin Oncol 2001; 19:2596-606. [ Links ]
15. Anastrozol alone or in combination with tamoxifen versus tamoxifen alone for adjuvant treatment of postmenopausal women with early breast cancer: first result of the ATAC randomised trial. Lancet 2002; 359:2131-9. [ Links ]
16. Anastrozol alone or in combination with tamoxifen versus tamoxifen alone for adjuvant treatment of postmenopausal women with early breast cancer. Result of the ATAC (Arimidex, Tamoxifen Alone or in Combination) trial efficacy and safety update analyses. Cancer 2003; 98:1802-10. [ Links ]
17. Taylor CW et al. J Clin Oncol 1998; 16:994-9. [ Links ]
18. Boccardo F et al. Ann Oncol 1994; 5:337-42. [ Links ]
19. Klijn JGM et al. J Clin Oncol 2001; 19:343-53 [ Links ]
20. Kaufmann M. Breast 2001; 10 (Suppl 1):S30, Abstr P53. [ Links ]
21. Castiglione-Gertsch et al. Proc ASCO 2002; 21:38a. Abstr.149. [ Links ]
22. Boccardo F, Rubagotti A, Amoroso D, et al. J Clin Oncol 2000; 18:2718-27. [ Links ]
23. Boccardo et al. JCO 2001;19(22):4209-15. [ Links ]
24. Baum M et al. Breast 2001; 10(Suppl 1):S32-3,Abstr P64. [ Links ]
25. Roche HH et al. Proc ASCO 2000; 19:72a,Abstr 279. [ Links ]
26. Aebi S et al. Lancet 2000; 355:1869-74. [ Links ]
27. Bianco AR et al. Proc ASCO 2001; 20:27a, Abstr 104. [ Links ]
28. Seminars in Oncology, 2002: (1)61-73 (edición española).
29. Goldhirsch A, Glick J, Gelber R y cols. Informe de congreso: Panel de consenso internacional sobre el tratamiento del cáncer de mama primario. J Clin Oncol.2001;19(18): 3817-27. [ Links ]
30. Aron Goldhirsch, William C. Wood, Richard D. Gelber, Alan S. Coates, Beat Thurlimann, and Hans-Jorg Senn. Meeting Highlights: Updated International Expert Consensus on the Primary Therapy of Early Breast Cancer. J Clin Oncol 2003; 21:3357-65. [ Links ] ]]>