600 UI/l en 3 pacientes del grupo de estudio y 10 del control (p = 0,001). Se detectó pancreatitis leve en 5,3% de los pacientes del grupo de estudio y 16% del control (p < 0,05). No hubo mortalidad ni eventos adversos. Conclusiones: indometacina rectal previo a CPRE disminuye el riesgo de hiperamilasemia y pancreatitis. La indometacina es accesible, de bajo costo con mínimos o nulos efectos secundarios.]]>
600 IU/L was found in 3 patients in the study group, and in 10 in the control group (p = 0.001). Mild pancreatitis was detected in 4 (5.3%) patients in the study group, and in 12 (16%) patients in the control group (p = 0.034). There were no deaths or adverse drug reactions. Conclusions: rectal indomethacin before ERCP decreases the risk of hyperamylasemia and pancreatitis. Indomethacine is a feasible, low-cost drug with minimal or nil side effects.]]>
Efecto de la administración de indometacina rectal sobre los niveles séricos de amilasa posteriores a colangiopancreatografía retrógrada endoscópica y su impacto en la aparición de episodios de pancreatitis secundaria
Effect of the rectal administration of indomethacin on amylase serum levels after endoscopic retrograde cholangiopancreatography, and its impact on the development of secondary pancreatitis episodes
A. Montaño Loza, X. Rodríguez Lomelí, J. E. García Correa, C. Dávalos Cobián, G. Cervantes Guevara1, F. Medrano Muñoz2, C. Fuentes Orozco2 y A. González Ojeda2
Departamentos de Gastroenterología y Endoscopia. UMAE. Hospital de Especialidades. CMNO-IMSS.
1Departamento de Endoscopia. Hospital Civil "Fray Antonio Alcalde". Universidad de Guadalajara. México.
2Unidad de Investigación en Epidemiología Clínica. UMAE. Hospital de Especialidades. CMNO, IMSS. Guadalajara. Jalisco, México
RESUMEN
Introducción: hiperamilasemia y pancreatitis aguda representan las complicaciones mayores más frecuentes posteriores a colangiopancreatografía retrógrada endoscópica (CPRE), apareciendo en 1-30% de los casos.
Objetivo: determinar la incidencia de hiperamilasemia y pancreatitis posterior a CPRE y evaluar la utilidad de indometacina rectal para la prevención de estos.
Material y métodos: ensayo clínico controlado. Durante un periodo de 12 meses se incluyeron 150 pacientes. Estos fueron divididos en grupo de estudio (n = 75), a quienes se administró indometacina rectal 100 mg 2 horas previas al procedimiento, y control (n = 75) que recibió glicerina. Dos horas posteriores a la CPRE se determinó el nivel de amilasa sérica y se clasificaron en: 0 ≤ 150 UI/l, 1 = 151-599 UI/l, 2 ≥ 600 UI/l. Los episodios de pancreatitis clínica se cuantificaron y clasificaron de acuerdo a los criterios de Ranson.
Resultados: distribución por género: 100 mujeres y 50 hombres. Edad media: 55,37 ± 18,0 para el grupo de estudio y 51,1 ± 17,0 para el control. El diagnóstico de patología benigna se presentó en 56 (74,7%) casos del grupo de estudio y 59 (78,7%) del control. Posterior al procedimiento, 13 (17,3%) pacientes del grupo experimental y 28 (37,3%) del control desarrollaron hiperamilasemia (p < 0,05). Se encontró hiperamilasemia > 600 UI/l en 3 pacientes del grupo de estudio y 10 del control (p = 0,001). Se detectó pancreatitis leve en 5,3% de los pacientes del grupo de estudio y 16% del control (p < 0,05). No hubo mortalidad ni eventos adversos.
Conclusiones: indometacina rectal previo a CPRE disminuye el riesgo de hiperamilasemia y pancreatitis. La indometacina es accesible, de bajo costo con mínimos o nulos efectos secundarios.
Palabras clave: Colangiopancreatografía retrógrada endoscópica (CPRE). Hiperamilasemia. Pancreatitis aguda. Indometacina.
Background: hyperamylasemia and acute pancreatitis represent the most frequent major complication after endoscopic retrograde cholangiopancreatography (ERCP), developing in 1-30% of cases.
Objective: to determine the incidence of hyperamylasemia and acute pancreatitis after ERCP, and to assess the utility of rectal indomethacin to prevent these events.
Material and methods: a randomized clinical trial. During a 12-month period 150 patients were included. They were divided up into a study group (n = 75), where 100 mg of rectal indomethacin were administered 2 hours prior to the procedure, and a control group (n = 75), which received rectal glycerin. Two hours after ERCP serum amylase levels were measured and classified as follows: 0 ≤ 150 IU/L, 1 = 151-599 IU/L, 2 ≥ 600 IU/L. Clinical pancreatitis episodes were quantified and classified according to Ranson's criteria.
Results: gender distribution: 100 women and 50 men. Mean age: 55.37 ± 18.0 for the study group, and 51.1 ± 17.0 for the control group. A diagnosis of benign pathology was present in 56 (74.7%) cases in the study group, and 59 (78.7%) controls. After ERCP 13 (17.3%) patients in the study group and 28 (37.3%) in the control group developed hyperamylasemia (p ≤ 0.05). Hyperamylasemia > 600 IU/L was found in 3 patients in the study group, and in 10 in the control group (p = 0.001). Mild pancreatitis was detected in 4 (5.3%) patients in the study group, and in 12 (16%) patients in the control group (p = 0.034). There were no deaths or adverse drug reactions.
Conclusions: rectal indomethacin before ERCP decreases the risk of hyperamylasemia and pancreatitis. Indomethacine is a feasible, low-cost drug with minimal or nil side effects.
Key words: Endoscopic retrograde cholangiopancreatography. Hyperamylasemia. Acute pancreatitis. Indomethacin.
]]> Introducción
La hiperamilasemia y pancreatitis son eventos frecuentes posteriores a colangiopancreatografía retrógrada endoscópica (CPRE), ocurriendo del 1 al 30% de los pacientes (1-5). La incidencia de pancreatitis posterior a CPRE varía de acuerdo a las indicaciones del procedimiento y la intervención realizada. La mortalidad oscila entre el 0,2 al 0,6% (6-8). Los factores de riesgo para pancreatitis post-CPRE incluye antecedente de pancreatitis (9), canulación difícil (7), inyección repetida del conducto pancreático (9), opacificación acinar pancreática (10), hipertensión del esfínter de Oddi (8,11), precorte y esfinterotomía (3,8,9).
La patogénesis de la pancreatitis post-CPRE no está clara. Al parecer la instrumentación u opacificación del conducto pancreático tienen un papel fundamental en el desarrollo de la respuesta inflamatoria (11). Los eventos intracelulares iniciales provocan daño acinar pancreático seguido de respuesta inflamatoria local liberando citocinas proinflamatorias a la circulación (12). La severidad del ataque se determina por la magnitud de la respuesta inflamatoria sistémica resultante (13).
Debido a que el evento inicial está bien identificado, hace de la pancreatitis aguda post-CPRE un modelo único de estudio para valorar el beneficio de la inmunomodulación temprana (11-15).
Los resultados de varios estudios controlados donde se han utilizado agentes profilácticos como glucagón (16), calcitonina (17), nifedipina (18), octreótide (19) y corticosteroides (20) han sido poco alentadores. Aunque los ensayos iniciales fallaron en mostrar reducción de la incidencia de pancreatitis post-CPRE, estudios recientes han detectado un efecto benéfico preventivo (21). Se considera que la fosfolipasa A2 (FLA2) juega un papel importante en la cascada inflamatoria inicial de pancreatitis aguda mediante la regulación de proinflamatorios, incluyendo prostaglandinas, leucotrienos y factor activador de plaquetas (22). La inhibición de FLA2 ha sido objetivo de varios agentes terapéuticos usados para tratar pancreatitis aguda no inducida por CPRE con resultados alentadores. Se ha demostrado que los antiinflamatorios no esteroideos (AINE) son potentes inhibidores de FLA2 en suero de pacientes con pancreatitis aguda (23), y también han demostrado efectos benéficos en modelos experimentales de pancreatitis en ratón (24).
El objetivo de este trabajo fue determinar el efecto de la indometacina aplicada vía rectal sobre los niveles de amilasa y cuadros de pancreatitis posteriores a CPRE.
Material y métodos
Ensayo clínico controlado con evaluación ciego simple de pacientes con indicación para realizar CPRE realizado en un periodo de 12 meses (junio 2004 a mayo 2005) en el Departamento de Endoscopia de la Unidad Médica de Alta Especialidad, Hospital de Especialidades del Centro Médico Nacional de Occidente del IMSS y el Departamento de Endoscopia del Hospital Civil "Fray Antonio Alcalde" de la Universidad de Guadalajara. Se incluyeron 150 pacientes sujetos a CPRE de un universo total de 250 candidatos bajo las siguientes condiciones:
-Pacientes mayores de 18 años con indicación para realizar CPRE por sospecha de obstrucción de la vía biliar, que aceptaran participar en el estudio previa firma de consentimiento informado.
]]> -No se incluyeron pacientes con pancreatitis aguda clínicamente evidente o hiperamilasemia ≥ 150 U/l antes del procedimiento ni aquellos con ingesta previa de AINE una semana antes del procedimiento.-Pacientes bajo tratamiento anticoagulante o antiagregante plaquetario como ácido acetilsalicílico y placitaxel o con un tiempo de protrombina con una diferencia > 5 segundos contra el testigo tomado en un periodo no mayor de 72 horas antes del estudio.
-Pacientes con alergia o hipersensibilidad a indometacina o material de contraste hidrosoluble ni aquellos con hemorragia activa de origen péptico o con incapacidad para adoptar el decúbito ventral para el procedimiento endoscópico.
Se estimó reducir con la maniobra de intervención un 15% los eventos de hiperamilasemia y/o pancreatitis aguda post-CPRE, por lo que se estimó un total de 150 casos (25), y fueron asignados al azar en grupo de estudio (n = 75) al que se le administró indometacina 100 mg vía rectal 2 horas antes del procedimiento y grupo control (n = 75) quienes recibieron supositorios de glicerina de 2 gramos.
A todos los pacientes se realizó determinación de amilasa sérica antes del procedimiento y dos horas posteriores, clasificándose de manera ordinal en: grado 0 ≤ 150 ui/l, grado 1: 151-599 UI/l y grado 2: > 600 UI/l.
Todo valor de amilasa ≤ 150 UI/l se consideró normal. Si la determinación de amilasa sérica fue > 150 y < 600 UI/l y no hubo evidencia clínica de pancreatitis aguda, los pacientes fueron dados de alta o si estaban hospitalizados se inició dieta líquida. Si el nivel de amilasa fue tres veces por arriba de su valor normal y el paciente presentó dolor epigástrico o en todo el abdomen con irradiación a espalda asociado a náusea o vómito, se estableció el diagnóstico de pancreatitis aguda post-CPRE, en ausencia de evidencia radiológica de neumoperitoneo o enfisema en el espacio retroperitoneal. Estos casos se manejaron con hospitalización, ayuno, hidratación con soluciones cristaloides y analgesia. Los episodios de pancreatitis se clasificaron de acuerdo a criterios pronósticos de Ranson (26).
Se registraron los detalles del estudio endoscópico especificando dificultad para la canulación, número de inyecciones al conducto pancreático, realización de esfinterotomía, características del conducto y vía biliar, presencia de coledocolitiasis, asimismo se definió si el procedimiento fue únicamente diagnóstico o terapéutico (colocación de endoprótesis). Previamente los autores informaron los resultados preliminares de este protocolo con un 80% de los casos evaluados y publicados en la Revista de Gastroenterología de México a finales del año 2006 (27).
Análisis estadístico
Los resultados se presentan con promedios, porcentajes y medias con desviación estándar. La inferencia estadística se hizo a través de la prueba de Chi cuadrado o exacta de Fisher para variables cualitativas, para las cuantitativas se empleó prueba T de Student. A fin de explorar el comportamiento de los factores de riesgo se calcularon los riesgos relativos e intervalos de confianza al 95%. Todo valor de p < 0,05 se consideró estadísticamente significativo. Finalmente se analizó la reducción del riesgo absoluto (RRA), reducción del riesgo relativo (RRR) y número necesario a tratar (NNT) a fin de prevenir un episodio de pancreatitis.
Consideraciones éticas
]]> El protocolo de investigación fue revisado y aprobado por los Comités de Investigación y Ética de las Instituciones participantes. Todos los pacientes firmaron su consentimiento para participar en el estudio. El proyecto fue financiado con recursos propios de ambas instituciones.
Resultados
La distribución por género fue 50 hombres (33,3%) y 100 mujeres (66,7%), relación 2:1 (p = 0,863). La distribución en el grupo de estudio fue de 26 hombres y 49 mujeres; grupo control 24 hombres y 51 mujeres sin diferencia significativa (p = 0,86). El promedio de edad para el grupo de estudio fue 55,37 ± 18,0 años y para el control 51,12 ± 17 (p = 0,985).
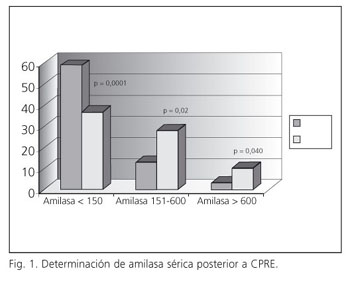
El diagnóstico de etiología benigna para ambos grupos correspondió a 115 (76,6%), de los cuales 56 fueron del grupo de estudio y 59 del control. La etiología maligna correspondió a 35 casos (23,3%) para ambos grupos, 19 del grupo de estudio y 16 del control. Los diagnósticos encontrados están descritos en la tabla I.
En la tabla II se anotan los factores de riesgo presentes al momento del procedimiento endoscópico. No se encontró diferencia significativa al análisis estadístico. El nivel basal de amilasa en el grupo de estudio fue 53,56 ± 22 UI/l y de 56,56 ± 22,8 UI/l en el control (p = 0,38). Los niveles alcanzados a las dos horas fueron de 148,22 ± 190,6 UI/l en el grupo de estudio y de 240,73 ± 256,2 UI/l en el control (p = 0,013).
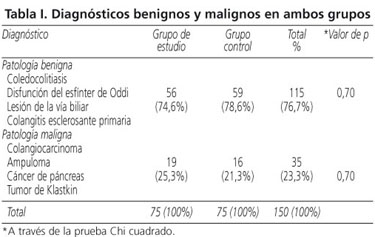
Un total de 41 pacientes presentaron hiperamilasemia (151 a 599 U/L), 13 (17,3%) del grupo de estudio y 28 (37,3%) del control (p = 0,02). Con valores mayores de 600 unidades se observaron 13 pacientes correspondiendo 3 al grupo de estudio (4%) y 10 (13,3%) al grupo control (p = 0,04) (Fig. 1). Desarrollaron pancreatitis aguda 16 pacientes (10,7%) que correspondieron 4 del grupo de estudio y 12 del control (p = 0,034). Una paciente del primer grupo y dos casos del segundo con pancreatitis tuvieron un nivel de amilasa a las dos horas justamente por debajo de las 600 U/l. A las 24 horas del procedimiento el promedio del nivel de amilasa sérica fue de 1342,20 ± 345,3 U/l. Estos casos se catalogaron de acuerdo a los criterios de Ranson a su ingreso y a las 48 horas como leves y se manejaron con tratamiento conservador con buena evolución. Todos fueron dados de alta del hospital antes de 5 días de manejo; no hubo mortalidad.
]]>
En la tabla III se consignan los diferentes factores de riesgo que se analizaron para el desarrollo de hiperamilasemia, encontrando significancia estadística para prevenir hiperamilasemia en el grupo de estudio independientemente de la naturaleza de la patología biliar. También hubo un menor número de casos de hiperamilasemia en el grupo de estudio cuando se realizó esfinterotomía (p = 0,03), biopsia y cepillado (p = 0,008) y al canalizar el conducto pancreático aunque con una significancia estadística marginal (p = 0,06). No hubo diferencia cuando se requirió de la colocación de prótesis (p = 1,0).
Todos los pacientes que desarrollaron pancreatitis clínicamente evidente se sometieron a esfinterotomía o canalización y opacificación del conducto pancreático. La tabla IV muestra la distribución de diagnósticos y procedimientos realizados durante la CPRE.
Encontramos una reducción del riesgo absoluto (RRA) de 10,7%, con una reducción del riesgo relativo (RRR) del 66% y un número necesario a tratar (NNT) de 13 para evitar un episodio de pancreatitis clínicamente evidente. No observamos ningún evento adverso con el uso de la indometacina rectal o la glicerina.
Discusión
La indometacina fue introducida en 1963 para el tratamiento de la artritis reumatoide y trastornos relacionados. Tiene propiedades antinflamatorias, analgésicas y antipiréticas semejantes a los salicilatos. Los efectos terapéuticos son consecuencia de su propiedad para inhibir la producción de prostaglandinas.
La primera enzima en la vía sintética de las prostaglandinas es la endoperóxido sintetasa o ciclooxigenasa de ácidos grasos; esta transforma al ácido araquidónico en productos intermediarios inestables. Se sabe ahora que hay dos formas de ciclooxigenasa llamadas ciclooxigenasa-1 (COX-1) y ciclooxigenasa-2 (COX-2). La primera es una isoforma constitutiva que aparece en vasos sanguíneos, estómago y riñones, en tanto que la segunda se presenta en situaciones de inflamación por citocinas y mediadores inflamatorios. La biotransformación de los productos de ciclooxigenasas PGG2/PGH2 difiere de un tejido a otro y depende de las actividades enzimáticas metabolizantes de PGG2/PGH2 particulares existentes. El ácido araquidónico también puede ser transformado por vía de la 5-lipooxigenasa en diversos leucotrienos. La indometacina y el resto de AINE inhiben la enzima ciclooxigenasa y la producción de prostaglandinas, pero no suprimen las vías de la lipooxigenasa ni la formación de leucotrienos. También inhibe la motilidad de los leucocitos polimorfonucleares. A diferencia de otros AINE, desacopla la fosforilación oxidativa a concentraciones supraterapéuticas y deprime la biosíntesis de los mucopolisacáridos (28).
La indometacina y la mayor parte de los AINE son ácidos orgánicos y a diferencia del ácido acetilsalicílico constituyen inhibidores competitivos reversibles de la actividad de ciclooxigenasa. En la forma de ácidos orgánicos, dichos compuestos casi siempre se absorben después de la ingestión, luego se ligan ávidamente a las proteínas plasmáticas y se excretan por filtración glomerular o secreción tubular. Por esa razón la indometacina, la aspirina y otros AINE se acumulan en sitios de inflamación, lo cual constituye una propiedad farmacocinética atractiva de los productos que se pretenden usar como antiinflamatorios. Tras la administración de dosis orales únicas de 25 ó 50 mg, la indometacina se absorbe fácilmente y alcanza concentraciones plasmáticas máximas de aproximadamente 1 y 2 mcg/ml respectivamente unas dos horas después de la administración. Tiene una biodisponibilidad de prácticamente 100% y a las cuatro horas se absorbe el 90% de la dosis administrada. La eliminación es por excreción renal, transformación metabólica, excreción biliar y experimenta una considerable circulación enterohepática. Se ha calculado que su semivida media es de alrededor de 4,5 horas. La absorción por vía rectal es ligeramente mayor (80-90%) que la absorbida de la cápsula (28).
]]> Dentro de los límites de variación de las concentraciones plasmáticas terapéuticas alrededor de 99% de la indometacina se une a las proteínas plasmáticas. También atraviesa la barrera hematoencefálica y la placenta (29). En cuanto a los mecanismos del daño pancreático, la fosfolipasa A2 (FLA2) juega un papel importante en la cascada inflamatoria inicial por medio de la regulación de mediadores proinflamatorios, incluyendo prostaglandinas, leucotrienos y factor activador de plaquetas (22). La inhibición de FLA2 ha sido el objetivo de varios agentes terapéuticos usados para tratar pancreatitis aguda no inducida por CPRE con resultados decepcionantes. En estudios previos sólo el mesilato de gabexato ha demostrado prevenir el daño pancreático relacionado con la CPRE y reduce la incidencia (30).Ebbehoj y cols. (31) informaron de los resultados de un ensayo clínico controlado de pacientes con pancreatitis aguda, en el que la administración de indometacina 50 mg vía rectal dos veces al día, disminuyó el dolor y la necesidad de uso de analgésicos opiáceos en el grupo tratado. Estos resultados prometedores fundamentaron nuestra idea de investigación para el desarrollo de este proyecto. Previamente, Murray y cols. (32), en un ensayo clínico controlado, demostraron que la aplicación de 100 mg de diclofenaco por vía rectal dos horas después del procedimiento redujo la incidencia de episodios de pancreatitis, ya que el evento se presentó en el 6,4% de los pacientes del grupo de estudio contra el 15,5% de los pacientes del grupo control (p ≤ 0,05). En nuestro estudio, la incidencia en el grupo de estudio fue de 5,3 contra 16% (p ≤ 0,05). Por fortuna, a diferencia del estudio anterior, la totalidad de los pacientes tuvieron pancreatitis leve contrario al estudio de Murray, quienes observaron en sus 24 pacientes con pancreatitis dos eventos graves por presencia de necrosis (8,3%).
Sin duda, se han identificado una gran variedad de factores para el desarrollo de pancreatitis post-CPRE. En un estudio reciente, Loperfido y cols. (33) identificaron tres factores de riesgo para el desarrollo de pancreatitis post-CPRE: conducto biliar no dilatado, opacificación del conducto pancreático y edad < 70 años. Un segundo estudio multicéntrico italiano (34) demostró tres factores de riesgo estadísticamente significativos: imposibilidad de eliminar litos del conducto biliar, esfinterotomía con precorte y edad < 60 años. Un estudio multicéntrico estadounidense (7) reveló otros factores de riesgo, como: historia de pancreatitis post-CPRE, dilatación con balón del esfínter biliar, canulación difícil, esfinterotomía pancreática, más de una inyección de contraste, disfunción del esfínter de Oddi, género femenino, bilirrubina sérica normal y la ausencia de pancreatitis crónica. Finalmente, un estudio francés (8) apoyó la esfinterotomía con precorte y la presencia de disfunción del esfínter de Oddi como variables independientes que aumentaron el riesgo de pancreatitis. Entre nuestros casos encontramos un franco efecto protector de la indometacina independientemente de la enfermedad y el procedimiento endoscópico realizado a excepción de la colocación de endoprótesis.
Con la identificación de varios factores de riesgo relacionados con el paciente (vgr; jóvenes, género femenino, historia de pancreatitis post-CPRE, etc.), los endoscopistas pueden usar ahora esta información en un análisis riesgo-beneficio cuando decidan realizar CPRE.
La mayoría de los casos de pancreatitis post-CPRE son leves; sin embargo, puede ocurrir pancreatitis severa hasta en 20% definida como desarrollo de necrosis, pseudoquiste, absceso o falla multiorgánica. Mientras la mayoría (22/24; 92%) de los pacientes que desarrollaron pancreatitis post-CPRE en el estudio de Murray tuvieron sólo pancreatitis leve, 8% (2/24) de los que la desarrollaron tuvieron la forma severa (32). En nuestro ensayo todos los casos fueron de la forma leve, sin evidencia clínica de necrosis pancreática o peripancreática.
La prevención de esta complicación es de primordial importancia. Una amplia variedad de medios farmacológicos para evitar pancreatitis post-CPRE han arrojado beneficios marginales. Los agentes más prometedores son somatostatina y gabexato, cuyos beneficios fueron significativos de acuerdo a Andriulli y cols. (21). No obstante, ambos agentes no están disponibles en Estados Unidos y requieren administración intravenosa (33). Andriulli y cols., compararon a ambos contra placebo sin encontrar efecto protector alguno. Octreótida, un análogo de la somatostatina de acción prolongada tampoco ha demostrado efectividad en la prevención de pancreatitis post-CPRE.
Otros agentes, tales como IL-10 (34,35) y gliceril trinitrato (nitroglicerina) (36,37) han revelado resultados alentadores; sin embargo, los datos con IL-10 son inconsistentes y la hipotensión inducida por la nitroglicerina limita su uso. En otro estudio, la heparina ha demostrado efectividad preventiva (38), pero se requieren ensayos controlados para confirmarlo.
Además de la farmacoterapia han sido utilizados métodos mecánicos para prevenir la pancreatitis, incluyendo la colocación de endoprótesis en el conducto pancreático de pacientes con alto riesgo. Las evidencias disponibles demuestran un importante efecto protector, aunque son apenas alentadores: requieren la confirmación a través de estudios controlados (9,39).
En fecha reciente, Menis (40) y Mahjoub (41) informaron dos casos de pancreatitis probablemente inducida por indometacina. Ambos pacientes del sexo masculino mayores de 50 años eran portadores de artritis reumatoide y recibían tratamiento con indometacina oral por al menos tres semanas. En el primer caso se identificó litiasis vesicular y en el segundo dilatación del conducto pancreático, sin embargo ambos autores consideraron que el único factor etiológico era la ingesta de este fármaco. No establecen mecanismo etiológico preciso, pero suponen que la pancreatitis se presenta como una respuesta a una disminución en los niveles de glutation, disminución en la actividad superóxido e incremento en el estrés oxidativo. En la más reciente actualización del catálogo de medicamentos inductores de pancreatitis publicado por Trivedi y Pitchumoni (42), incluyen a los analgésicos antiinflamatorios no esteroideos como fármacos clase III (entre los cuales destaca el diclofenaco y no consignan a la indometacina) o fármacos posiblemente inductores de pancreatitis en un número menor de 10 casos reportados en la literatura. A fin de que un fármaco se considere definitivamente asociado a la aparición de pancreatitis, se requiere además del antecedente de la ingesta y mejoría del cuadro al suspender el medicamento, la recurrencia al readministrar el mismo medicamento y además para ser clasificado como clase I (definitivamente asociado), se requieren más de 20 informes de casos en la literatura internacional. Cuando este protocolo fue diseñado, se estableció como criterio de inclusión que los pacientes no tuvieran hiperamilasemia antes de la CPRE ni antecedente de ingesta de ningún analgésico anti-inflamatorio no esteroideo. Los autores consideramos que aún los pacientes del grupo de estudio que desarrollaron pancreatitis, fue resultado de la maniobra endoscópica y no producto de la aplicación de una sola dosis de indometacina vía rectal.
En conclusión, al realizar la maniobra de intervención, 13 pacientes (17,3%) del grupo de estudio y 28 (37,3%) del control presentaron hiperamilasemia. Niveles mayores de 600 UI/l se presentaron en 3 (4%) casos del grupo de estudio y 10 (13,3%) del control. Se encontró pancreatitis clínicamente evidente post-CPRE en 4 pacientes del grupo de estudio (5,3%) y 12 (16%) del control (p = 0,034, RR = 0,33). Nuestros resultados indican que el uso de indometacina vía rectal previo a la realización de CPRE disminuyó la incidencia de hiperamilasemia y pancreatitis clínica, por lo que sugerimos emplearla especialmente en aquellos pacientes con factores de riesgo para el desarrollo de esta.
]]>Bibliografía
1. Nebel OT, Silvis SE, Rogers G, Sugawa C, Mandelstam P. Complications associated with endoscopic retrograde cholangiopancreatography. Results of the 1974 A/S/G/E survey. Gastrointest Endosc 1975; 22: 34-6. [ Links ]
2. LaFerla G, Gordon S, Archibald M, Murray WR. Hyperamilasaemia and acute pancreatitis following endoscopic retrograde cholangiography. Pancreas 1986; 1: 160-3.
3. De Palma GD, Catanzano C. Use of corticosteroids in the prevention of post-ERCP pancreatitis: Results of a controlled prospective study. Am J Gastroenterol 1999; 94: 982-5.
4. Rabenstein T, Hahn EG. Post-ERCP pancreatitis: New momentum. Endoscopy 2002; 34: 325-9.
5. García Cano Lizcano J, González Martín JA, Morillas Ariño J, Pérez Sola A. Complications of endoscopic retrograde cholangiopancreatography. A study in a small ERCP Unit. Rev Esp Enferm Dig 2004; 96: 163-73.
6. Vaira D, D'Anna L, Ainley C, Dowsett J, Williams S, Baillie J, et al. Endoscopic sphincterotomy in 1000 consecutive patients. Lancet 1989; 2: 431-4.
7. Freeman ML, DiSario JA, Nelson DB, Fennerty MB, Lee JG, Bjorkman DJ, et al. Risk factors for post-ERCP pancreatitis: a prospective, multicenter study. Gastrointest Endosc 2001; 54: 425-34.
8. Barthet M, Lesavre N, Desjeux A, Gasmi M, Berthezene P, Berdah S, et al. Complications of endoscopic sphincterotomy: Results from a single tertiary referral center. Endoscopy 2002; 34: 991-7.
]]> 9. Rodríguez Muñoz S. Towards safer ERCP: Selection, experience and prophylaxis. Rev Esp Enferm Dig 2004; 96: 155-62.10. Podolsky I, Haber GB, Kortan P, Gray R. Risk factors for pancreatitis following ERCP. A prospective study (abstr). Am J Gastroenterol 1987; 82: 972A.
11. Bilbao MK, Dotter CT, Lee TG, Katon RM. Complications of endoscopic retrograde cholangiopancreatography (ERCP). A study of 10,000 cases. Gastroenterology 1976; 70: 314-20.
12. Freeman ML, Nelson DB, Sherman S, Haber GB, Herman ME, Dorsher PJ, et al. Complications of endoscopic biliary sphincterotomy. N Engl J Med 1996; 335: 909-18.
13. Messmann H, Vogt W, Holstege A, Lock G, Heinisch A, von Furstenberg A, et al. Post ERP pancreatitis as a model for cytokine induced acute phase response in acute pancreatitis. Gut 1997; 40: 80-5.
14. Karne S, Gorelick FS. Etiopathogenesis of acute pancreatitis. Surg Clin North Am 1999; 79: 699-710.
15. Bhatia M, Brady M, Shokuhi S, Christmas S, Neoptolemos JP, Slavin J. Inflammatory mediators in acute pancreatitis. J Pathol 2000; 190: 117-25.
16. Silvis SE, Vennes JA. The role of glucagon in endoscopic cholangiopancreatography. Gastrointest Endosc 1975; 21: 162-3.
17. Odes HS, Novis BN, Bank S. Effect of calcitonin on the serum amylase levels after endoscopic retrograde cholangiopancreatography. Digestion 1977; 16: 180-4.
18. Sand J, Nordback I. Prospective randomized trial of the effect of nifedipine on pancreatic irritation after endoscopic retrograde cholangiopancreatography. Digestion 1993; 54: 105-11.
]]> 19. Arcidiacono R, Gambitta P, Rossi A, Grosso C, Bini M, Zanasi G. The use of a long-acting somatostatine analogue (octreotide) for prophylaxis of acute pancreatitis after endoscopic sphincterotomy. Endoscopy 1994; 26: 715-8.20. Dumot JA, Conwell DL, O'Connor JB, Ferguson DR, Vargo JJ, Barnes DS, et al. Pretreatment with methylprednisolone to prevent ERCP induced pancreatitis: A randomized, multicenter, placebo controlled clinical trial. Am J Gastroenterol 1998; 93: 61-5.
21. Andriulli A, Leandro G, Niro G, Mangia A, Festa V, Gambassi G, et al. Pharmacologic treatment can prevent pancreatic injury after ERCP: A meta-analysis. Gastrointest Endosc 2000; 51: 1-7.
22. Gross V, Leser HG, Heinisch A, Scholmerich J. Inflammatory mediators and cytokines: New aspects of the pathophysiology and assessment of severity of acute pancreatitis? Hepatogastroenterology 1993; 40: 522-30.
23. Makela A, Kuusi T, Schroder T. Inhibition of serum phospholipase A2 in acute pancreatitis by pharmacological agents in vitro. Scand J Clin Lab Invest 1997; 57: 401-7.
24. Wildenhain PM, Melhem MF, Birsic WI, Sell HW, Rao KN. Acute hemorrhagic pancreatitis in mice: Improved survival after indomethacin administration. Digestion 1989; 44: 41-51.
25. Mejía Aranguré JM, Fajardo Gutiérrez A, Gómez Delgado A, Cuevas Orióstegui ML, Hernández Hernández DM, Garduño Espinosa J, et al. El tamaño de la muestra: un enfoque práctico en la investigación clínica. Bol Med Hosp Infant Mex 1995; 52: 381-90.
26. Osvaldt AB, Viero P, Borges da Costa MS, Wendt LR, Bersch VP, et al. Evaluation of Ranson, Glasgow, APACHE-II, and APACHE-O criteria to predict severity in acute biliary pancreatitis. Int Surg 2001; 86: 158-61.
27. Montaño Loza A, García Correa J, González Ojeda A, Fuentes Orozco C, Davalos Cobián C, Rodríguez Lomelí X. Prevención de hiperamilasemia y pancreatitis posterior a colangiografía retrógrada endoscópica con la administración rectal de indometacina. Rev Gastroenterol Mex 2006; 71: 262-8.
27. Insel PA. Analgesic, antipyretic and anti-inflammatory agents and drugs employed in the treatment of Gout. In Goodman and Gilman. The Pharmacological basis of therapeutics. 9th ed. Nashville, Tennessee: McGraw Hill 1996. p. 643-5.
]]> 28. Giagoudakis G, Markantonis SL. Relationships between the concentrations of prostaglandins and the nonsteroidal anti-inflammatory drugs indomethacin, diclofenac, and ibuprofen. Pharmacotherapy 2005; 25: 18-25.29. Italian Digestive Endoscopy Group: Cavallini G, Tittobello A, Frulloni L, Masci E, Mariana A, Di Francesco V. Gabexate for the prevention of pancreatic damage related to endoscopic retrograde cholangiopancreatography. N Engl J Med 1996; 335: 919-23.
30. Ebbehoj N, Friis J, Svendsen LB, Bulow S, Madsen P. Indomethacin treatment of acute pancreatitis. A controlled double-blind trial. Scand J Gastroenterol 1985; 20: 798-800.
31. Murray B, Carter R, Imrie C, Evans S, O'suilleabhain C. Diclofenac reduces the incidence of acute pancreatitis after endoscopic retrograde cholangiopancreatography. Gastroenterology 2003; 124: 1786-91.
32. Loperfido S, Angelini G, Benedetti G, Chilovi F, Costan F, De Bernardinis F, et al. Major early complications from diagnostic and therapeutic ERCP: A prospective multicenter study. Gastrointest Endosc 1998; 48: 1-10.
33. Masci E, Toti G, Mariani A, Curioni S, Lomazzi A, Dinelli M, et al. Complications of diagnostic and therapeutic ERCP: A prospective multicenter study. Am J Gastroenterol 2001; 96: 417- 23.
34. Deviere J, Le Moine O, Van Laethem JL, Eisendrath P, Ghilain A, Severs N, et al. Interleukin-10 reduces the incidence of pancreatitis after therapeutic endoscopic retrograde cholangiopancreatography. Gastroenterology 2001; 120: 498-505.
35. Dumot JA, Conwell DL, Zuccaro G, Vargo JJ, Shay SS, Easley KA, et al. A randomized double blind study of interleukin 10 for the prevention of ERCP-induced pancreatitis. Am J Gastroenterol 2001; 96: 2098-102.
36. Sudhindran S, Bromwich E, Edwards PR. Prospective randomized double-blind placebo-controlled trial of glyceryl trinitrate in endoscopic retrograde cholangiopancreatography-induced pancreatitis. Br J Surg 2001; 88: 1178-82.
37. Moreto M, Zaballa M, Casado I, Merino O, Rueda M, Ramírez Z, et al. Transdermal glyceryl trinitrate for prevention of post-ERCP pancreatitis: A randomized double-blind trial. Gastrointest Endosc 2003; 57: 1-7.
]]> 38. Rabenstein T, Roggenbuck S, Framke B, Martus P, Fischer B, Nusko G, et al. Complications of endoscopic sphincterotomy: Can heparin prevent acute pancreatitis after ERCP? Gastrointest Endosc 2002; 55: 476-83.39. Frank CD, Adler DG. Post-ERCP pancreatitis and its prevention. Nat Clin Pract Gastroenterol Hepatol 2006; 3: 680-8.
40. Memis D, Akalin E, Yüvel T. Indomethacin-induced pancreatitis. A case report. JOP 2005; 6: 344-7.
41. Mahjoub W, Jarboui S, Ben Moussa M, Abdesselem MM, Zaouche A. Indomethacin-induced pancreatitis; a second case report. JOP 2006; 7: 321-3.
42. Trivedi ChD, Pitchumoni CS. Drug-induced pancreatitis. An update. J Clin Gastroenterol 2005; 39: 709-16.
![]() Dirección para correspondencia:
Dirección para correspondencia:
Alejandro González Ojeda.
C/ José Enrqiue Rodó 2558. ]]>
Colonia Providencia.
44670 Guadalajara, Jalisco, México.
Fax: 00 52 33 3848-5400.
e-mail: avygail5@yahoo.com.mx
Recibido: 31-07-06.
Aceptado: 16-03-07.