REVISIÓN
Tratamiento del dolor en el anciano: opioides y adyuvantes
Drug treatment invasive joint in osteoarthritis
M.P. Sáez López, N. Sánchez Hernández1, S. Jiménez Mola2, N. Alonso García1 y J.A. Valverde García1
Unidad de Geriatría y 1Servicio de Cirugía Ortopédica y Traumatología. Complejo Asistencial de Ávila.
2Unidad de Geriatría. Complejo Asistencial de León
RESUMEN
Se dispone de pocos estudios sobre el uso de opioides en ancianos.
En pacientes seleccionados, los opioides pueden proporcionar una adecuada analgesia en el marco de un abordaje integral. Se ha revisado la utilización de opioides fuertes en ancianos con dolor oncológico o no oncológico. Se ha demostrado eficacia en dolor músculo-esquelético a corto plazo y algunos tipos de dolor neuropático. No obstante, no se dispone de datos sobre eficacia y seguridad a largo plazo. Aunque los antidepresivos tricíclicos son eficaces para el dolor neuropático, sus efectos anticolinérgicos suponen un problema para el anciano. Antiepilépticos como gabapentina y pregabalina son eficaces para el dolor neuropático y mejor tolerados. La administración tópica de algunos fármacos mejora la tolerabilidad de los mismos.
Palabras clave: Anciano, dolor, fragilidad, analgésicos opioides, adyuvantes.
ABSTRACT
There is a small number of primary studies relating to opioid use in older people.
In carefully selected and monitored patients, opioids may provide effective pain relief as part of comprehensive pain management strategy. Use of strong opioids in the management of chronic, severe cancer and non-cancer pain in older people has been reviewed. Studies have demonstrated short-term efficacy in persistent musculoskeletal pain and various neuropathic pains. However, longer-term efficacy and safety data are lacking. Some adjuvant drugs should be considered for older people with neuropathic. Although tricyclic antidepressants have good efficacy, anticholinergic side effects are often problematic for older people. Anti-epileptic drugs such as gabapentin or pregabalin, are effective for neuropathic pain and are probably better tolerated. Topical administration may have improved tolerability than other routes of administration and may be preferable for elderly.
Introducción
Con frecuencia, el dolor del anciano no se controla con fármacos de primer escalón. En el dolor moderado-severo y en el dolor neuropático tienen su indicación los opioides y los adyuvantes. Como ocurre con muchos fármacos, no se dispone de clara evidencia que nos permita utilizar estos fármacos con seguridad, pero cada vez hay más experiencia que avala su uso.
Opioides
Opioides en el anciano
Según la OMS, el tratamiento con opioides es de elección para el dolor oncológico moderado-severo y cada vez existe mayor evidencia para el dolor no oncológico.
No se dispone de una clara evidencia sobre el tratamiento de opioides en ancianos, ya que sólo el 3,4 % de los ensayos randomizados incluyen a ancianos, y siempre menores de 85 años y sin pluripatología. Por este motivo, el uso de estos fármacos en la población geriátrica se basa en la experiencia y en los resultados de los estudios realizados en población adulta (1). Además, las reticencias al uso de opioides todavía están presentes (aunque menos que hace unos años), lo que interfiere en gran medida en el correcto abordaje del dolor (2).
De hecho, en ancianos que están en tratamiento con opioides, si sufren deterioro funcional o cognitivo se suele atribuir al opioide, aunque tenga buena eficacia analgésica. Son muchos los fármacos o patologías agudas que pueden provocar deterioro funcional y cognitivo, por lo que una adecuada valoración geriátrica puede ayudar a diagnosticar la causa (3).
]]> Efectos secundarios de los opioides en el ancianoLos ancianos tienen un 10-25 % más de riesgo de desarrollar efectos adversos que los jóvenes, lo que interfiere con el uso a largo plazo y el cumplimiento terapéutico. La mayoría de los efectos adversos disminuyen con el uso a largo plazo, excepto el estreñimiento. Una adecuada titulación, prevención e información sobre los efectos secundarios, mejora la adherencia y la eficacia de estos fármacos.
Según Barber, la posibilidad de sufrir efectos secundarios, especialmente con daños en órganos, es superior para los AINE que para los opioides (4). Para minimizar los posibles efectos secundarios es preciso seguir las siguientes pautas:
- Siempre que se prescribe opioide añadir laxante y antiemético preventivo al inicio del tratamiento.
- Hidratación adecuada.
- Revisar el resto de tratamiento para prevenir posibles interacciones, especialmente si toma algún psicofármaco.
- Evaluar balance riesgo/beneficio y respuesta analgésica.
- Asegurar el cumplimiento terapéutico.
Y cuando aparecen efectos secundarios, se puede bajar la dosis del opioide o rotarle, o cambiar la vía de administración o manejar los síntomas de los efectos adversos con otros medios.
]]> Efectos secundarios gastrointestinalesLos ancianos tienen aumentado el pH gástrico, reducida la motilidad gástrica e intestinal y menor actividad enzimática y absorción. Estos cambios favorecen aún más el tránsito intestinal prolongado.
Es el efecto secundario más frecuente y se mantiene en el tiempo (50-100 % de los pacientes). Además del uso de laxantes, se puede plantear la metilnaltrexona, que por su efecto antagonista opioide no selectivo con mayor afinidad por el receptor mu, puede aliviar el estreñimiento. También la naloxona oral se utiliza con este fin y se han comercializado combinaciones de naloxona y oxicodona.
Las náuseas y vómitos se pueden tratar con metoclopramida, clorpromazina y ondasentrón, y suelen desaparecer días después del inicio del tratamiento.
Depresión respiratoria
La depresión respiratoria está mediada por el receptor opioide mu, y agonistas puros, como la morfina y el fentanilo, tienen un efecto dosis dependiente y a altas dosis o combinados con otros depresores del SNC pueden provocar apnea (5).
La buprenorfina tiene un efecto techo para la depresión respiratoria. Aunque no se conoce la razón, podría ser que la dosis analgésica es inferior a la necesaria para producir depresión respiratoria. De cualquier forma, si aparece depresión respiratoria con buprenorfina se puede revertir con antagonistas opioides como naloxona pero en infusión continua durante al menos 90 minutos o más, no sólo hasta que se normalice la respiración.
Es un efecto poco frecuente, que no suele ocurrir con un adecuado manejo de los fármacos (titulación y monitorización cuidadosa), ni en pacientes que tienen dolor.
Los pacientes con apnea del sueño o enfermedad pulmonar obstructiva crónica presentan mayor riesgo de depresión respiratoria, por lo que precisan una mayor monitorización. También el uso de altas dosis de opioides o una rápida titulación en ancianos que no lo tomaban previamente o que tenían cierto grado de sedación previo puede favorecer la aparición de este problema.
Neurotoxicidad
]]> Se manifiesta como deterioro cognitivo, delirium, trastornos perceptivos, alteración del nivel de conciencia, alodinia e hiperalgesia, crisis comiciales y mioclonias. La mayoría de los opioides tienen estos efectos, especialmente en pacientes deshidratados, con insuficiencia renal y muy enfermos.El tratamiento consiste en evaluar todo el tratamiento, reducción de dosis de opioide o rotación si precisa, hidratar y manejar los síntomas.
En el caso de las mioclonías se puede utilizar midazolam o baclofeno.
Los pacientes ancianos con opioides tienen el doble de riesgo de sufrir delirium (6).
Morrison encontró que el riesgo de delirium en pacientes sin demencia previa disminuía según aumentaba la dosis de opioides diaria en ancianos con fractura de cadera. También se ha observado que el dolor severo medido con escala aumenta 9 veces el riesgo de delirium. Por tanto, los opioides aumentan el delirium pero el dolor probablemente más.
La meperidina es el opioide con mayor riesgo de delirium.
Lesiones
En un metanálisis de 6 estudios observacionales encontraron que la exposición a opioides aumentaba un 38 % el riesgo de fracturas, doblándose el riesgo si la dosis de morfina es superior a 50 mg de morfina oral al día o equivalente (7).
También se han relacionado con aumento de lesiones, laceraciones, aunque en estos pacientes puede haber muchos factores de confusión. El uso combinado de psicotropos aumentó mucho el riesgo de caídas recurrentes.
Otros efectos adversos
]]> El prurito puede aparecer en el 2-10 % de los pacientes y se suele tratar con antihistamínicos.La acción anticolinérgica predispone, además del estreñimiento e impactación fecal, a la retención urinaria.
La metadona puede prolongar el intervalo Q-T y provocar arritmias como torsades de pointes.
Se pueden dar aumento de niveles de prolactina y disminución de hormonas sexuales.
Otros efectos que se han descrito son mayor mortalidad, más hospitalizaciones y mayor riesgo de neumonía en inmunocompetentes (especialmente con codeína, morfina, fentanilo y metadona) (8).
Sobredosis de opioides
Se caracteriza por disminución del nivel de conciencia, de las respiraciones por minuto, de los ruidos intestinales, hipotensión, hipotermia y pupilas mióticas. Ante estas circunstancias se debe mantener la vía aérea y respiración, administrar naloxona y no está indicado el lavado gástrico.
Tipos de opioides
Tramadol
Es un analgésico bimodal, agonista del receptor opioide mu e inhibidor de recaptación de serotonina y norepinefrina. Por estos múltiples mecanismos, la droga es útil para tratar dolor agudo y crónico, neuropático y nociceptivo.
]]> No obstante, también tiene los efectos adversos de los antidepresivos y de los opioides. Los más frecuentes son náuseas, estreñimiento y mareo, que puede aumentar el riesgo de caídas y fracturas.Deprime poco el centro respiratorio, tiene actividad antitusígena y menor estreñimiento y sedación que los opiáceos puros.
En administración crónica puede producir tolerancia, pero menos intensa y de aparición más lenta que otros fármacos del grupo.
Puede provocar convulsiones si se excede la dosis recomendada por el menor aclaramiento del fármaco, por lo que se debe ajustar la dosis en mayores de 75, y evitar en pacientes epilépticos.
La retirada de este fármaco debe ser paulatina para evitar el síndrome de retirada de serotonina que cursa con náuseas y mareo.
No puede tomarse junto con IMAOs y se recomienda evitar antidepresivos y ciclobenzaprina.
El tramadol tiene potenciales interacciones con inhibidores de CYP2D6 (quinidina, cimetidina) que pueden enlentecer su metabolismo, y con inductores de CYP2D6 (carbamacepina) que pueden aumentar el metabolismo de opioides.
Además, el tramadol puede potenciar el efecto de otros inhibidores de la recaptación de serotonina y noradrenalina (IRSN) y otros agentes de acción central, con riesgo de provocar el síndrome serotoninérgico.
Revisiones de la Cochrane encontraron eficacia analgésica y para el dolor neuropático con NNT (número de pacientes a tratar para conseguir que un paciente obtenga un 50 % de alivio de dolor) entre 3,8 y 6 y NNH (9) (número de pacientes a tratar para que un paciente sufra un evento adverso) de 8,3, aunque con 2,27 veces mayor riesgo de desarrollar efectos adversos menores.
En pacientes muy mayores, empezar con dosis menores (gotas, solución) para titular la dosis analgésica. Se recomienda iniciar 25 mg/8 h y no sobrepasar los 200-300 mg/día, prefiriéndose la liberación retardada (10).
]]> La combinación de tramadol 37,5 y paracetamol 325 mg alcanza control de dolor con menor dosis de cada fármaco, mejorando la seguridad.Los parámetros farmacocinéticos se complementan con rápido comienzo del paracetamol y efecto prolongado del tramadol.
Codeína
Indicado para el dolor leve-moderado. Opiáceo agonista puro derivado de morfina de menor potencia analgésica, que se metaboliza a morfina por CYP2D6.
Provoca náuseas y estreñimiento con frecuencia, lo que requiere añadir laxante y antiemético.
Hay un grado de variabilidad en su eficacia porque el 30 % de los pacientes lo metabolizan lentamente y puede no producir analgesia. También un porcentaje inferior (1-3 % de los británicos) son metabolizadores ultrarrápidos de codeína y tramadol, por lo que se convierten en las formas activas rápidamente, con riesgo de provocar depresión respiratoria y apnea (11).
Por otro lado, la conversión en metabolitos activos es inhibida por fármacos como cimetidina, haloperidol, amitryptilina e inhibidores de la recaptación de serotonina.
Tiene techo analgésico y riesgo de acumularse en pacientes con insuficiencia renal.
En el anciano se recomienda limitar su uso como antitusígeno, utilizar opciones más seguras como analgésicos, y optimizar la dosis en las combinaciones con paracetamol o AINE.
Morfina
]]> Es el fármaco más representativo de los opioides y el más utilizado. Está indicado en el dolor moderado-severo.Es el único sin límite de dosis (sin techo analgésico), mientras se obtenga analgesia y no aparezcan efectos secundarios (somnolencia, déficit de memoria, desorientación, etc.).
El inicio de tratamiento debe ser lento e incrementos lentos (20-25 % de dosis inicial cada 3-4 días hasta analgesia). Utilizando fórmulas rápidas se recomienda 5-10 mg/12 h comenzando por la noche, y por vía parenteral 1,5-2,5 mg/4 h. Con fórmulas retardadas se puede empezar con 10 mg cada 24 h.
Tiene una buena absorción digestiva y una vida media corta (2-4 h), lo que es útil para la titulación rápida.
La eliminación es por vía renal y es hidrofílico, por lo que la velocidad de distribución es menor, así como la eliminación por descenso de aclaramiento renal.
Un estudio sobre cambios farmacocinéticos de morfina (12) encuentra menor aclaramiento por menor volumen de distribución y mayor pico máximo de concentración plasmática en ancianos respecto a jóvenes. Esto supone mayor riesgo de acumularse el metabolito activo y de toxicidad.
La morfina es ampliamente metabolizada en el hígado, excepto el 10 % que se excreta por la orina sin cambios.
Mediante la glucuronización se transforma la mayor parte de morfina en morfina 3 glucurónido y morfina 6 glucurónido. Este último tiene gran afinidad por el receptor mu y el doble de potencia analgésica, mientras que la morfina 3 glucurónido se cree que es la responsable de los efectos neurotóxicos y contribuye al riesgo de crisis comiciales. Los dos metabolitos se eliminan por vía renal.
Se ha encontrado relación entre la fragilidad y alteración de la conjugación, lo que podría explicar la farmacología clínica en esta población. No obstante, los efectos de la edad sobre la farmacocinética de la morfina no explican la mayor sensibilidad de esta población al fármaco.
Sí se conoce cada vez más la variabilidad genética en cuanto al gen que influye en el receptor del opioide, lo que contribuye en la variabilidad de la respuesta a morfina y otros opioides (13).
]]> FentaniloEs un agonista puro con actividad analgésica más potente que la morfina (80-100 veces más), indicado en el dolor moderado-severo.
Este opioide semisintético potente es muy lipofílico y penetra la barrera hematoencefálica rápidamente consiguiendo una analgesia rápida.
La forma de administración transdérmica es posible por su bajo peso molecular, alta permeabilidad y alta liposolubilidad (dosis 12, 25, 50, 75, y 100 mcg/h/10 cm2 cada 72 h). Otras formas de administración son nasal, transmucoso, bucal y sublingual, y son una buena alternativa para el dolor irruptivo por su rapidez de acción.
No tiene presentación oral adecuada por el importante efecto de primer paso.
Se elimina vía renal y precisa ajuste en insuficiencia renal e insuficiencia hepática.
En ancianos, el aclaramiento está disminuido y la vida media aumentada, pero se desconoce si estos cambios influyen en la fórmula transdérmica.
Levron (14) no encuentra diferencia en concentraciones plasmáticas de fentanilo transdérmico en pacientes menores de 65 y mayores de 75 años.
La naturaleza lipofílica del fentanilo puede provocar un amplio volumen de distribución. Dado que el anciano tiene proporcionalmente más masa grasa, el fentanilo tendrá mayor volumen de distribución y mayor vida media.
Además, el fentanilo tiene una gran extracción hepática, por lo que la menor perfusión hepática relacionada con la edad puede conllevar menor aclaramiento.
]]> Ariano (15) comparó la farmacocinética de una única dosis de fentanilo en jóvenes y mayores y, aunque no encontró diferencia en volumen de distribución ni aclaramiento, sí encontró mayor variabilidad entre los sujetos mayores y variabilidad entre las concentraciones del fármaco entre los distintos pacientes (16).La fórmula transdérmica implica retraso en el inicio del efecto y persiste analgesia y posibles efectos secundarios tras la retirada (continúa la absorción de la piel y permanece el 50 % a las 17 h de la retirada). Este hecho debe tenerse en cuenta si se hace rotación de opioide, iniciando el nuevo fármaco unas horas después de la retirada del fentanilo.
Aunque se puede pensar que cambios en temperatura, sudor e integridad de la piel pueden influir en su absorción, la inclusión de una membrana que limita la liberación hace que sólo cambios extremos afecten a la misma.
El impacto de la fragilidad de muchos ancianos sobre CYP3A4 puede influir en el aclaramiento del fármaco, más que la propia edad cronológica. No obstante, todavía no se ha investigado el efecto de la inflamación asociada a la fragilidad.
Aunque la duración de acción suele ser de 3 días, en ancianos varía de 48 a 96 horas.
El efecto máximo de primera dosis ocurre a las 18-24 h, por ello, puede necesitar un opioide de acción corta las primeras horas.
La dosis inicial, si previamente no toma opioides, es de 12 ug/3 días, haciendo incrementos de 12 en 12. Si toma morfina, se recomienda utilizar 25 de fentanilo por cada 60 mg/día de morfina oral.
Algunos autores (17,18) evalúan la tolerancia y facilidad del uso en ancianos, concluyendo que puede utilizarse durante periodos largos de tiempo en dolor oncológico.
Un metanálisis comparó fentanilo transdérmico con morfina de liberación retardada, resultando tan eficaz como morfina en dolor basal y mejor en dolor incidental en pacientes con dolor crónico no maligno (19).
El fentanilo no se recomienda para el dolor agudo por su retraso del efecto analgésico y riesgo de depresión respiratoria.
]]> BuprenorfinaEs un opioide semisintético mixto agonista de receptores u/antagonista de receptores kappa con potencia analgésica superior a la morfina (25-40 veces más).
Tiene bajo peso molecular y es muy lipofílico.
Se metaboliza en el hígado a metabolitos activos débiles que se eliminan por vía biliar, precisando ajuste en insuficiencia hepática.
La ausencia de eliminación renal y de diferencias en la farmacocinética de buprenorfina en pacientes con insuficiencia renal (20) hace que sea el preferido en pacientes nefrópatas.
Tampoco se han encontrado cambios en la farmacocinética de la forma transdérmica en pacientes mayores (21).
Se recomienda especial precaución en pacientes con problemas pulmonares o fármacos depresores del SNC, por la dificultad de revertir la posible depresión respiratoria con naloxona.
La dosis inicial si no toma previamente opioides es de 35 transdérmico, y la duración se estima de 96 h, lo que supone cambio de parche 2 días fijos a la semana (22).
Un estudio observacional prospectivo no controlado con 3 meses de seguimiento en pacientes entre 65 y 75 años concluye que es efectivo y, al menos, tan seguro como en pacientes jóvenes en las condiciones de práctica clínica habitual (23).
La buprenorfina es bien tolerada y eficaz en dolor oncológico, no oncológico y neuropático, independientemente de la edad.
]]> Ha sido utilizada cada vez más en el anciano por su disponibilidad transdérmica y por la analgesia sostenida durante un tiempo, a pesar de la falta de información de la farmacología clínica de este analgésico en ancianos frágiles.Una teórica limitación es la posibilidad de dar fármacos de liberación inmediata, como morfina/oxicodona, para dolor incidental, que sería antagonizado por buprenorfina limitando la utilidad clínica de esta combinación. Sin embargo, algunos estudios muestran que morfina y otros opioides son seguros y eficaces para este uso (21).
Buprenorfina es metabolizada por CYP3A4, pero se han observado pocas interacciones con fármacos tanto in vivo como in vitro.
Oxicodona
Es un agonista opioide semisintético con afinidad por receptores u y kappa, formulado para uso parenteral, rectal e intranasal y vía oral con liberaciones inmediata y controlada. Está indicado en el dolor moderado-severo.
Las vías de administración son oral de liberación rápida y retardada y parenteral. La dosis de inicio es de 5-10 mg/12 h vía oral.
Tiene una potencia superior a morfina (morfina/oxicodona 2/1) y mayor biodisponibilidad oral que la morfina, quizá porque el metabolismo de primer paso es menor.
Se metaboliza en el hígado mediante CYP3A4 y CIP2D6, resultando dos metabolitos activos (noroxicodona y oximorfona), y se elimina por el riñón, por lo que precisa ajuste en insuficiencia hepática y renal leve. Está contraindicada en insuficiencia hepática grave. También precisan ajuste de dosis al 30-50 % los pacientes caquécticos. Las concentraciones plasmáticas en el anciano son un 15 % superiores que en el adulto, y la duración del efecto analgésico puede ser mayor en el anciano (4-5 h en la fórmula de liberación rápida y 12 h en liberación prolongada en adultos).
Tiene un papel establecido en el dolor agudo y en los últimos años se ha estudiado su eficacia y seguridad a largo plazo en el dolor nociceptivo y neuropático. Aunque estos estudios han incluido una proporción razonable de mayores de 65 años, no disponemos de información sobre eficacia y tolerabilidad en el muy anciano.
La farmacocinética estudiada en jóvenes indica su posible seguridad en ancianos, por su vida media corta y su bajo porcentaje de excreción renal (9 %). Se suele recomendar en el anciano hospitalizado por su menor complejidad farmacológica en el ajuste de dosis en insuficiencia renal y por las escasas interacciones.
]]> Aunque no hay estudios sobre el efecto de la fragilidad en la farmacocinética y farmacodinamia de este fármaco, sí que hay un estudio que no encuentra alteraciones significativas en la respuesta a oxicodona entre mayores sanos (65-79 años) y jóvenes sanos (21-45 años) (24).Liukas (25) publicó en 2008 sobre la farmacocinética de oxicodona y sus metabolitos, encontrando mayor exposición en los mayores (70-90 años), lo que puede estar mediado por el genotipo CYP2D6, ya que los metabolizadores lentos necesitan menos dosis para el mismo efecto.
Tapentadol
Está indicado en el dolor crónico intenso en adultos que sólo se puede tratar adecuadamente con un analgésico opioide.
Tiene un mecanismo de acción dual, agonista del receptor mu e inhibidor de la recaptación de noradrenalina, lo que explica su efecto en dolor nociceptivo y dolor neuropático y su efecto "ahorrador mu opioide" con similar eficacia a otros opioides, pero con menos efectos secundarios.
La dosis de inicio es 50 mg vía oral/12 h, aunque se dispone de la presentación de 25 mg para titular mejor. El rescate se puede hacer con cualquier opioide.
Su principal metabolismo por glucuronización y en menor medida por el citocromo p450, y su baja unión a proteínas plasmáticas, conlleva un menor riesgo de interacciones y no precisa ajuste de dosis en insuficiencia renal y hepática leve. Tiene menos efectos adversos gastrointestinales que otros opioides (25).
El tapentadol ejerce su efecto analgésico directamente sin un metabolito farmacológicamente activo, lo que supone una ventaja a la hora del cálculo de dosis o la duración del efecto.
Hidromorfona
Es un opioide agonista puro de los receptores u, indicado para el dolor intenso.
]]> Tiene una vida media de 2,6 a 4 h e inicio de acción de 30 minutos.Equivalencia con morfina es de 7,5 a 1 (4 mg de hidromorfona corresponde con 30 mg de morfina).
No se metaboliza por el citocromo p450, lo que supone menor riesgo de interacciones.
La excreción renal hace que precise ajuste de dosis en insuficiencia renal o aumentar el intervalo. En pacientes con hemodiálisis se ha observado una reducción del 60 % de la dosis prediálisis.
En insuficiencia hepática se recomienda iniciar el 50 % de la dosis habitual.
Una revisión de la Cochrane 2007 concluye que, aunque parece ser un analgésico potente, no hay evidencia disponible de la superioridad respecto a la morfina.
La vía de administración es oral, con una dosis de inicio de 4-8 mg/24 h. La dosis única diaria puede favorecer el cumplimiento terapéutico (26).
Metadona
Es un antagonista del receptor NMDA, inhibidor de la recaptación de serotonina y norepinefrina y con afinidad por el receptor delta. Tiene una potencia similar o superior a la morfina. Las vías de administración disponibles son oral y parenteral.
Entre sus ventajas figuran la ausencia de metabolitos activos y la alta biodisponibilidad oral (del 80 %).
]]> Es un fármaco complejo y poco predecible porque tiene una vida media de 3-6 horas, pero la media de eliminación puede variar entre 20 y 120 h. El cálculo de la dosis equianalgésica no es sencillo. Por ello, precisa experiencia en su uso, monitorización estricta y precaución con la titulación. Además puede producir alteraciones en el intervalo QT.Puede resultar útil como alternativa en la rotación de opioides, siempre que se utilice por profesionales entrenados.
Evitar en anciano
- Propoxyphene, meperidina, pentazocina y dosis altas de tramadol (> 200 mg/día).
- La petidina tiene un metabolito que se puede acumular en paciente con insuficiencia renal.
- El propoxifeno presenta toxicidad en varios órganos, cardiotoxicidad y en SNC (por indicación de la FDA las fábricas lo están retirando del mercado americano).
- Hay que evitar la meperidina en el anciano y en insuficiencia renal por su corta duración de acción, efectos anticolinérgicos y riesgo de neurotoxicidad por acúmulo de su metabolito activo (normeperidina).
- El dextropropoxifeno tiene vida media muy larga y se ha asociado con alto riesgo de efectos secundarios en mayores.
- Con codeína y tramadol se recomienda precaución en ancianos con deterioro cognitivo por mayor riesgo de interacciones fármaco-fármaco y fármaco-enfermedad, así como mayor variabilidad en la respuesta y efectos adversos. Ambos se metabolizan por CYP2D6 a metabolitos activos determinado genéticamente o pueden producir interacciones que pueden empeorar el ratio riesgo/beneficio (27).
- Evitar la metadona por la complejidad del manejo.
]]> - Pentazocina: el aumento de la actividad farmacodinámica de los opioides en los ancianos, independiente de la farmacocinética, es parte del motivo de los efectos psicomiméticos de la pentazocina, por ello se debe evitar en ancianos.Manejo de los opioides en el anciano (28)
Teniendo en cuenta los cambios farmacocinéticos y farmacodinámicos del anciano, se debe empezar con una dosis entre el 25 y 50 % de la dosis habitual en adultos.
Se recomienda iniciar la pauta con una fórmula de acción corta para ajuste rápido y cuando la dosis sea estable, cambiar a una fórmula de liberación retardada o transdérmica.
También se puede empezar con fórmulas de liberación prolongada, utilizando dosis de rescate.
Es necesario reevaluar frecuentemente para valorar eficacia y efectos secundarios. La titulación se hace aumentando el 30 % de la dosis total diaria, a un intervalo mínimo de 24-48 h, hasta conseguir la estabilización.
La dosis del opioide viene determinada por el control analgésico, la tolerancia y la aparición de efectos secundarios.
Un 30 % de los pacientes pueden no responder al opioide pautado por distintos motivos (analgesia insuficiente o efectos secundarios intolerables) y en estos casos está indicada la rotación de opioide.
Para ello existen tablas de dosis equianalgésicas (28), que se pueden utilizar como guía sobre las potencias relativas de cada opioide, pero hay que recordar que, aunque se desarrolle tolerancia a un opioide, la estructura molecular de cada opioide y el modo de interacción con los receptores es distinto para cada fármaco/paciente, por lo que existe la llamada "tolerancia incompleta cruzada". Por ello, se recomienda una reducción inicial de la dosis equianalgésica del 25-50 % con una cuidadosa titulación individual.
La sedación y el deterioro cognitivo secundarios a opioides en ancianos se suelen tratar reduciendo la dosis de opioides, pero ocasionalmente se pueden utilizar estimulantes como dextroamfetamina y metilfenidato.
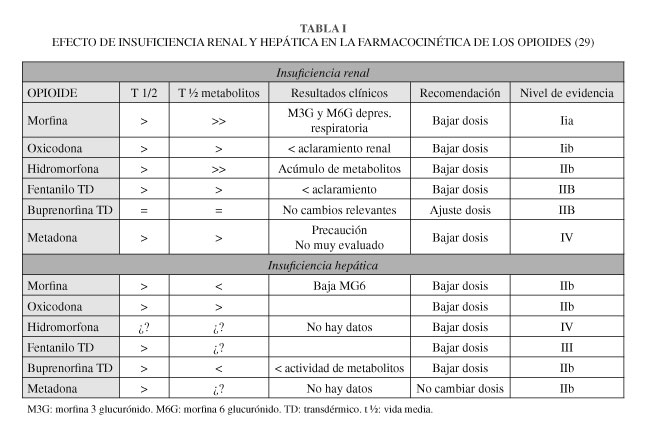
]]> Se presenta la Tabla I para el uso de opioides en pacientes con función renal y hepática alteradas (29).
Analgésicos adyuvantes
Los analgésicos coadyuvantes son fármacos que se desarrollaron para otra indicación, pero que han demostrado ser útiles en el tratamiento del dolor persistente y refractario, especialmente neuropático (Tabla II) (30).
Antidepresivos
]]> Inhiben la recaptación de monoaminas con distinto grado de selectividad. Es posible que la inhibición de recaptación de noradrenalina, como modulador descendente, sea más eficaz que la inhibición de serotonina. Han demostrado efecto analgésico, independientemente del efecto antidepresivo, y este efecto se consigue antes y con menos dosis.Antidepresivos tricíclicos (ATD)
Son fármacos que actúan en varias localizaciones: inhiben la recaptación de noradreanilina y serotonina, bloquean receptores alfa-adrenérgicos, colinérgicos, histaminérgicos y NMDA, y canales iónicos, incluso cierta actividad opioide.
Los más utilizados son amitriptilina, nortriptilina e imipramina.
Son los antidepresivos más antiguos y con mayor eficacia analgésica.
Se han mostrado eficaces en cefalea, neuralgia postherpética (NPH), y del trigémino (TGN), polineuropatía diabética (DPN), dolor oncológico neuropático y síndrome de dolor regional complejo.
Aunque tienen el menor NNT (2-3), también cuentan con el menor NNH (13-15). Esto se traduce en que este tipo de antidepresivos cuenta con múltiples efectos secundarios a múltiples niveles: anticolinérgicos (sequedad de mucosas, visión borrosa, estreñimiento, retención urinaria), cardiovasculares (hipotensión ortostática, palpitaciones, taquicardia, alteraciones de la conducción), neurológicos (mareo, sedación, insomnio, temblor, convulsiones, aumento de peso), alteración de la función hepática, disfunción sexual y reacciones anafilácticas.
Son metabolizados por sistema enzimático CYP450, con el consiguiente riesgo de interacciones farmacológicas.
Además, los tricíclicos tomados junto con fármacos activos en el SNC (serotoninérgicos, noradrenérgicos o anticolinérgicos) producen interacciones no deseadas, al igual que con fármacos cardiovasculares.
Especial precaución se debe tener en pacientes con epilepsia o si están tomando fármacos como tramadol (que disminuye el umbral de las convulsiones). Son inapropiados en ancianos con enfermedad cardiovascular o caídas.
]]> Están contraindicados en cardiópatas, epilepsia, glaucoma y desaconsejados en demencia, estreñimiento, prostatismo, retención urinaria y tratamiento habitual con opioides y antagonistas del calcio.Una revisión de la Cochrane (31) realizada sobre 61 estudios randomizados, controlados con 3.293 participantes, confirmaba evidencia suficiente sobre la eficacia de los antidepresivos en alivio, al menos moderado, del dolor neuropático.
Con tricíclicos el NNT fue de 3,6 y con venlafaxina de 3,1.
En cuanto al NNH, la Cochrane clasificó en efectos adversos mayores (los que obligó a la retirada) y menores que no afectaban necesariamente a la seguridad.
El NNH para efectos mayores fue de 28 para amitriptilina y de 16,2 para venlafaxina, mientras que para efectos menores fue de 6 y 9,5, respectivamente.
En definitiva, los antidepresivos tricíclicos son un coadyuvante de segunda línea en el anciano, mientras que en el adulto joven puede utilizarse como primera opción.
Inhibidores selectivos de la recaptación de serotonina y noradrenalina
La eficacia es menor que la de los tricíclicos.
También tienen menos efectos secundarios que se suelen relacionar con el efecto serotoninérgico (náuseas, vómitos, alteración del ritmo intestinal, anorexia, sequedad de boca, nerviosismo, agitación y sudoración).
Son considerados de primera elección en el tratamiento del dolor neuropático del anciano, especialmente si se asocia trastorno del ánimo.
]]> VenlafaxinaHa demostrado su eficacia en dolor neuropático postmastectomía y polineuropatía diabética, donde fue más eficaz y con mayor tolerancia que los tricíclicos (32).
Duloxetina
Ha sido aprobada por la FDA para dolor neuropático diabético e incontinencia de esfuerzo. También ha resultado ser útil en fibromialgia, dolor lumbar crónico y artrosis (33).
Aunque tiene menos efectos cardiovasculares y anticolinérgicos, las interacciones farmacológicas son todavía una duda con estos fármacos.
Puede tener interacciones con inhibidores de CYP1A como fluoroquinolonas y cimetidina, con CYP2D6 inhibidores como quinidina y ritonavir y con CYP2D6 como metoprolol, propafenona, codeína, dextrometorfano, mexiletina, ondasentron y tramadol.
Además se precisa precaución en pacientes con hepatitis, HTA, convulsiones, glaucoma y DM.
Las contraindicaciones son enfermedad renal terminal, enfermedad hepática, glaucoma y asociación con IMAOS.
Los resultados de NNT en 3 análisis randomizados controlados con duloxetina 60 mg y placebo fueron entre 5,2 y 4,9 y NNH entre 17 y 8,8.
Antiepilépticos
]]> Los antiepilépticos inhiben la excitación neuronal y estabilizan las membranas mediante el bloqueo de canales iónicos nerviosos.Se utilizan en dolor neuropático, como fármacos de primera línea en monoterapia o junto con antidepresivos. Los más utilizados son gabapentina, pregabalina y carbamacepina, aunque también lamotrigina o lacosamida han mostrado utilidad en el dolor neuropático del anciano.
Gabapentina
Es el antiepiléptico más estudiado en dolor neuropático de distintos tipos (DPN, NPH, TGN, síndrome de dolor regional complejo, postmastectomía, oncológico y miembro fantasma).
En DPN a dosis superiores a 900 mg/día resultó no inferior a 75 mg de amitriptilina.
Los efectos secundarios más frecuentes se relacionan con su efecto en SNC: somnolencia, sedación, nistagmo, temblor y ataxia, así como ganancia de peso y edema.
La gabapentina puede aumentar sus niveles si se asocia con morfina o naproxeno y disminuirlos asociado con antiácidos.
Especial precaución se debe tener en pacientes con insuficiencia renal ajustando a 1.200 mg/día para 30-59 de aclaramiento, 600 mg para 15 a 29 y 300 para menos de 15 ml/min.
En la Tabla II se presentan los NNT y NNH de estos fármacos.
Pregabalina
]]> Es el antiepiléptico aprobado más recientemente para dolor neuropático de DPN, NPH y central.Tiene una biodisponibilidad oral del 90 %, con escasa unión a proteínas plasmáticas y no inhiben enzimas mayores CYP450, lo que le confiere menos interacciones y efectos secundarios. No obstante, la asociación con otros psicofármacos puede tener efectos en SNC. También la asociación con tiazolidinediona aumenta el peso y el edema.
La eliminación renal hace que sea preciso su ajuste en nefrópatas.
Consigue el efecto analgésico de forma más precoz y entre los efectos adversos puede aparecer euforia, vértigo y edema.
No se debe suspender bruscamente por riesgo de náuseas, diarrea e insomnio.
La Cochrane 2009 concluye que no hay evidencia para uso de pregabalina en dolor nociceptivo.
No obstante, 19 estudios con 7.003 pacientes concluyen que es eficaz para neuralgia postherpética, diabética, dolor neuropático central y fibromialgia (30).
El 18-28 % de pacientes abandonaron el tratamiento.
La pregabalina y la gabapentina son de elección en ancianos por su perfil de seguridad
Carbamacepina
]]> Se considera de primera elección en TGN y de segunda línea en el resto de dolor neuropático. La oxcarbacepina se tolera mejor.Ambas, carbamacepina y oxcarbacepina, tienen riesgo de hiponatremia y SIADH, especialmente problemático en ancianos.
La carbamacepina bloquea los canales de sodio y calcio y conlleva más efectos secundarios (mareo, fatiga, náuseas, arritmias, diplopía y prurito).
Todos los antiepilépticos precisan ajuste según función renal, excepto lamotrigina y tiagabina.
En disfunción hepática se prefiere gabapentina, pregabalina y levetiracetam (30).
Analgésicos tópicos
La FDA ha aprobado fórmulas de capsaicina, diclofenaco y lidocaína.
No hay estudios de alta calidad controlados sobre estos agentes, aunque pueden ser beneficiosos.
Sólo existe evidencia sobre la aplicación tópica de AINE, lidocaína y capsaicina.
]]> La naturaleza regional y periférica de la neuralgia postherpética es susceptible de tratar con terapia local como parche o como crema.Apósito de lidocaína al 5 %
Es un coanalgésico con una escasa absorción sistémica de lidocaína.
Inhibe la nocicepción periférica actuando sobre las fibras nerviosas A y C, bloqueando los canales de sodio sobreexcitados.
Si se asocia a pregabalina se consigue mayor alivio con menos dosis.
La lidocaína parche 5 % ha demostrado, en varios estudios randomizados, eficacia y seguridad para tratar la alodinia de la neuralgia postherpética (NNT: 2) (34) (así como head to head con pregabalina).
También ha demostrado, en un estudio de seguimiento de un año, buena tolerancia hasta el punto de poder recomendarse como primera elección en dolor neuropático localizado y en otras neuropatías, como túnel carpiano o combinado con otros (gabapentina).
Capsaicina
Es un alcaloide natural derivado de la guindilla que, de forma tópica, depleciona la sustancia P de las terminaciones nerviosas periféricas o centrales.
La crema de capsaicina al 0,025 y 0,075 resultaba muy irritante y mal tolerada.
]]> Recientemente se dispone de un parche al 8 % indicado para dolor neuropático no diabético.Un estudio controlado, randomizado de capsaicina 8 % parche demostró reducción significativa en dolor con una bajada media de las escalas del 29,6% respecto al 19,9 % del control. Los efectos adversos se relacionaban con la aplicación: eritema y dolor (35).
AINE tópicos
AINE tópicos, como diclofenaco, estudiado en 19 doble ciegos con 3.000 pacientes, algunos con enfermedad reumática y artrosis, demuestran consistentemente eficacia sobre dolor y función respecto a placebo (36). Los estudios han mostrado que diclofenaco tópico permanece al principio en el lugar de aplicación (dermis y tejido celular subcutáneo), aliviando el dolor sin efectos adversos sistémicos, pero además se distribuye preferentemente al líquido sinovial más que al plasma, dejando concentraciones terapéuticas en los tejidos "objetivo de tratamiento".
La eficacia es comparable a fórmulas orales de diclofenaco, ibuprofeno y naproxeno, pero con menos efectos gastrointestinales.
Conclusiones
El manejo del dolor en el anciano precisa de un conocimiento específico de los fármacos, de sus características farmacocinéticas y farmacodinámicas y de la relaciones entre éstas y el tipo de paciente anciano, con características diferentes en el paciente frágil. Al objetivo de aliviar el dolor, se debe sumar el de evitar yatrogenia (Tabla III) (30).
]]>
Bibliografía
1. Viloria Jiménez A. Opioides en el anciano: mitos y realidades. En: Guía de buena práctica Clínica en Geriatría. Dolor crónico en el anciano. Madrid: Sociedad Española de Geriatría y Gerontología; 2012. p. 57-75. [ Links ]
2. Sullivan MD, Von Korff M, Banta-Green C, Merrill JO, Saunders K. Problems and concerns of patients receiving chronic opioid therapy for chronic non-cancer pain. Pain 2010;149(2):345-53. DOI: 10.1016/j.pain.2010.02.037. [ Links ]
3. Pepin JF. The marginalization of chronic patients on chronic opioid therapy. Pain Physician 2009;12:493-8. [ Links ]
4. Barber JB, Gibson SJ. Treatment of chronic non-malignant pain in the elderly. Safety considerations. Drug safety 2009;32(6):457-74. DOI: 10.2165/00002018-200932060-00003. [ Links ]
5. Dahan A, Yassen A, Bijl H, Romberg R, Sarton E, Teppenma L, et al. Comparison of the respiratory effects of intravenous buprenorphine and fentanyl in humans and rats. Br J Anaesth 2005;94:825-34. DOI: 10.1093/bja/aei145. [ Links ]
6. Morrison RS, Magaziner J, Gilbert M, Koval KJ, McLaughlin MA, Orosz G, et al. Relationship between pain and opioid analgesics on the development of delirium following hip fracture. J Gerontol A Biol Sci Med Sci 2003;58(1):76-81. DOI: 10.1093/gerona/58.1.M76. [ Links ]
7. Takkouche B1, Montes-Martínez A, Gill SS, Etminan M. Psychotropic medications and the risk of fracture: A meta-analysis. Drug Saf 2007;30(2):171-84. DOI: 10.2165/00002018-200730020-00006. [ Links ]
8. Dublin S, Walker RL, Jackson ML, Nelson JC, NS Weiss, Korff M, et al. Use of opioids or benzodiazepines and risk of pneumonia in older adults: A population-based case-control study. Journal of the American Geriatrics Society 2011;(59(10):1899-907. DOI: 10.1111/j.1532-5415.2011.03586.x DOI: 10.1111/j.1532-5415.2011.03586.x. [ Links ]
9. Hollingshead J, Dühmke RM, Cornblath DR. Tramadol para el dolor neuropático (Revisión Cochrane traducida). En: La Biblioteca Cochrane Plus, número 4. Oxford: Update Software Ltd.; 2008. Disponible en: http://www.update-software.com. (Traducida de The Cochrane Library, 2008 Issue 3. Chichester, UK: John Wiley & Sons, Ltd. [ Links ]).
10. Mercadante S, Arcuri E. Pharmacological management of cancer pain in the elderly. Drugs Aging 2007;24:761-76. DOI: 10.2165/00002512-200724090-00004. [ Links ]
11. White SM, Rashid N, Chakladar A. An análisis of renal dysfunction in 1511 patients with fractured neck of fémur: The implications for perioperative analgesia. Anaesthesia 2009;64(10):1061-5. DOI: 10.1111/j.1365-2044.2009.06012.x. [ Links ]
12. Baillie SP, Bateman DN, Coates PE, Woodhouse KW. Age and the pharmacokinetics of morphine. Age Ageing 1989;18(4):258-62. DOI: 10.1093/ageing/18.4.258. [ Links ]
13. Lötsch J, von Hentig N, Freynhagen R, Griessinger N, Zimmermann M, Doehring A, et al. Cross-sectional analysis of the influence of currently known pharmacogenetic modulators on opioid therapy in outpatient pain centers. Pharmacogenet Genomics 2009;19(6):429-36. DOI: 10.1097/FPC.0b013e32832b89da. [ Links ]
14. Levron. Pharmacokinetics of transdermal fentanyl: the effect of age John Libbey Eurotext. Translation from French; 1992. p. 199-203. [ Links ]
15. Ariano RE, Duke PC, Sitar DS Population pharmacokinetics of fentanyl in healthy volunteers. J Clin Pharmacol 2001;41(7):757-63. DOI: 10.1177/00912700122010663. [ Links ]
16. Solassol I, Bressolle F, Caumette L, García F, Poujol S, Culine S, et al. Inter- and intraindividual variabilities in pharmacokinetics of fentanyl after repeated 72-hour transdermal applications in cancer pain patients. Ther Drug Monit 2005;27(4):491-8. DOI: 10.1097/01.ftd.0000160717.50704.42. [ Links ]
17. Menten J, Desmedt M, Lossignol D, Mullie A. Longitudinal follow-up of TTS-fentanyl use in patients with cancer-related pain: Results of a compassionate-use study with special focus on elderly patients. Curr Med Res Opin 2002;18(8):488-98. DOI: 10.1185/030079902125001272. [ Links ]
18. Wouter Zuurmond. Transdermal fentanyl shows a similar safety and efficacy profile in elderly and non-elderly patients with cander pain. Annals of Oncology 2002; 13(10) (Suppl. 5): 171. [ Links ]
19. Clark AJ, Ahmedzai SH, Allan LG, Camacho F, Horbay GL, Richarz U, et al. Efficacy and safety of transdermal fentanyl and sustained-release oral morphine in patients with cancer and chronic non-cancer pain. Curr Med Res Opin 2004;20(9):1419-28. DOI: 10.1185/030079904X2114. [ Links ]
20. Hand CW, Sear JW, Uppington J, Ball MJ, McQuay HJ, Moore RA. Buprenorfine disposition in patients with renal impairment: Single and continuos doping with special referente to metabolitos. Br J Anaesth 1990;64(3):276-8. DOI: 10.1093/bja/64.3.276. [ Links ]
21. Kress HG. Clinical update on the pharmacology, efficacy and safety of transdermal buprenorphine. Eur J Pain 2009;13(3):219-30. DOI: 10.1016/j.ejpain.2008.04.011. [ Links ]
22. Muriel Villoria C, Pérez-Castejón Garrote JM, Sánchez Magro I, Neira Alvarez M. Effectiveness and safety of transdermal buprenorphine for chronic pain treatment in the elderly: A prospective observational study. Med Clin (Barc) 2007;128(6):204-10. DOI: 10.1157/13098717. [ Links ]
23. Griessinger, Sittl R, Likar R. Transdermal buprenorphine in clinical practice - a post-marketing surveillance study in 13,179 patients. Current Medical Research and Opinion Aug 2005;21(8):1147-56. DOI: 10.1185/030079905X53315. [ Links ]
24. Kaiko RF, Benziger DP, Fitzmartin RD, Burke BE, Reder RF, Goldenheim PD. Pharmacokinetic-pharmacodynamic relationships of controlled-release oxycodone. Clin Pharmacol Ther 1996;59(1):52-61. DOI: 10.1016/S0009-9236(96)90024-7. [ Links ]
25. Lange B, Kuperwasser B, Okamoto A, Steup A, Häufel T, Ashworth J, et al. Efficacy and safety of tapentadol prolonged release for chronic osteoarthritis pain and low back pain. Adv Ther 2010;27(6):381-99. DOI: 10.1007/s12325-010-0036-3. Epub 2010 Jun 11. DOI: 10.1007/s12325-010-0036-3. Epub 2010 Jun 11. [ Links ]
26. Quingley C. Hidromorfona para dolor agudo y crónico. Biblioteca Cochrane Plus (revisión Cochrane traducida). n.o 3; 2007. DOI: 10.1136/bmj.39153.682454.FA. [ Links ]
27. Somogyi AA, Barratt DT, Coller JK. Pharmacogenetics of opioids. Clin Pharmacol Ther 2007;81:429-44. [ Links ]
28. Furlan AD, Reardon R, Weppler C. Opioids for chronic noncancer pain: A new Canadian practice guideline. CMAJ 2010;182(9):923-30. Epub 2010 May 3 National Disease and Therapeutic Index (NDTI). http://www.ndti.org DOI: 10.1503/cmaj.100187. [ Links ]
29. Pergolizzi J, Böger RH, Budd K, Dahan A, Erdine S, Hans G, et al. Opioids and the management of chronic severe pain in the elderly: Consensus statement of an International Expert Panel with focus on the six clinically most often used World Health Organization Step III opioids (buprenorphine, fentanyl, hydromorphone, methadone, morphine, oxycodone). Pain Pract 2008;8(4):287-313. doi: 10.1111/j.1533-2500.2008.00204.x. Epub 2008 May 23. DOI: 10.1111/j.1533-2500.2008.00204.x. Epub 2008 May 23. [ Links ]
30. Reisner L. Pharmacological management of persistent pain in older persons. The Journal of pain 2011;12(3) Suppl 1:S21-S29. [ Links ]
31. Saarto T, Wiffen PJ. Antidepressants for neuropathic pain. Cochrane Database Syst Rev 2007;(4):CD005454. [ Links ]
32. Saarto T, Wiffen PJ. Antidepressants for neuropathic pain: A Cochrane review. J Neurol Neurosurg Psychiatry 2010;81:1372-3. DOI: 10.1136/jnnp.2008.144964. [ Links ]
33. Duloxetine (Cymbalta) for chronic musculoskeletal pain. Med Lett Drugs Ther 2011;53:33. [ Links ]
34. Kahlid W, Alam S, Purin N. Topical lidocaine for the treatment of postherpetic neuralgia. Cochrane Database Syst Rev 2007;18;(2):CD004846. [ Links ]
35. Backonja M, Wallace MS, Blonsky ER, Cutler BJ, Malan P Jr, Rauck R, et al. NGX-4010, a high-concentration capsaicin match, for the treatment of postherpetic neuralgia: A randomised, double-blind study. Lancet Neurol 2008;7:1106-12. DOI: 10.1016/S1474-4422(08)70228-X. [ Links ]
36. Zacher J, Altman R, Bellamy N, Brühlmann P, Da Silva J, Huskisson E, et al. Topical diclofenac and its role in pain and inflammation: An evidence-based review. Curr Med Res Opin 2008;24:925-50. DOI: 10.1185/030079908X273066. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
María del Pilar Sáez López
pisalop@gmail.com