Obesidad, inflamación e insulino-resistencia: papel de los ligandos del receptor gp 130
Obesity, inflammation and insulin resistance: role of gp 130 receptor ligands
B. Marcos-Gómez1, M. Bustos2, J. Prieto2, J. A. Martínez1, M. J. Moreno-Aliaga1
1. Departamento de Ciencias de la Alimentación, Fisiología y Toxicología. Facultad de Farmacia. Universidad de Navarra. Pamplona.
2. Área de Terapia Génica y Hepatología. Centro de Investigación Médica Aplicada (CIMA). Universidad de Navarra. Pamplona.
Dirección para correspondencia
]]>
RESUMEN
La obesidad puede ser considerada como una patología inflamatoria crónica de bajo grado, caracterizada por una elevación de los niveles plasmáticos de citoquinas proinflamatorias como el factor de necrosis tumoral alfa (TNF-a), y proteínas reactantes de fase aguda como la proteína C reactiva. En este contexto, algunas de las citoquinas de la familia de interleuquina (IL-6) han sido también implicadas en el proceso inflamatorio asociado a obesidad y enfermedades relacionadas. Además de IL-6, pertenecen a esta familia citoquinas como IL-11, ciliary neurotrophic factor (CNTF), cardiotrophin-1 (CT-1), cardiotrophin- like cytokine (CLC), leukemia inhibitory factor (LIF) y oncostatin M (OsM). Todas ellas ejercen sus acciones biológicas mediante la interacción con un complejo receptor del que forma parte una molécula glicoproteica transductora de la señal denominada glicoproteína 130 (gp130), por lo que también se denominan citoquinas gp130.
Sin embargo, su papel en obesidad y sus complicaciones es controvertido; así, mientras que algunas han sido implicadas en el desarrollo de obesidad y enfermedades relacionadas como enfermedad hepática, insulino-resistencia y patología cardiovascular, otros estudios han llevado a proponer a los ligandos del receptor gp130 como potenciales agentes terapéuticos para el tratamiento de la obesidad y sus patologías asociadas. De hecho, el tratamiento con CNTF ha demostrado ser efectivo en la reducción del peso corporal, promoviendo la inhibición de la ingesta, la activación del gasto energético y la sensibilidad a la insulina. En esta revisión se analiza el potencial terapéutico de algunas de las citoquinas ligando del receptor gp130 en procesos de obesidad y enfermedades relacionadas.
Palabras clave. Obesidad. Inflamación. Insulino-resistencia. Citoquinas gp130. Interleuquina-6. CNTF.
ABSTRACT
Obesity can be considered as a low grade inflammatory disease, characterized by increased plasma levels of proinflammatory cytokines such as tumoral necrosis factor-a (TNF-a), and acute phase reactant proteins like C-reactive protein.
In this context, some cytokines of the interleukin-6 (IL-6) family have been involved in the inflammatory processes associated to obesity. In addition to IL-6, the IL-6 cytokine family includes IL-11, ciliary neurotrophic factor (cntf), cardiotrophin-1 (CT-1), cardiotrophin-like cytokine (CLC), leukemia inhibitory factor (LIF) y Oncostatin M (OsM). These proteins are also known as gp130 cytokines because all of them exert their action via the glycoprotein 130 (gp130) as a common transducer protein within their functional receptor complexes. However, their role in obesity and related disorders is controversial; thus, whereas some studies have described the involvement of gp130 cytokines in the development of obesity and its related cluster of pathophysiologic conditions like insulin-resistance, fatty liver and cardiovascular diseases, other trials have proposed the gp130 receptor ligands as therapeutic targets in the treatment of obesity and its related disorders. In fact, CNTF treatment has demonstrated to be effective in the reduction of body weight, by promoting the inhibition of food intake and the activation of the energy expenditure, together with an improvement of insulin sensitivity.
This review analyzes the potential therapeutic role of some of the gp130 ligands in obesity and related diseases.
Introducción
La obesidad es un serio problema de salud pública que ha alcanzado proporciones epidémicas en muchos países desarrollados. Además, la prevalencia de las patologías cardiovasculares está directamente relacionada con el alarmante incremento de las tasas de obesidad y sus consiguientes alteraciones metabólicas como la resistencia insulínica y las dislipemias1. El coste económico-sanitario de la obesidad y sus comorbilidades es considerable, y demandará la utilización de una proporción cada vez mayor de los recursos sanitarios en los próximos años, a menos que esta tendencia pueda ser revertida.
El aumento de la ingesta y el seguimiento de hábitos alimentarios poco saludables, junto con el estilo de vida sedentario de nuestras sociedades desarrolladas han contribuido, sin duda, a la gran expansión de la obesidad. Sin embargo, esta incidencia epidémica de la obesidad no puede atribuirse únicamente a los factores ambientales, y se ha sugerido un papel relevante de la carga genética en la susceptibilidad al desarrollo de obesidad2. En este sentido, algunos estudios han descrito que una parte de la población es más sensible al desarrollo de obesidad inducida por un alto consumo de grasa. Las bases genéticas y moleculares que subyacen a esta susceptibilidad al desarrollo de obesidad y sus complicaciones asociadas no están claras.
Obesidad e inflamación
Durante los últimos años, varios estudios han sugerido que la obesidad se asocia a un proceso inflamatorio. De hecho, se ha considerado a la obesidad como una patología inflamatoria crónica de bajo grado, caracterizada por una elevación los niveles plasmáticos de citoquinas proinflamatorias como el factor de necrosis tumoral alfa (TNF-a), la interleuquina 6 (IL-6) y proteínas reactantes de fase aguda tales como la proteína C reactiva (PCR)3. Un hecho importante en el estado inflamatorio asociado con la obesidad es que parece estar predominantemente provocado, y residir en el tejido adiposo blanco (TAB), aunque otros órganos claves del metabolismo también puedan estar implicados en el curso de la inflamación.
Algunas citoquinas inflamatorias (TNF-a, IL-6, IL-1b, IL-8, IL-18) son expresadas y secretadas por el tejido adiposo. Así, la ingesta excesiva de nutrientes, algunas infecciones y el estrés oxidativo pueden provocar un aumento en los niveles de secreción de estas citoquinas que conducen a la inflamación crónica en tejido adiposo blanco favoreciendo la activación e infiltración de macrófagos maduros. De hecho, varios estudios han demostrado que el incremento en la secreción de citoquinas como el TNF-a puede estimular a los preadipocitos y a las células endoteliales a producir MCP-1, atrayendo a los macrófagos al tejido adiposo. Una vez infiltrados en el tejido adiposo, los macrófagos maduros comienzan a secretar citoquinas y quimioquinas tales como TNF-a, IL-1, IL-6, y MCP-1. Este patrón de secreción, junto con el producido por adipocitos y otros tipos celulares, puede perpetuar un círculo vicioso de reclutamiento de macrófagos y producción de citoquinas inflamatorias, llevando a una inflamación primaria local en el tejido adiposo. Posteriormente, estas citoquinas secretadas por el tejido adiposo podrían desencadenar el aumento de la producción de proteínas inflamatorias en el hígado y conducir así a la inflamación sistémica de bajo grado observada en obesidad4.
Además, este estado inflamatorio asociado con la obesidad ha sido propuesto como nexo de unión con varios desórdenes asociados a la misma como la resistencia a la insulina, las dislipemias y las complicaciones vasculares y hepáticas4 conduciendo al denominado Síndrome Metabólico Cardiovascular1. Así, varios estudios han confirmado que la presencia de inflamación predice el futuro desarrollo de diabetes tipo 2. Auque esta correlación se ha demostrado a nivel clínico, se conoce poco la relación a nivel molecular y fisiológico entre la inflamación y la resistencia insulínica inducida por obesidad.
]]> Junto con el tejido adiposo, el músculo esquelético y el hígado desempeñan un papel clave en el metabolismo de la glucosa dependiente de insulina. El paso más importante en la cascada de señalización de la insulina es la autofosforilación del receptor de la insulina (IR). Tras ello se produce la fosforilación de la tirosina del sustrato 1 del receptor de la insulina (IRS-1). En este sentido, se ha demostrado que TNF-a causa un descenso moderado en la autofosforilación del IR estimulada por insulina y un dramático descenso en la fosforilación del IRS-1, sugiriendo un importante papel del TNF-a en el desarrollo de resistencia a insulina. Además, cuando la actividad del TNF-a se bloquea, bioquímica o genéticamente, el resultado es una mejoría en la sensibilidad a insulina. Asimismo, también se ha demostrado que la IL-6 desequilibra la señalización de insulina tanto en adipocitos como en hepatocitos.El aumento de lipólisis estimulada por citoquinas observado en TAB en los sujetos obesos podría ser otra pieza del rompecabezas. El posterior incremento de los ácidos grasos libres circulantes y el incremento de los metabolitos derivados de ácidos grasos intracelulares se han relacionado con el desarrollo de resistencia insulínica en el músculo esquelético y en el hígado sugiriendo que los ácidos grasos libres pueden ser un importante eslabón entre la inflamación crónica del tejido adiposo y la resistencia insulínica sistémica.
La arteriosclerosis, uno de los mayores componentes del síndrome metabólico, se ha descrito también como una enfermedad inflamatoria crónica caracterizada por la activación de mecanismos proinflamatorios y la acumulación de monocitos y macrófagos en la capa íntima junto con la infiltración de lípidos. Además, niveles altos de marcadores de inflamación, como la PCR e IL-6, se han asociado con elevado riesgo de desarrollo de arteriosclerosis y sus complicaciones como el infarto agudo de miocardio.
Asimismo, también la alta concentración de ácidos grasos en plasma podría tener un papel en el desarrollo de la arteriosclerosis. Además, se ha demostrado que la elevación de los ácidos grasos libres induce la inflamación y desequilibra la reactividad vascular en sujetos sanos. Por otra parte, se ha observado que la infusión de dosis bajas de insulina en pacientes con infarto agudo de miocardio produce una reducción en la inflamación, sugiriendo que la insulina posee a la vez acciones anti-inflamatorias y anti-aterogénicas. Por ello, se ha propuesto como posible mecanismo para explicar la conexión entre inflamación y arterioesclerosis, ya que la resistencia a insulina podría facilitar un estado proinflamatorio por el descenso en los efectos anti-inflamatorios y anti-ateroscleróticos de la insulina5.
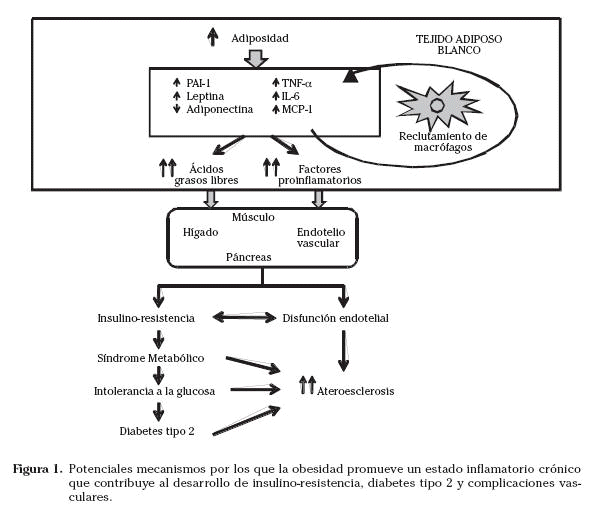
La figura 1 esquematiza los potenciales mecanismos por los que la obesidad promueve un estado inflamatorio crónico que contribuye al desarrollo de insulino-resistencia, diabetes tipo 2 y complicaciones vasculares.
Aunque el estado inflamatorio asociado a obesidad se ha considerado una consecuencia de la misma, algunos estudios recientes han sugerido que la susceptibilidad a desarrollar obesidad y resistencia insulínica pudiera ser secundaria a un estado proinflamatorio4.
Sin embargo, no puede olvidarse que las citoquinas como TNF-a, IL-1, IL-6, IL-15, IL-12 y IL-18 están también implicadas en el proceso anorexigénico mediado por la inflamación. Todas ellas disminuyen el peso corporal y la masa grasa cuando son administradas a roedores.
Citoquinas ligando del receptor gp130 y obesidad
]]> Teniendo en cuenta todo lo expuesto anteriormente resulta por tanto controvertido el papel que las distintas citoquinas puedan jugar en la susceptibilidad o prevención de obesidad. En concreto, en esta revisión se analiza el papel de algunas de las principales citoquinas gp130 o también llamadas citoquinas de la familia de interleuquina (IL-6), en procesos de obesidad y enfermedades relacionadas. Además de la propia IL-6, forman parte de esta familia otras citoquinas como IL-11, ciliary neurotrophic factor (CNTF), cardiotrophin-1 (CT-1), cardiotrophin-like cytokine (CLC), leukemia inhibitory factor (LIF) y oncostatin M (OsM)6. Todas ellas ejercen sus acciones biológicas mediante la interacción con un complejo receptor del que forma parte una molécula glicoproteica transductora de la señal denominada glicoproteína 130 (gp130).Esta familia de citoquinas puede ser subdividida en dos grandes grupos según qué receptores de señalización se encuentren incorporados en el complejo final. El primer grupo de citoquinas gp130 incluye IL-6 e IL-11, ambas requieren la asociación con un receptor a específico previo al paso de unión con los homodímeros de gp130. El segundo grupo de citoquinas gp130 necesita la heterodimerización del receptor gp130 con un segundo receptor de señalización, LIFRb. Este grupo representa el mayor grupo de citoquinas gp130 e incluye CNTF, CT-1, CLC, LIF y OsM. Se ha demostrado que CNTF, CT-1 y CLC primero necesitan unirse al receptor especifico a, el cual aunque no participa en la señalización per se induce la formación del heterodímero gp130 con LIFRb. Además, Schuster y colaboradores7 mostraron que la especificidad del receptor a para cada citoquina anteriormente comentada quedaba controvertida al demostrar que CNTF puede señalizar vía CNTFRa/gp130/LIFRb o vía IL-6a/gp130/LIFRb, además CLC utiliza CNTFRa como receptor a8. Finalmente, las citoquinas LIF y OsM directamente inducen la formación del heterodímero gp130/ LIFRb. Por otro lado, se ha descrito que la OsM humana puede señalizar independientemente de LIFRb, dimerizando su propio receptor OsmR con gp130 (Fig. 2).
El papel de las citoquinas de la familia de IL-6 en obesidad y sus complicaciones es controvertido; así, mientras que algunas de las citoquinas de la familia de IL-6 han sido implicadas en el desarrollo de procesos de obesidad y enfermedades relacionadas como enfermedad hepática, insulino-resistencia y patología cardiovascular, otros estudios han llevado a proponer a los ligandos del receptor gp130 como potenciales agentes terapéuticos para el tratamiento de la obesidad y sus patologías asociadas8. Esto derivaría del hecho de que las citoquinas gp130 señalizan a través de un receptor que tiene muchas similitudes con la señalización de la leptina, la cual promueve la inhibición de la ingesta, la activación del gasto energético y la sensibilidad a la insulina9.
La participación de la citoquina IL-6 en estos procesos es una de las más ampliamente estudiadas, y se puede encontrar en la literatura gran controversia en los resultados obtenidos tal como lo describen Kristiansen y colaboradores10. Cabe resaltar que la producción y niveles circulantes de IL-6 se relacionan positivamente con distintos indicadores de adiposidad, como el peso, el índice de masa corporal (IMC) y el perímetro de cintura-cadera, mientras que la pérdida de peso provoca una disminución en los niveles plasmáticos de IL-6 en personas obesas11. Además, son múltiples los estudios tanto in vitro como in vivo que demuestran la capacidad de IL-6 para inducir resistencia a la insulina. De hecho, los niveles elevados de IL-6 se consideran indicadores de riesgo de síndrome metabólico, ya que como inductor de inflamación, parece estar relacionada con las alteraciones lipídicas y vasculares, que acompañan a la resistencia a la insulina.
Teniendo en cuenta estas observaciones parece lógico sugerir que la deficiencia de IL-6 tendría un efecto protector sobre la obesidad y sus complicaciones asociadas. Sin embargo, diversos estudios en ratones deficientes en IL-6 han arrojado resultados discrepantes. Así, mientras que algunos han observado que estos ratones no presentan obesidad, ni hiperglucemia ni metabolismo lipídico anormal tanto cuando son jóvenes como en la edad adulta12, otros han descrito que la deficiencia de IL-6 provoca una mayor susceptibilidad a desarrollar obesidad, insulino-resistencia e hígado graso en la edad adulta, lo cual era parcialmente revertido por la administración de IL-613.
En apoyo de este potencial efecto beneficioso de IL-6, otros trabajos han sugerido también que en algunas circunstancias IL-6 puede activar vías que promueven el gasto energético y la sensibilidad a la insulina, y por tanto la función de IL-6 en la determinación de la sensibilidad a la insulina es controvertida10. Así, en varios estudios recientes se ha observado que la IL-6, al igual que la leptina, es capaz de activar AMPK tanto en músculo esquelético como en tejido adiposo14. La activación de AMPK en el hígado conduce a una estimulación de la oxidación de ácidos grasos e inhibición de lipogénesis, producción de glucosa y síntesis de proteínas. El interés clínico de AMPK ha crecido debido a la demostración de que AMPK podría mediar algunos de los efectos de la adiponectina y de drogas antidiabéticas como metfomina y thiazolidinedionas. Actualmente, se tiene la idea de que la activación farmacológica de AMPK puede proporcionar a través de su señalización y efectos en la expresión de genes, una nueva estrategia para el tratamiento de las alteraciones metabólicas unidas a diabetes tipo 2 y obesidad15. La activación de AMPK en músculo e hígado limita el depósito de grasa. De esta forma, AMPK mantiene la respuesta a la insulina en el hígado y músculo. Así pues, en concordancia con su capacidad de activar AMPK, se ha demostrado la capacidad de IL-6 para incrementar la oxidación de grasa in vitro, ex vivo, y en humanos in vivo. Además, la inactivación de AMPK mediante siRNA o un adenovirus dominante negativo bloquea los efectos de IL-6 sobre la oxidación de grasas8. Sin embargo, y a pesar de estos efectos, el tratamiento con IL-6 recombinante no puede considerarse como una terapia adecuada para la obesidad debido a sus propiedades proinflamatorias, especialmente en el hígado16.
La citoquina CNTF ha demostrado también tener un potencial terapéutico en situaciones de obesidad, insulino-resistencia e hígado graso, mejorando todos estos parámetros17. Sus acciones antiobesidad derivan en parte de sus acciones anorexígenas centrales. En este sentido, se ha demostrado que tanto el receptor de CNTF (CNTFRa) como el receptor de leptina (LRb) están localizados en la región hipotalámica del cerebro involucrada en la regulación del balance energético. Así, CNTF, al igual que la leptina, es capaz de poner en marcha la señalización anorexigénica neuronal, ya que su administración sistémica ejerce las mismas acciones que la leptina en las neuronas del núcleo arqueado, siendo capaz de producir hipofagia, y pérdida de peso en modelos de obesidad (ob/ob) y de resistencia a la leptina (db/db y dieta alta en grasa).
Las neuronas de los núcleos arqueados del hipotálamo representan, al parecer, un lugar de convergencia para muchas de las señales nerviosas y periféricas que regulan los depósitos energéticos. Estos núcleos contienen dos tipos de neuronas muy importantes en la regulación del apetito y del consumo energético: las neuronas POMC (proopiomelanocortina), cuya estimulación reduce la ingesta y aumenta el consumo energético, y las neuronas NPY-AGRP cuya activación tiene efectos opuestos. El lugar exacto de acción de CNTF en el núcleo arqueado ha sido recientemente identificado mediante la utilización de ratones gp130∆POMC, con una deleción selectiva del receptor gp130 en las neuronas POMC del núcleo arqueado. Cuando estos ratones gp130 POMC fueron alimentados con una dieta normal o una dieta alta en grasa mostraron un fenotipo normal, sugiriendo que el CNTF endógeno no juega un papel en el balance energético. Sin embargo, las acciones centrales observadas tras la administración de CNTF recombinante estaban anuladas en los ratones gp130∆POMC, sugiriendo que las acciones hipotalámicas de CNTF requieren la activación del circuito de las neuronas POMC.
Además, se ha observado que la acción central de CNTF está mediada vía inhibición de AMPK, al igual que ocurre en alguna de las acciones centrales de la leptina, ya que tanto la administración intraperitoneal como la inyección intracerebroventricular de CNTFAx15 disminuyen la actividad AMPKa2 en el núcleo arqueado, reduciendo la ingesta energética y el peso corporal en los animales alimentados con una dieta control o con una dieta alta en grasa18. En resumen, CNTF y sus análogos parecen activar específicamente neuronas POMC en el núcleo arqueado y disminuir la activación de AMPK.
]]> Por otra parte, se ha confirmado además que el tratamiento con CNTFAx15 no solo era capaz de corregir el fenotipo obeso en modelos de resistencia a la leptina, sino que sus efectos se mantenían varios días después de finalizar el tratamiento. Este hallazgo sugirió que el modo de acción de CNTF no se producía solo a través de la activación del complejo CNTFRa/gp130Rb/LIFRb. Kokoeva y colaboradores19 demostraron recientemente que la administración central de CNTF provoca una proliferación celular en el hipotálamo de ratones, en concreto en la región del cerebro que contiene neuronas como las de la propiomelanocortina (POMC) y el Neuropeptido Y (NPY), que se sabe poseen un papel en la regulación del balance energético. Estas nuevas neuronas serían capaces de responder a la leptina en el hipotálamo, haciendo al cerebro más sensible a los compuestos que modulan las neuronas de POMC y NPY, incluso tras el cese del tratamiento. Esta neurogénesis hipotalámica inducida por CNTF fue prevenida por la coadministración de un bloqueador mitótico, y fue acompañada de una ganancia de peso de rebote8.Sin embargo, no puede ignorarse que el crecimiento de nuevas células en el sistema nervioso central podría conducir a efectos secundarios adversos que pudieran limitar la eficacia del tratamiento. Existe además, cierta ambigüedad sobre si CNTF o el tratamiento con CNTFAx15 pudiera causar una respuesta pro-inflamatoria en el sistema nervioso central, ya que algunos estudios han observado el desarrollo de fiebre así como sobreexpresión de genes pro-inflamatorios tras su administración8.
Además de los efectos centrales de CNTF, varios estudios tanto in vivo como in vitro han sugerido que CNTFAx15 podría prevenir la ganancia de peso, incrementando el gasto energético independientemente de sus efectos en la ingesta energética, actuando sobre tejidos periféricos tales como el adiposo pardo y blanco, así como el músculo esquelético. Con el fin de demostrar que las acciones de CNTF sobre el metabolismo tienen lugar a nivel periférico y no solo central, Watt y colaboradores20 trataron ratones con CNTF tanto por vía intraperitoneal como intracerebroventricular, observándose un incremento en la fosforilación de STAT3 y la actividad AMPK en músculo esquelético sólo cuando se administró por vía intraperitoneal y no intracerebroventricular. Además, demostraron que CNTF fue capaz de incrementar la oxidación en el músculo esquelético a través de un mecanismo dependiente de AMPK, ya que la infección de células musculares con un adenovirus AMPK dominante negativo suprimió el efecto de CNTF sobre el aumento en la oxidación grasa.
Esto pone de manifiesto que los efectos antiobesogénicos de CNTF en la periferia resultan de sus efectos directos sobre el músculo esquelético. Además, se ha observado que estos efectos periféricos no se ven suprimidos ni en modelos genéticos ni dietéticos de obesidad con resistencia a la leptina.
Este estudio reciente ha aumentado el interés en la posibilidad del uso de CNTF o sus análogos como tratamiento de la obesidad21, y también ha descubierto un posible mecanismo por el cual las citoquinas ligandos del receptor gp130 podrían vencer la resistencia a la leptina. Además, se ha observado que el tratamiento de ratones con CNTF atenuó fuertemente la acumulación de lípidos en el músculo esquelético inducida por una dieta alta en grasa20. De hecho, la acumulación intramuscular de triacilglicerol, diacilglicerol y ceramida fue revertida a niveles similares a los observados en los ratones alimentados con una dieta control. La acumulación de metabolitos lipídicos en los tejidos periféricos se correlaciona con resistencia a la insulina. Así, la producción de metabolitos de ácidos grasos en los tejidos sensibles a la insulina activa una serie de quinasas incluyendo la PKC-q, Ik quinasa y JAK, que han mostrado dañar la transducción de la señal y la acción de la insulina in vivo. El tratamiento con CNTF podría atenuar la lipotoxicidad resultante de la activación de las cascadas de serina quinasa inflamatorias. En este sentido, el tratamiento de ratas con CNTFAx15 durante dos horas de infusión lipídica restauró la acción de la insulina tanto en el hígado como en el músculo esquelético20. Además, el tratamiento agudo con CNTF fue capaz de prevenir la activación de JNK inducida por la acumulación lipídica en el músculo esquelético y de JNK y NF-kB en el hígado. Este efecto fue asociado con una baja deposición de grasa en esos tejidos, confirmando previas observaciones por las cuales CNTF puede atenuar la esteatosis hepática17.
Además, se ha descrito también un incremento en la tasa metabólica basal de los ratones db/db que fueron tratados con CNTFAx15, así como un incremento en los niveles de expresión de ARNm de UCP-1 en el tejido adiposo pardo. Esta última observación es compatible con el hallazgo de que CNTF puede incrementar los niveles de expresión de ARNm de Ppargc1a, y prevenir la disminución inducida por una dieta alta en grasa de su proteína codificada, PPARg coactivador 1a (PGC-1a), en el músculo esquelético20. Varios estudios han implicado la etiología de la insulino-resistencia y la diabetes tipo 2 con una respuesta mitocondrial defectuosa, secundaria a una disminución de la expresión génica de PGC-1a.
Así pues, aunque es todavía especulativo, una de las acciones antiobesigénicas de las citoquinas ligandos del receptor gp130 podría ocurrir vía el incremento de los niveles de PGC-1a mediado por las AMPK y con el consecuente incremento en la biogénesis mitocondrial.
En resumen, además de las acciones anorexigénicas centrales de CNTF y sus análogos, estas citoquinas son capaces también de mejorar la acción de la insulina y promover la oxidación de lípidos en los tejidos periféricos (por la acción directa en estos tejidos). Esto ha llevado a proponer a esta citoquina como posible tratamiento para obesidad y enfermedades relacionadas21; sin embargo, el entusiasmo del potencial terapéutico de esta citoquina es controvertido debido a que algún estudio ha observado su capacidad para producir reacción inflamatoria y febril. Además, ensayos clínicos en fase II en humanos sugieren que la eficacia de CNTFAx15 como tratamiento parece limitada, ya que los pacientes que fueron tratados con altas dosis de la droga mostraron nauseas o desarrollaron anticuerpos anti-CNTFAx15.
Respecto a las acciones de otras citoquinas de la familia de IL-6 y CNTF en la fisiopatología de la obesidad y sus complicaciones asociadas existen pocos estudios, y algunos describen resultados poco concluyentes. Así, respecto a la Oncostatina M, estudios in vitro han observado que reduce la adipogénesis e induce desdiferenciación de adipocitos, pero se ha descrito también su capacidad de disminuir la producción de leptina e incrementar la de PAI-1, lo que contribuiría a un mayor riesgo cardiovascular22.
Un estudio reciente ha mostrado que los niveles circulantes de cardiotrofina-1 se correlacionan positivamente con los de glucosa plasmática, y que se encuentran elevados en pacientes con síndrome metabólico23. Sin embargo, varios estudios han descrito la capacidad protectora de CT-1 frente al daño hepático24, 25. El tratamiento periférico con LIF provoca una reducción de la masa grasa en ratones ovariectomizados26.
]]> En conclusión, teniendo en cuenta el potencial terapéutico que los ligandos del receptor gp130 pudieran presentar para el tratamiento de la obesidad y enfermedades relacionadas, resulta de gran interés profundizar en el estudio de las acciones de otras citoquinas de esta familia en la prevención/tratamiento de estas patologías. Resultarían de gran interés aquellas que fueran capaces de activar el receptor gp130b solamente en la periferia, y no presentasen las complicaciones descritas para la IL-6 y el CNTF a nivel central.
Bibliografía
1. Rana JS, Nieuwdorp M, Jukema JW, Kastelein JJ. Cardiovascular metabolic syndrome - an interplay of, obesity, inflammation, diabetes and coronary heart disease. Diabetes Obes Metab 2007; 9: 218-232. [ Links ]
2. Moreno-Aliaga MJ, Santos JL, Marti A, Martinez JA. Does weight loss prognosis depend on genetic make-up? Obes Rev 2005; 6: 155-168. [ Links ]
3. Das UN. Is obesity an inflammatory condition? Nutrition 2001; 17: 953-966. [ Links ]
4. Moreno-Aliaga MJ, Campion J, Milagro F, Berjon A, Martinez JA. Adiposity and proinflammatory state: the chicken or the egg Adipocytes 2005; 1: 1-13. [ Links ]
5. Dandona P, Aljada A, Bandyopadhyay A. Inflammation: the link between insulin resistance, obesity and diabetes. Trends Immunol 2004; 25: 4-7. [ Links ]
6. Pennica D, Shaw KJ, Swanson TA, Moore MW, Shelton DL, Zioncheck KA et al. Cardiotrophin-1. Biological activities and binding to the leukemia inhibitory factor receptor/gp130 signaling complex. J Biol Chem 1995; 270: 10915-10922. [ Links ]
7. Schuster B, Kovaleva M, Sun Y, Regenhard P, Matthews V, Grötzinger J et al. Signaling of human ciliary neurotrophic factor (CNTF) revisited. The interleukin-6 receptor can serve as an alpha-receptor for CTNF. J Biol Chem 2003; 278: 9528-9535. [ Links ]
8. Febbraio MA. gp130 receptor ligands as potential therapeutic targets for obesity. J Clin Invest 2007; 117: 841-849. [ Links ]
9. Flier JS. Obesity wars: Molecular progress confronts an expanding epidemic. Cell 2004; 116: 337-350. [ Links ]
10. Kristiansen OP, Mandrup-Poulsen T. Interleukin-6 and diabetes: the good, the bad, or the indifferent? Diabetes 2005; 54 (Suppl 2): S114-124. [ Links ]
11. Goyenechea E, Parra MD, Martínez Hernández JA. Implicación de la IL-6 y su polimorfismo -174G>C en el control del peso corporal y en las complicaciones metabólicas asociadas a la obesidad. An Sist Sanit Navar 2005; 28: 357-366. Review. Spanish. [ Links ]
12. Di Gregorio GB, Hensley L, Lu T, Ranganathan G, Kern PA. Lipid and carbohydrate metabolism in mice with a targeted mutation in the IL-6 gene: absence of development of age-related obesity. Am J Physiol Endocrinol Metab 2004; 287: 182-187. [ Links ]
13. Wallenius V, Wallenius K, Ahren B, Rudling M, Carlsten H, Dickson SL et al. Interleukin-6-deficient mice develop mature-onset obesity. Nat Med 2002; 8: 75-79. [ Links ]
14. Carey AL, Steinberg GR , Macaulay SL, Thomas WG, Holmes AG, Ramm G et al. Interleukin-6 increases insulin-stimulated glucose disposal in humans and glucose uptake and fatty acid oxidation in vitro via AMP-activated protein kinase. Diabetes 2006; 55: 2688-2697. [ Links ]
15. Viollet B, Foretz M, Guigas B, Horman S, Dentin R, Bertrand et al. Activation of AMP-activated protein kinase in the liver: a new strategy for the management of metabolic hepatic disorders. J Physiol 2006; 574: 41-53. [ Links ]
16. Klover PJ, zimmers TA, Koniaris LG, Mooney RA. Chronic exposure to interleukin-6 causes hepatic insulin resistance in mice. Diabetes 2003; 52: 2784-2789. [ Links ]
17. Sleeman MW, Garcia K, Liu R, Murray JD, Malinova L, Moncrieffe M et al. Ciliary neurotrophic factor improves diabetic parameters and hepatic steatosis and increases basal metabolic rate in db/db mice. Proc Natl Acad Sci U S A 2003; 100: 14297-14302. [ Links ]
18. Steinberg GR, Watt MJ, Fam BC, Proietto J, Andrikopoulos S, Allen AM et al. Ciliary neurotrophic factor suppresses hypothalamic AMP-kinase signaling in leptin-resistant obese mice. Endocrinology 2006; 147: 3906-3914. [ Links ]
19. Kokoeva MV, Yin H, Flier JS. Neurogenesis in the hypothalamus of adult mice: potential role in energy balance. Science 2005; 310: 679-683. [ Links ]
20. Watt MJ, Dzamko N, Thomas WG, Rose-John S, Ernst M, Carling D et al. CNTF reverses obesity-induced insulin resistance by activating skeletal muscle AMPK. Nat Med 2006; 12: 541-548. [ Links ]
21. Ahima, RS. Overcoming insulin resistance with CNTF. Nat Med 2006; 12: 511-512. [ Links ]
22. Miyaoka Y, Tanaka M, Naiki T, Miyajima A. Oncostatin M inhibits adipogenesis through the RAS/ERK and STAT5 signaling pathways. J Biol Chem 2006; 281: 37913-37920. [ Links ]
23. Natal C, Fortuno MA, Restituto P, Colina MI, Diez J, Varo N. Cardiotrophin-1 Is Expressed in Adipose Tissue and It Is up-Regulated in the Metabolic Syndrome. Am J Physiol Endocrinol Metab 2007; 294: E52-60. [ Links ]
24. Iniguez M, Berasain C, Martinez-Anso E, Bustos M, Fortes P, Pennica D et al. Cardiotrophin-1 defends the liver against ischemia-reperfusion injury and mediates the protective effect of ischemic preconditioning. J Exp Med 2006; 203: 2809-2815. [ Links ]
25. Marques JM, Belza I, Holtmann B, Pennica D, Prieto J, Bustos M. Cardiotrophin-1 is an essential factor in the natural defense of the liver against apoptosis. Hepatology 2007; 45: 639-648. [ Links ]
26. Jansson JO, Moverare-SkrticA S, Berndtsson I, Wernstedt H, Carlsten H, Ohlsson C. Leukemia inhibitory factor reduces body fat mass in ovariectomized mice. Eur J Endocrinol 2006; 154: 349-354. [ Links ]
]]>
![]() Dirección para correspondencia:
Dirección para correspondencia:
María Jesús Moreno Aliaga
Departamento de Ciencias de la Alimentación,
Fisiología y Toxicología
Facultad de Farmacia. Universidad de Navarra
Tfno. 948 425600
E-mail: mjmoreno@unav.es