Efecto del quitosán de alto peso molecular y del alginato de sodio sobre la hidrofobicidad y adhesión de Candida albicans a células
Effect of the high molecular weight chitosan and sodium alginate on Candida albicans hydrophobicity and adhesion to cells
Ana Isabel Azcurra1, Silvina Ruth Barembaum1, María Alejandra Bojanich1, Silvia Edith Calamari2,
Javier Aguilar3, Luis José Battellino4, Susana Tereza Dorronsoro5
(1) Jefe de Trabajos Prácticos Cátedra de Introducción a la Química y Física Biológicas, Facultad de Odontología
(2) Profesor Adjunto Cátedra de Introducción a la Química y Física Biológicas, Facultad de Odontología ]]>
(3) Jefe de Trabajos Prácticos, Instituto de Virología Varella, Facultad de Ciencias Médicas
(4) Profesor Titular Cátedra de Química Biológica, Facultad de Odontología
(5) Profesor Titular Cátedra de Introducción a la Química y Física Biológicas, Facultad de Odontología,
Universidad Nacional de Córdoba, Argentina
Dirección para correspondencia
RESUMEN
Objetivo: Evaluar el efecto del quitosán de alto peso molecular (QAPM) y del alginato de sodio (NaAL) sobre la hidrofobicidad superficial de Candida albicans y la adhesión de esta levadura a células epiteliales y fibroblastos de distinto origen.
Diseño del estudio: Para el estudio de la hidrofobicidad, las levaduras (n=7) se hicieron crecer en agar glucosado de Sabouraud suplementado con QAPM o NaAL o en ausencia de los mismos (controles). La determinación de la hidrofobicidad se realizó por el método de adhesión a hidrocarburos utilizando dos solventes orgánicos (xileno y cloroformo). En los estudios de adhesión, las levaduras se pusieron en contacto con soluciones de biopolímeros y luego se enfrentaron a diferentes células (fibroblastos humanos y de rata y células epiteliales Hep-2). La cuantificación se realizó por microscopía óptica. ]]>
Resultados: Se observó una disminución del 44% de la hidrofobicidad en presencia de QAPM y del 82%, con NaAL, o del 30% con QAPM y 19% con NaAL, cuando los solventes orgánicos empleados fueron cloroformo o xileno, respectivamente. La adhesión de C. albicans a células epiteliales y fibroblastos humanos disminuyó significativamente con ambos biopolímeros. En el caso de los fibroblastos de encía de rata, sólo se observó una disminución con NaAL. En ninguno de los experimentos se observaron diferencias significativas en asociación al tipo de fibroblasto empleado.
Conclusiones: Los biopolímeros resultaron efectivos en la reducción de la hidrofobicidad y la adhesión de C. albicans a células, las cuales son importantes factores de virulencia relacionados con la colonización de los tejidos blandos del hospedador o superficies acrílicas presentes en el sistema estomatognático.
Palabras clave: Candida albicans, quitosán, alginato, adhesión, hidrofobicidad.
ABSTRACT
The aim of the present paper is to evaluate the effect of the high molecular weight chitosan (HMWC) and of sodium alginate (NaAL) on surface hydrophobicity of Candida albicans and on adhesion of the yeast to epithelial cells and fibroblasts of different proceeding.
For this study, a collection strain and seven isolates of C. albicans from saliva (patients with denture stomatitis) were grown in Sabouraud glucose agar supplemented with HMWC or NaAL or in absence of them (control). Hydrophobicity was determined by adhesion to hydrocarbons method using two organic media (xylene and chloroform). For adhesion experiments, aqueous suspensions of yeasts were contacted with solutions of biopolymers and different cells (rat and human fibroblasts and epithelial cells Hep-2). The quantification of adhesion was made by optical microscopy.
Results: a decrease in hydrophobicity was observed in the presence of HMWC (44%) and of NaAL (82%) when chloroform was employed as organic medium, meanwhile the decreases were of 30% with HMWC and 19% with NaAL in the presence of xylene. Adhesion of C. albicans to epithelial cells and human fibroblasts decreased significantly with both biopolymers. In the case of rat fibroblasts, a decrease was observed only with NaAL. None of experiments showed significant differences associated to fibroblast type.
Conclusions: biopolymers showed effectiveness in reducing hydrophobicity and adhesion of C. albicans to cells, which are important virulence factors related to colonization of the soft tissues of host or acrylic surfaces present in the oral system.
Key words: Candida albicans, chitosan, alginate, adhesion, hydrophobicity.
]]> Introducción
El desarrollo de nuevos materiales de uso en odontología, tanto para la prevención como para el tratamiento de las enfermedades bucales, se ha incrementado en los últimos años. Entre ellos se encuentran, el quitosán de alto peso molecular (QAPM), polímero catiónico proveniente de la quitina, utilizado como un vehículo de liberación controlada de fármacos, con propiedad osteoconductora y con acción sobre la proliferación de fibroblastos (1-4) y el alginato de sodio (NaAL), copolímero aniónico, que se emplea como material para la impresión dental (5,6). Además, ambos materiales biocompatibles son utilizados en aplicaciones biomédicas.
La estomatitis protética, causada principalmente por la especie C. albicans, puede observarse en un alto porcentaje de la población portadora de prótesis dental (7,8). El desarrollo de la infección depende de diversos factores, como la interacción tipo proteína proteína entre Candida y las células del hospedador, la morfología de la levadura (blastoconidia o micelio) y el estado inmunológico del hospedador (9). La capacidad de adhesión a superficies plásticas y a tejidos blandos constituye un factor de virulencia que predomina en C. albicans respecto a otras especies de Candida. Los estudios de adhesión fúngica utilizan como soporte células epiteliales bucales, líneas celulares y diferentes materiales plásticos (10,11). En dicho proceso participan distintas fuerzas, siendo la hidrofobicidad de la superficie celular (HSC) una de las más importantes (12). Diferentes métodos se han utilizado para determinar la HSC; el más empleado por su simplicidad es el de adhesión a hidrocarburos (13,14). Factores como la temperatura, el tiempo de interacción, el pH, la fuerza iónica, la concentración relativa de las especies interactuantes y el carácter ácido-base del solvente orgánico empleado en la determinación, modifican esta HSC.
El propósito de este trabajo ha sido evaluar el efecto de QAPM y NaAL sobre la HSC y la adhesión de C. albicans a células epiteliales y fibroblastos.
Material y métodos
Aislamiento e identificación de Candida:
Se utilizaron cepas de C. albicans de colección (ATCC 10231) y cepas autóctonas aisladasde saliva sin estimular de pacientes con estomatitis protética (n = 7) asistidos en la Cátedra de Prostodoncia III, Facultad de Odontología, Universidad Nacional de Córdoba (UNC), con consentimiento por escrito. En ningún caso se empleó saliva de pacientes que usaron antimicóticos en forma sistémica por un período de 7 a 10 días previos al examen, fármacos xerostomizantes o medicación prolongada con antiinflamatorios. El aislamiento se realizó en medio específico de agar glucosado de Sabouraud con cloranfenicol al 1% (Britania, Argentina). Todos los aislamientos se identificaron bioquímicamente mediante pruebas de fermentación de azúcares (Candifast, International Microbio, Francia) y la identificación se completó mediante estudio micromorfológico sobre agar harina de maíz y prueba de producción del tubo germinativo (15).
Preparación de las levaduras para el ensayo de hidrofobicidad de la superficie celular (HSC)
Una vez aisladas e identificadas, las levaduras fueron crecidas por 24-48 h a 37 ºC en agar glucosado de Sabouraud sin polímero (control) y en medios suplementados con QAPM 0,05 g% (90% deacetilado, 280 cps, PM 300 kDa, Unifarma Argentina) y NaAL 0,2 g% (420 cps, Kimitsu, Chile). Dichas concentraciones sub-inhibitorias de los polímeros fueron determinadas previamente en las mismas condiciones de crecimiento recién descritas.
]]> Determinación de la HSC: método de adhesión a hidrocarburos:El procedimiento consistió en enfrentar las suspensiones de levadura en buffer salino de fosfato (PBS) (Absorbancia 520 nm = 0,400) a fases orgánicas diferentes, xileno o cloroformo, en una relación de volúmenes de 5:1; la mezcla se agitó durante 1 min y se dejó reposar 10 min. La HSC se calculó en base a la absorbancia de la fase acuosa a 520 nm antes y después de enfrentar la suspensión de C. albicans a la fase orgánica (13).
Preparación de las levaduras para el ensayo de adherencia:
Las levaduras fueron crecidas en agar glucosado de Sabouraud 24-48 h a 37 ºC y luego se inocularon en caldo glucosado de Sabouraud 16 a 18 h a 37 ºC. Se lavaron en dos ciclos de centrifugación (400 rpm, 5 min) con PBS estéril y la suspensión final fue de 1 x 107 células/ ml en PBS. El número de células se ajustó mediante recuento en cámara hematológica de Neubauer.
Condiciones de crecimiento y preparación de las células
a) Cultivo celular de fibroblastos humanos y línea epitelial:
Se usaron fibroblastos provenientes de prepucio de bebé (PH) y línea celular humana (Hep2, ATCC CCl 23 ) proveniente de carcinoma de faringe, donados por el Centro de Estudios Médicos e Investigaciones Clínicas (CEMIC) de Buenos Aires y el Instituto de Virología, Dr. Varella, UNC, respectivamente. Para los cultivos se utilizó el medio MEM Eagle (Gibco, USA) con 10% de suero fetal bovino y 50 mg/ml de gentamicina. El cultivo se lavó dos veces con PBS (pH 7,4) y se disgregó con tripsinaEDTA al 0,05%, se agregó nuevamente medio de cultivo y la suspensión final fue de 1 x 105 células / ml. Se añadieron 100 ml de dicha suspensión a una cubeta de 24 pocillos, se lo dejó crecer durante 24 h previo al ensayo de adherencia, a 37 ºC en estufa con CO2 al 5% y 100% de humedad (16).
b) Cultivo primario de fibroblastos de encía de rata:
Se utilizaron tres ratas Wistar machos de 3 a 5 semanas de vida (200 a 300 g) como donantes de fibroblastos gingivales (FR). Posterior a la anestesia, se extrajo tejido conectivo de la encía superior e inferior, según criterios de Freshney (16). Las muestras fueron lavadas tres veces con PBS estéril pH 7,2, y el tejido conectivo fue seccionado en porciones muy pequeñas, cultivadas en placas de Petri con medio MEM Eagle, suplementado con 20% de suero fetal bovino, y mantenidas a 37 ºC en una estufa con aire húmedo y CO2 5%. Se dejó crecer el cultivo entre 10 y 14 días o hasta tener un cultivo confluente (17). Los fibroblastos se cosecharon con tripsina al 0,05%, se centrifugaron y se resuspendieron en medio de cultivo a una concentración de 1 x 105 cel / ml.
Ensayo de Adherencia:
]]> Las células fueron lavadas con PBS y tratadas con saliva inactivada (30 min a 60 °C) durante 1 h a 37 °C. Se controló que todos los cultivos estuvieran libres de levaduras adheridas después del contacto con la saliva mediante la observación microscópica de los extendidos. Se agregaron simultáneamente la suspensión de C. albicans y los biopolímeros en estudio (QAPM 0,25% P/V en ácido acético al 1% y NaAL 0,10% P/V en H2O destilada estéril) (18,19); las muestras fueron incubadas por 1 h a 37 °C, secadas al aire, fijadas con metanol y coloreadas con cristal violeta. Se utilizó para el control el mismo procedimiento sin la inclusión de los biopolímeros. La cuantificación de C. albicans adheridas a las células se realizó por microscopía óptica (400 x) (n=150) en tres campos al azar. Las imágenes fueron analizadas mediante un sistema de análisis de imágenes (Image Pro Plus 4.0 Media Cybernetics v. 2002, USA). No se cuantificaron campos en los que las levaduras adheridas a células estuvieran agregadas entre sí (18). Los ensayos se realizaron por triplicado y en tres momentos diferentes.Análisis estadístico: los datos fueron procesados estadísticamente mediante MANOVA (hidrofobicidad), ANOVA y test LSD-Fisher (adhesión) para cada ensayo y procesados con el paquete estadístico SPSS 10.0. Se fijó un valor de p ≤ 0,05 para determinar diferencias significativas.
Resultados
Hidrofobicidad de la superficie celular
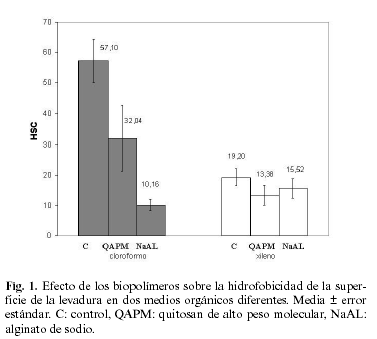
La figura 1 muestra el efecto de los biopolímeros sobre la HSC de las levaduras, observándose una disminución significativa en relación al control (p = 0,025) con ambos solventes orgánicos (44% con QAPM y 82% con NaAL en cloroformo, y 30% con QAPM y 19% con NaAL, en xileno).
Las levaduras crecidas en presencia de QAPM y NaAL no mostraron diferencias significativas entre sí en los valores de HSC para ambos solventes. La HSC de las levaduras control fue significativamente mayor con cloroformo que con xileno (p = 0,001). Los valores obtenidos en presencia de los biopolímeros no se modificaron significativamente al variar la fase orgánica.
Ensayo de Adherencia:
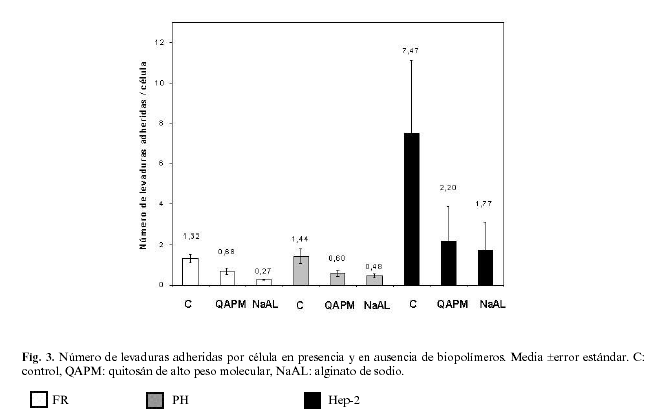
En la figura 2 se observa que para todos los tipos de células, los controles muestran mayor número de levaduras adheridas (Figura 2: A-I, B-I y C-I) que las células tratadas con NaAL (Figura 2: A-II,B-II,C-II) y QAPM (Figura 2: A-III, B-III, C-III). La adherencia de C. albicans a PH y a la línea Hep-2 disminuyó significativamente con QAPM y NaAL respecto al control (p < 0,05). Al comparar el número de C. albicans adheridas a FR, sólo se observaron diferencias estadísticamente significativas entre NaAL y control, pero no entre los dos biopolímeros. Tampoco se detectaron diferencias al evaluar los Resultados entre los dos tipos de fibroblastos (figura 3).
]]>
Discusión
La adhesión de C. albicans a las superficies del hospedador es considerada la etapa inicial para la candidiasis. Ésta es un proceso complejo que involucra factores biológicos, químicos y fuerzas intervinientes en la adhesión; entre ellas, las de tipo hidrofóbicas juegan un rol importante. La HSC, factor de virulencia para el proceso de adhesión fúngica, no debe analizarse puramente desde lo termodinámico (12) debido a que diversas estructuras microbianas también contribuyen a la misma, tales como proteínas de membrana, lipoproteínas, fosfolípidos y lipopolisacáridos (20). En la bibliografía, el método de adhesión a hidrocarburos empleando xileno como fase orgánica es el más utilizado (13,21). En este solvente de carácter neutro, las levaduras se adhieren solamente a través de interacciones hidrófobas, mientras que con cloroformo, se suman las interacciones de tipo ácido-base, por ser aceptor electrónico, y la superficie microbiana, donante electrónica; esto determina valores mayores de HSC (14). Nuestros Resultados concuerdan con dichas diferencias. Cuando las muestras fueron tratadas con QAPM y NaAL, la HSC disminuyó con respecto al control, tanto al usar cloroformo como xileno. Esto se debería a las condiciones de cultivo, que modificarían la estructura de la pared fúngica, y por lo tanto, la carga superficial (21). Estos hallazgos sugerirían que las interacciones ácido-base contribuyen a la acción antifúngica de estos polímeros.
Los estudios referidos a la adhesión fúngica a diferentes superficies muestran que Candida posee numerosas adhesinas, entre las que se encuentran el receptor CR3, homólogo a la integrina humana, mananoproteínas que pueden interactuar con moléculas similares a lectinas de las células epiteliales, el receptor CR2, que promueve la adherencia a superficies acrílicas (22,23) y receptores para proteínas inmovilizadas de la película salival (24). La adhesión se ve favorecida por traumatismos, maceración u oclusión de la mucosa, como ocurre en la estomatitis protética (10). En este trabajo se demostró una mayor adhesión a células epiteliales que a fibroblastos, lo cual estaría asociado a un mayor número de receptores en las primeras. La disminución de la adhesión de Candida producida por los biopolímeros podría interpretarse como resultado de modificaciones de la carga superficial del hongo (25) y de las células por las características físico-químicas de los polímeros. También habría que considerar el posible bloqueo de los receptores de la levadura y de las células por la viscosidad propia de estos compuestos (19). Estos Resultados son congruentes con los obtenidos de HSC, reforzando la correlación que existe entre estos factores de virulencia. El mayor efecto observado para NaAL se debería a las propiedades mecánicas del propio gel, sumadas a las modificaciones que produciría sobre las superficies de las células en estudio.
El tratamiento de la candidiasis oral resulta más sencillo en los pacientes con inmunodeficiencia leve, en los que generalmente los antifúngicos tópicos resultan eficaces. Éstos actúan sobre la síntesis del ergosterol de la membrana celular del hongo o sobre enzimas que regulan la síntesis de los ácidos nucleicos, pero interfieren en las vías metabólicas de las células humanas. Sin embargo, se observan formas clínicas de candidiasis oral crónica resistentes al tratamiento o bien efectos colaterales indeseables (26). Una alternativa en el tratamiento es el uso de QAPM y NaAL, solos o asociado, que ha sido empleado para la preparación de microcápsulas adhesivas para la liberación controlada de fármacos en la mucosa bucal, como también se ha informado un efecto inhibitorio por si mismo sobre el crecimiento fúngico y la adhesión de C. albicans a células epiteliales (27-29). La disminución de HSC y adhesión a superficies biológicas en presencia de estos productos producirían una disminución del potencial patogénico del hongo (21).
Las propiedades bioadhesivas del quitosán y alginato de sodio y su uso como liberadores de drogas intraorales (27) así como la inhibición de la adhesión a células bucales y efectos antifúngicos no específicos del quitosán (29) permitirían considerar a estos productos como una alternativa terapéutica para la estomatitis protética con una mejor aceptación del paciente y una disminución de los efectos colaterales de los tratamientos antifúngicos convencionales.
Bibliografía
]]>1. Gerentes P, Vachoud L, Doury J, Domard A. Study of chitin based gel as injectable material in periodontal surgery. Biomaterials 2002; 23:1295-02. [ Links ]
2. Liu H, Du Y, Yang J, Zhu H. Structural characterization and antimicrobial activity of chitosan/betaine derivative complex. Carbohydr Polymers 2004; 55: 2917. [ Links ]
3. Muzzarelli R. Biochemical significance of exogenous chitin and chitosans in animal and patients. Carbohydr Polymers 1993; 20:7-16. [ Links ]
4.Fakhry A, Schneider GB, Zaharias R, Senel S. Chitosan supports the initial attachment and spreading of osteoblasts preferentially over fibroblasts. Biomaterials 2004;25:2075-9. [ Links ]
5. Draget KI, Skjak-Braek, Smirsrod O. Alginate based new materials. Int J Biol Macromol 1997;21:47-55. [ Links ]
6. Flanagan DA, Palenik CJ, Setcos JC, Miller CH. Antimicrobial activities of dental impression materials. Dental Materials 1998;14:399-04. [ Links ]
7. Delgado W, Aguirre JM. Las micosis orales en la era del SIDA. Rev Iberoam Micol 1997;14:14-22. [ Links ]
8. Baena-Monroy T, Moreno-Maldonado V, Franco-Martínez F, Aldape-Barrios B, Quindós G, Sánchez-Vargas LO. Candida albicans, Staphylococcus aureus and Streptococcus mutans colonization in patients wearing dental prosthesis. Med Oral Patol Oral Cir Bucal 2005;10:E27-E39. [ Links ]
9. Cannon RD, Holmes AR, Mason AB, Monk BC. Oral Candida: clearance, colonization or candidiasis?. J Dent Res 1995;74:1152-61. [ Links ]
10. Samaranayake LP, Mac Farlane TW. Factors affecting the in vitro adherence of the fungal oral pathogen Candida albicans to epithelial cells of human origin. Arch Oral Biol 1982;22:869-73. [ Links ]
11. San Millán R, Elguezabal N, Regúlez P, Moragues MD, Quindós G, Pontón J. Effect of salivary secretory IgA on the adhesion of Candida albicans to polystyrene. Microbiology 2000;146:2105-12. [ Links ]
12. Doyle RJ. Contribution of the hydrophobic effect to microbial infection. Microb Infect 2000;2:391-400. [ Links ]
13. Gallardo Moreno AM, Garduño AE, Gonzalez Martin ML, Pérez Giraldo C, Bruque JM, Gómez García AC. Analysis of the hydrophobic behavior of different strains of Candida parapsilopsis under two growth temperatures. Colloids Surf B Biointerfaces 2003;28:119-26. [ Links ]
14. Bellon-Fontaine MN, Rault J, van Oss CJ. Microbial adhesion to solvents: a novel method to determine electron-donor/electron-acceptor or Lewis acid-base properties of the microbial cells. Colloids Surf B Biointerfaces 1996;7:147-53. [ Links ]
15. Nota técnica. Medios de cultivo caseros para la identificación de hongos de interés médico. Rev Arg Micol 1994;17:26-33. [ Links ]
16. Freshney RI. Culture of Animal Cells: A Manual of Basic Techniques, New York: Alan R. Liss Inc. Editores; 1987. p. 57-84; p. 107-126. [ Links ]
17. Simain Sato F, Lahmouzi J, Kalykakis GK, Heinen E, Defrensne MP, De Pauw MC et al. Culture of gingival fibroblasts on bioabsorbable regenerative materials in vitro. J Periodontol 1999;70:1234-9. [ Links ]
18. Kimura LH, Pearsall NN. Relationship between germination of Candida albicans and increased adherence to human buccal epithelial cells. Infect Immun 1980;28:464-8. [ Links ]
19. Barembaum S, Virga C, Bojanich A, Cornejo S, Calamari S, Pontón J et al. Efecto de QAPM y alginato de sodio sobre la adherencia de Candida albicans autóctonas a células epiteliales bucales (in vitro). Med Oral 2003;8:188-96. [ Links ]
20. Egusa H, Ellepola An, Nikawa H, Hamada T, Samaranayake LP. Sub- therapeutic exposure to polyene antimycotics elicits a post-antifungal effect and depresses the cell surface hydrophobicity of oral Candida albicans isolates. J Oral Pathol Med 2000;29:206-13. [ Links ] [ Links ]
22. Crocket DN, OGrady JF, Reade PC. Candida species and Candida albicans morphotypes in erythematous candidiasis. Oral Surg Oral Med Oral Pathol 1992;73:559-63. [ Links ]
23. Chakir J, Côté L, Coulombe C, Deslauriers N. Differential pattern of infection and immune response during experimental oral candidiasis in BALB/C and DBA/2 (H-2d) mice. Oral Microbiol Immunol 1994;9: 88-94. [ Links ]
24. Sullivan JM, Jenkinson HF, Cannon RD. Adhesion of Candida albicans to oral streptococci is promoted by selective adsorption of salivary proteins to the streptococcal cell surface. Microbiol 2000;146:41-8. [ Links ]
25. Singleton DR, Masuoka J, Hazen KC. Surface hydrophobicity changes of two Candida albicans serotype B mnn4delta mutants. Eukaryot Cell 2005;4:639-48. [ Links ]
26. Quindós G, Ribacoba L, Contreras I, Aguirre JM. Tratamiento de las candidiasis orofaríngeas. Rev Iberoam Micol 1996;13: 511-15. [ Links ]
27. Miyazaki S, Nakayama A, Oda M, Takada M, Attwood D. Chitosan and sodium alginate based bioadhesive tablets for intraoral delivery. Biol Pharm Bull 1994;17:745-7. [ Links ]
28. Giunchedi P, Juliano C, Gabbini E, Cossu M, Sorrenti M. Formulation and in vivo evaluation of chlorhexidine buccal tablets prepared using drug-loaded chitosan microspheres. Eur J Pharm and Biopharm 2002;53:233-9. [ Links ]
29. Knapczyk J,Macura AB, Pawlik B. Simple tests demonstrating the antimycotic effect of chitosan. International Journal of Pharmaceutics 1992;80:33-8. [ Links ]
]]>
![]() Dirección para correspondencia
Dirección para correspondencia
Dra. Ana Isabel Azcurra
Departamento de Biología Bucal,
Facultad de Odontología, Universidad Nacional de Córdoba.
Haya de la Torre S/N. Ciudad Universitaria,
Casilla Postal 4, 5000-Córdoba, Argentina.
E-mail: azcurra@fcq.unc.edu.ar
Recibido: 6-05-2005
Aceptado: 4-01-2006