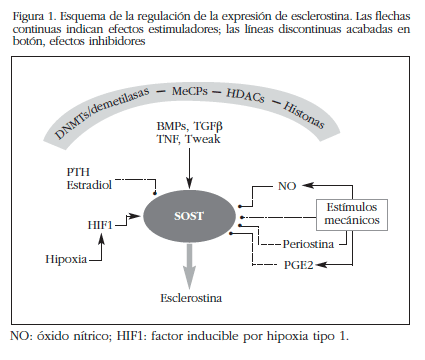
Avances en el estudio de los mecanismos involucrados en la modulación de la expresión de esclerostina en células humanas
Advances in the study of the mechanisms involved in the modulation of the expression of sclerostin in human cells
Delgado-Calle J.1, Pérez-Campo F.M.2 y Riancho J.A.2
1 Departamento de Anatomía y Biología Celular - Facultad de Medicina de Indiana - Centro Médico de Administración de Veteranos Roudebush - Indianapolis (EE.UU. )
2 Departamento de Medicina Interna - Hospital Universitario Marqués de Valdecilla - Universidad de Cantabria - IDIVAL - Santander (España)
Trabajo premiado con la beca investigación FEIOMM 2011.
]]> Dirección para correspondencia
RESUMEN
Objetivos: La esclerostina desempeña un papel importante en la regulación del metabolismo óseo, como queda demostrado por los cambios dramáticos en la masa ósea que se producen cuando se inhibe su actividad mediante anticuerpos monoclonales. Sin embargo, aún no se conocen bien los mecanismos que regulan su expresión. Varios estudios han demostrado una asociación entre polimorfismos del promotor del gen SOST (que codifica la esclerostina) y la densidad mineral ósea. Asimismo, el grado de metilación de una isla CpG próxima al inicio de la transcripción se asocia a cambios marcados en la expresión del gen. Por tanto, parece que la producción de esclerostina está influida tanto por mecanismos genéticos como epigenéticos, además de otros factores hormonales y mecánicos. Un mejor conocimiento de los mismos no sólo contribuirá a entender mejor la biología ósea, sino que puede abrir nuevas oportunidades terapéuticas.
Palabras clave: esclerostina, SOST, metilación, epigenética.
SUMMARY
Sclerostin plays an important role in the regulation of bone metabolism, as is shown in the dramatic changes in bone mass which occur when its activity is inhibited by means of monoclonal antibodies. However, the mechanisms which regulate its expression are still not well-understood. Various studies have shown an association between polymorphisms of the SOST gene promoter (which codes for sclerostin) and bone mineral density. Also, the degree of methylation of a CpG island near the start of the transcription is associated with marked changes in the expression of the gene. Therefore, it appears that the production of sclerostin is influenced by both genetic and epigenetic mechanisms, in addition to other hormonal and mechanical factors. A greater knowledge of these mechanisms would not only contribute to a better understanding of bone biology, but could open up new therapeutic opportunities.
Key words: sclerostin, SOST, methylation, epigenetic.
]]> Introducción
La esclerostina es una proteína codificada por el gen SOST. Esta proteína es segregada específicamente por los osteocitos y tiene un efecto negativo sobre la formación ósea, a través de la inhibición de la vía Wnt canónica1. La inhibición de esta vía tiene profundas consecuencias sobre la actividad de los osteoblastos; en concreto, se inhibe su diferenciación y se induce su apoptosis2,3. La importancia de la esclerostina en la biología ósea se ha puesto de manifiesto por la descripción de casos de mutaciones del gen SOST en humanos que provocan un fenotipo óseo alterado, con una masa ósea aumentada4,5. Por otro lado, la inhibición de la esclerostina mediante el uso de anticuerpos neutralizantes ha demostrado tener un potente efecto anabólico óseo, tanto en animales como en humanos6,7.
Aunque la importancia de la esclerostina en la homeostasis ósea parece indudable, son varios los aspectos de su biología que aún permanecen desconocidos. Algunos de los aspectos peor conocidos son los factores que regulan la expresión de esclerostina y los mecanismos implicados. Por un lado, se desconoce por qué únicamente los osteocitos, y no otras células de estirpe osteoblástica, son capaces de expresar esclerostina. Aún si cabe más intrigante resulta el hecho de que dentro del hueso existen osteocitos que producen esclerostina, mientras que otros situados a unas pocas micras de ellos no lo hacen8.
En algunos modelos experimentales se han identificado varios efectores capaces de regular los niveles de esclerostina. Por un lado, dentro de los efectores positivos se encuentran las proteínas morfogenéticas óseas (BMPs)9 o la acción combinada del factor de necrosis tumoral (TNF) y el factor de necrosis tumoral inductor débil de la apoptosis (TWEAK)10. Por otro lado, dentro de los reguladores negativos destacan la hormona paratiroidea (PTH)11,12, la prostaglandina E2 (PGE2)12 y la carga mecánica, siendo esta última de especial relevancia debido al papel que este tipo de estimulo tiene sobre la homeostasis ósea13. Desgraciadamente, muchos de estos experimentos se han llevado a cabo en modelos murinos y está por ver hasta qué punto son trasladables al hueso humano. Además, aunque se han descrito los efectos de esos factores, apenas se han identificado los mecanismos moleculares que subyacen bajo sus efectos sobre la expresión de SOST.
Uno de los obstáculos que se encuentran los investigadores a la hora de estudiar la regulación de la producción de esclerostina es la ausencia de sistemas en los que este gen se exprese activamente. Actualmente no hay líneas osteocíticas humanas disponibles. Se ha comunicado la generación de algunas líneas murinas, pero a pesar de que éstas muestran algunas características fenotípicas propias de los osteocitos, su producción de esclerostina es apenas detectable. Por ello es de sumo interés encontrar un buen sistema en el que identificar los factores involucrados en la regulación de la expresión de este gen.
Curiosamente, no toda la secuencia promotora del gen SOST está conservada entre especies, lo que sugiere que la regulación puede ser diferente en función de la especie. Ello hace todavía más evidente la necesidad de desarrollar modelos humanos. Algunos trabajos sugieren que la región 5' del gen tendría dos partes: una región cercana al inicio de la transcripción, que muestra una marcada actividad transcripcional, y otra, situada a unas 1.000 pares de bases de distancia del inicio de la transcripción, que podría tener un efecto inhibidor14. Por otro lado, es interesante señalar que varios grupos, incluido el nuestro, han demostrado la asociación de algunos polimorfismos situados en la región 5' del gen con la densidad mineral ósea (DMO)15,16. En esa misma línea, también en estudios de asociación genómica (GWAS) se han encontrado algunos polimorfismos de un nucleótido (SNPs) próximos a este gen asociados con la DMO17. Ello sugiere que dichos polimorfismos pueden tener una repercusión funcional y modular la expresión del gen, pero en realidad se desconoce si realmente es así y cuáles serían los mecanismos moleculares implicados.
Dada la importancia que se le atribuye a la esclerostina en la formación ósea, la identificación de mecanismos moleculares que regulan sus niveles puede abrir nuevos campos de investigación en la biología ósea, y quizás ayudar a identificar nuevas dianas terapéuticas en relación con la inhibición de su producción, lo que tendría un efecto anabólico sobre el hueso. Además, la validación de nuevos modelos celulares de origen humano en los que poder estudiar estos mecanismos puede ser crucial para el avance en el conocimiento de la regulación de la esclerostina. En este artículo revisaremos brevemente algunos resultados recientes de nuestro laboratorio y de otros investigadores que van aportando nueva luz sobre estas cuestiones.
Metilación del ADN y regulación de la expresión génica
Buena parte de las citosinas del ADN de los mamíferos están metiladas, en especial cuando van seguidas de una guanina, es decir, formando dinucleótidos CG (a menudo denominados también CpG, con una "p” que indica el grupo fosfato que une ambas bases). Se supone que la metilación aporta estabilidad al ADN y evita el "ruido transcripcional” de fondo. Existen zonas del ADN, llamadas "islas CpG”, que tienen un comportamiento peculiar. Esas islas consisten en regiones de unos cuantos cientos de nucleótidos que son particularmente ricas en CpG y se hallan frecuentemente en las regiones promotoras de muchos genes. En los últimos años se ha ido demostrando que el nivel de metilación de esas islas CpG (y de las regiones adyacentes, denominadas "orillas CpG”) desempeña un importante papel en la regulación de la expresión de muchos genes. En general, cuando las CpG de las regiones promotoras se encuentran muy metiladas, se reprime la trascripción del ADN en ARN y, en consecuencia, se reducen los niveles de la proteína codificada por ese gen. A la inversa, la desmetilación del promotor tiende a asociarse a una transcripción activa del gen.
]]> Los mecanismos moleculares implicados en la regulación de la expresión génica a través de cambios en la metilación son múltiples y sólo se conocen en parte. Así, por ejemplo, la metilación del ADN puede impedir la unión al mismo de algunos factores activadores de la transcripción. Por otro lado, las regiones metiladas reclutan algunas proteínas que se fijan específicamente a esas regiones metiladas. Es el caso de la MeCP2, proteína fijadora de CpG metiladas18. Por otro lado, hay que tener en cuenta que la metilación del ADN actúa en combinación con otros mecanismos epigenéticos, específicamente con las modificaciones postraslacionales de las histonas. De hecho, cuando MeCP2 se fija al ADN, recluta otras proteínas, como las HDAC (desacetilasas de histonas) que modifican las colas de las histonas próximas a esa región. En su conjunto, esas modificaciones contribuyen a modular la expresión génica. Por ejemplo, la mayor acetilación de las histonas suele asociarse a una activación de la transcripción; por el contrario, la metilación de ciertas lisinas presentes en las histonas se asocia a una represión génica19.Los patrones de metilación del ADN se transmiten a través de la mitosis, es decir, se heredan de la célula que se divide a las dos células hijas. En ello desempeña un papel esencial una familia de enzimas llamadas ADN-metiltransferasas (DNMTs), en particular la tipo 120,21.
La desmetilación del ADN puede ser un fenómeno pasivo, es decir, puede aparecer a lo largo de algunas divisiones celulares si las DNMT no realizan su función de re-metilación de las cadenas hijas del ADN. Pero la desmetilación puede ser también un proceso activo. Es decir, es posible que algunas regiones del ADN se desmetilen sin necesidad de que tenga lugar la división de la célula y la consiguiente replicación del ADN. El proceso por el que se lleva a cabo la desmetilación activa no se conoce bien, pero en él parecen jugar un papel especial la enzima GADD45 y la conversión de las metilcitosinas a hidroximetilcitosinas19;22;23. Tampoco se conoce bien cuál es su importancia real en la homeostasis tisular. No obstante, se ha sugerido que puede estar implicada en la diferenciación de los osteoblastos24.
Nuestro grupo ha demostrado que la metilación y desmetilación de algunos genes desempeñan un papel esencial en las variaciones de los patrones de expresión génica que tienen lugar a lo largo de los diversos estadios de la diferenciación de la estirpe osteoblástica. Por ejemplo, utilizando una técnica de microdisección asistida por láser y posterior análisis del ADN de las células así capturadas, hemos comprobado que en el paso de osteoblastos a osteocitos tiene lugar una reducción marcada de la metilación del promotor del gen SOST. Ese es un requisito necesario para que, a diferencia de lo que ocurre con los osteoblastos, los osteocitos puedan sintetizar esclerostina25. También otros genes implicados en la biología del esqueleto se regulan, en parte, a través del nivel de metilación de sus promotores. Es el caso, por ejemplo, de la osteoprotegerina, el ligando RANK (RANKL), la fosfatasa alcalina, osterix o el receptor de estrógenos26-28.
Desmetilacion del ADN como herramienta experimental
Los cambios en la metilación de las islas CpG son mecanismos de regulación muy potentes. Posiblemente no están implicados en la regulación fina de la expresión génica, sino que ejercen como una especie de "interruptores” moleculares que encienden y apagan la transcripción génica. Una vez la desmetilación permite la transcripción, otros mecanismos (humorales, físicos, etc.) serán los responsables de ajustar de manera precisa la expresión del gen, en función de las necesidades del momento29.
La potencia reguladora de los mecanismos ligados a la metilación se pone de manifiesto en determinados experimentos en los cuales se induce farmacológicamente la desmetilación del ADN. Para ello, a menudo se utilizan análogos de nucleótidos, como la azacitidina y la deoxiazacitidina (o decitabina) que inhiben la actividad de las DNMTs. Así, hemos podido demostrar que la incubación de diferentes tipos de células con decitabina induce de manera intensa la expresión de esclerostina aun cuando en condiciones normales esas células no expresen el gen25.
Este fenómeno tiene además una interesante repercusión práctica, puesto que facilita el estudio de los mecanismos moduladores de la expresión de esclerostina. Dado que no existen líneas osteocíticas humanas, ni tampoco métodos para aislar osteocitos viables de huesos humanos, resulta complicado explorar los mecanismos reguladores de este gen en humanos. Aunque existen diferentes líneas inmortalizadas de tipo osteoblástico y es relativamente fácil obtener osteoblastos a partir de biopsias de hueso, estas células no expresan esclerostina. Ahora bien, la desmetilación de su promotor con decitabina induce la expresión de ese gen, pudiendo así funcionar en teoría como un modelo experimental para analizar los factores físicos y químicos implicados en su regulación. No obstante, para ser realmente útil este modelo, los osteoblastos deberían mantener un patrón de respuesta a diferentes estímulos similar a la que presentan los osteocitos en modelos experimentales animales en vivo30,31.
Efectivamente, parece ser así. Los resultados que hemos obtenido en este modelo de osteoblastos tratados con decitabina han confirmado el efecto inhibidor de la PTH y el efecto estimulador de las BMPs (proteínas morfogenéticas óseas) sobre la expresión de SOST32. Por otro lado, hemos podido comprobar que los osteoblastos tratados con decitabina mantienen la respuesta no sólo a los factores humorales, sino también a los estímulos mecánicos. Cuando estas células se someten a un flujo pulsátil del medio de cultivo (que simula el estímulo de las membranas de los osteocitos por el líquido presente en las lagunas y canalículos del hueso) se inducen una serie de respuestas bioquímicas entre las que destaca la inducción de sintasas de óxido nítrico (NOS), con la consiguiente acumulación del mismo en el medio. Esta respuesta se mantiene en los osteoblastos pretratados con decitabina. Además, en esos cultivos se puede comprobar que el estímulo mecánico induce una reducción de la expresión de esclerostina, en línea con lo demostrado en modelos experimentales en vivo13,33. Los experimentos posteriores con inhibidores y donadores de óxido nítrico han permitido comprobar que realmente la síntesis de óxido nítrico está implicada en el efecto inhibidor de la expresión de SOST inducida por el estímulo mecánico34.
]]>Promotor del gen SOST, esclerostina y masa ósea
En varios estudios de genes candidatos y también en algunos de asociación genómica (GWAS) se han encontrado algunos polimorfismos del gen SOST asociados con la densidad mineral ósea15,35. Así, hemos comprobado que las mujeres homocigóticas para el alelo minoritario (G) del SNP rs851054, situado en la región promotora 5' del gen, tienen una DMO significativamente más baja que las mujeres con otros genotipos. Ello sugiere que ese polimorfismo puede provocar diferencias en la actividad transcripcional en función del alelo que esté presente. Para profundizar en los mecanismos implicados, hemos clonado la región completa del promotor de SOST (posiciones -1440/+30 en relación con el sitio de inicio de la transcripción o TSS) y comprobado su actividad transcripcional en un vector reportero de luciferasa, tras su transfección en diferentes tipos celulares. La clonación de varias regiones de ese fragmento nos ha permitido comprobar que la región más activa parece estar en los primeros 500 nucleótidos. De hecho, la actividad transcripcional de los vectores con inserción de la región -581/+30 es algo mayor que la de la región completa (-1440/+30). Por el contrario, la región más distal (-1440/-1030) no es activa, mientras que una región intermedia (-1032/-571) tiene una cierta actividad, aunque claramente menor que la de la región completa o la de la región más próxima a la TSS. Asimismo, hemos comprobado que BMP2 incrementa la actividad transcripcional de esas construcciones, mientras que la PTH no tiene efecto, lo que está de acuerdo con los estudios que indican que el efecto de esta hormona está mediado por una región enhancer localizada a varios miles de pares de bases32.
Por otro lado, a partir de ADN genómico de individuos homocigotos para varios polimorfismos frecuentes del promotor de SOST (rs801054 y rs801056), hemos clonado las regiones promotoras con cada uno de los alelos posibles de esos polimorfismos en vectores reporteros de luciferasa. Hemos analizado después su actividad transcripcional previa transfección en diversas líneas de tipo osteoblástico. Sin embargo, las diferencias en la actividad de los diversos alelos han sido pequeñas (datos no publicados). Ello sugiere que la asociación demostrada de estos alelos con la densidad mineral ósea debe estar mediada por mecanismos indirectos que no se reproducen en estos modelos experimentales. Entre ellos, cabe pensar en determinados factores, físicos o humorales, presentes en vivo y no in vitro; la interacción de otros elementos celulares presentes en el microambiente óseo; o interacciones complejas que implican la estructura tridimensional de la cromatina y la implicación de otras regiones distantes del ADN. Un candidato evidente es la llamada región de Van Buchem, situada a varios miles de bases del gen, y en la cual se ha descrito regiones reguladoras (como la llamada ECR5), que parecen mediar la respuesta a algunos factores, en particular a la PTH36,37.
Conclusión
La esclerostina desempeña un papel importante en la regulación del metabolismo óseo, como queda demostrado por los cambios dramáticos en la masa ósea que se producen cuando se inhibe su actividad mediante anticuerpos monoclonales38,39. Sin embargo, el conocimiento de los mecanismos que regulan su expresión es aún incompleto. No obstante, en los últimos años se han generado nuevos datos que permiten ir dibujando, aunque sea esquemáticamente, algunos de los factores y vías implicados (Figura 1).
]]> Este trabajo y los experimentos que se mencionan en él se han realizado también con la ayuda de becas investigación del ISCIII (PI12/615) y con ayudas del IFIMAV-IDIVAL.
Los autores no tienen conflictos de interés relevantes para este trabajo.
Bibliografía
1. van Bezooijen RL, Roelen BA, Visser A, Wee-Pals L, de Wilt E, Karperien M, et al. Sclerostin is an osteocyte-expressed negative regulator of bone formation, but not a classical BMP antagonist. J Exp Med 2004;199:805-14. [ Links ]
2. Sutherland MK, Geoghegan JC, Yu C, Turcott E, Skonier JE, Winkler DG, et al. Sclerostin promotes the apoptosis of human osteoblastic cells: a novel regulation of bone formation. Bone 2004;35:828-35. [ Links ]
3. Poole KE, van Bezooijen RL, Loveridge N, Hamersma H, Papapoulos SE, Lowik CW, et al. Sclerostin is a delayed secreted product of osteocytes that inhibits bone formation. FASEB J 2005;19(13):1842-4. [ Links ]
]]>4. Balemans W, Ebeling M, Patel N, Van Hul E, Olson P, Dioszegi M, et al. Increased bone density in sclerosteosis is due to the deficiency of a novel secreted protein (SOST). Hum Mol Genet 2001;10:537-43. [ Links ]
5. Brunkow ME, Gardner JC, Van Ness J, Paeper BW, Kovacevich BR, Proll S, et al. Bone dysplasia sclerosteosis results from loss of the SOST gene product, a novel cystine knot-containing protein. Am J Hum Genet 2001;68:577-89. [ Links ]
6. Padhi D, Jang G, Stouch B, Fang L, Posvar E. Single-dose, placebo-controlled, randomized study of AMG 785, a sclerostin monoclonal antibody. J Bone Miner Res 2011;26:19-26. [ Links ]
7. Agholme F, Li X, Isaksson H, Ke HZ, Aspenberg P. Sclerostin antibody treatment enhances metaphyseal bone healing in rats. J Bone Miner Res 2010;25:2412-8. [ Links ]
8. Delgado-Calle J, Arozamena J, Garcia-Renedo R, Garcia-Ibarbia C, Pascual-Carra MA, Gonzalez-Macias J, et al. Osteocyte deficiency in hip fractures. Calcif Tissue Int 2011;89:327-34. [ Links ]
]]>9. Kamiya N, Kobayashi T, Mochida Y, Yu PB, Yamauchi M, Kronenberg HM, et al. Wnt inhibitors Dkk1 and Sost are downstream targets of BMP signaling through the type IA receptor (BMPRIA) in osteoblasts. J Bone Miner Res 2010;25:200-10. [ Links ]
10. Vincent C, Findlay DM, Welldon KJ, Wijenayaka AR, Zheng TS, Haynes DR, et al. Pro-inflammatory cytokines TNF-related weak inducer of apoptosis (TWEAK) and TNFalpha induce the mitogen-activated protein kinase (MAPK)-dependent expression of sclerostin in human osteoblasts. J Bone Miner Res 2009;24:1434-49. [ Links ]
11. Miniati M, Pistolesi M, Marini C, Di Ricco G, Formichi B, Prediletto R, et al. Value of perfusion lung scan in the diagnosis of pulmonary embolism: results of the prospective investigative study of acute pulmonary embolism (PISA-PED). Am J Respir Crit Care Med 1996;154:1387-93. [ Links ]
12. Genetos DC, Yellowley CE, Loots GG. Prostaglandin E(2) Signals Through PTGER2 to Regulate Sclerostin Expression. PLoS ONE 2011;6:e17772. [ Links ]
13. Robling AG, Bellido T, Turner CH. Mechanical stimulation in vivo reduces osteocyte expression of sclerostin. J Musculoskelet Neuronal Interact 2006;6:354. [ Links ]
]]>14. Sevetson B, Taylor S, Pan Y. Cbfa1/RUNX2 directs specific expression of the sclerosteosis gene (SOST). J Biol Chem 2004;279:13849-58. [ Links ]
15. Valero C, Zarrabeitia MT, Hernandez JL, Pineda B, Cano A, Garcia-Perez MA, et al. Relationship of sclerostin and secreted frizzled protein polymorphisms with bone mineral density: an association study with replication in postmenopausal women. Menopause 2011;18:802-7. [ Links ]
16. Huang QY, Li GH, Kung AW. The -9247 T/C polymorphism in the SOST upstream regulatory region that potentially affects C/EBPalpha and FOXA1 binding is associated with osteoporosis. Bone 2009;45:289-94. [ Links ]
17. Richards JB, Kavvoura FK, Rivadeneira F, Styrkarsdottir U, Estrada K, Halldorsson BV, et al. Collaborative meta-analysis: associations of 150 candidate genes with osteoporosis and osteoporotic fracture. Ann Intern Med 2009;151:528-37. [ Links ]
18. Reddington JP, Pennings S, Meehan RR. Non-canonical functions of the DNA methylome in gene regulation. Biochem J 2013;451:13-23. [ Links ]
]]>19. Branco MR, Ficz G, Reik W. Uncovering the role of 5-hydroxymethylcytosine in the epigenome. Nat Rev Genet 2012;13:7-13. [ Links ]
20. Calvanese V, Lara E, Kahn A, Fraga MF. The role of epigenetics in aging and age-related diseases. Ageing Res Rev 2009;8:268-76. [ Links ]
21. Subramaniam D, Thombre R, Dhar A, Anant S. DNA methyltransferases: a novel target for prevention and therapy. Front Oncol 2014;4:80. [ Links ]
22. Niehrs C, Schafer A. Active DNA demethylation by Gadd45 and DNA repair. Trends Cell Biol 2012;22:220-7. [ Links ]
23. Pfeifer GP, Kadam S, Jin SG. 5-hydroxymethylcytosine and its potential roles in development and cancer. Epigenetics Chromatin 2013;6:10. [ Links ]
]]>24. Zhang RP, Shao JZ, Xiang LX. GADD45A protein plays an essential role in active DNA demethylation during terminal osteogenic differentiation of adipose-derived mesenchymal stem cells. J Biol Chem 2011;286:41083-94. [ Links ]
25. Delgado-Calle J, Sanudo C, Bolado A, Fernandez AF, Arozamena J, Pascual-Carra MA, et al. DNA methylation contributes to the regulation of sclerostin expression in human osteocytes. J Bone Miner Res 2012;27:926-37. [ Links ]
26. Vrtacnik P, Marc J, Ostanek B. Epigenetic mechanisms in bone. Clin Chem Lab Med 2014;52:589-608. [ Links ]
27. Delgado-Calle J, Sanudo C, Sanchez-Verde L, Garcia-Renedo RJ, Arozamena J, Riancho JA. Epigenetic regulation of alkaline phosphatase in human cells of the osteoblastic lineage. Bone 2011;49:830-8. [ Links ]
28. Delgado-Calle J, Sanudo C, Fernandez AF, Garcia-Renedo R, Fraga MF, Riancho JA. Role of DNA methylation in the regulation of the RANKL-OPG system in human bone. Epigenetics 2012;7:83-91. [ Links ]
]]>29. Delgado-Calle J, Garmilla P, Riancho JA. Do epigenetic marks govern bone mass and homeostasis? Curr Genomics 2012;13:252-63. [ Links ]
30. Robling AG, Niziolek PJ, Baldridge LA, Condon KW, Allen MR, Alam I, et al. Mechanical stimulation of bone in vivo reduces osteocyte expression of Sost/sclerostin. J Biol Chem 2008;283:5866-75. [ Links ]
31. Silvestrini G, Ballanti P, Leopizzi M, Sebastiani M, Berni S, Di Vito M, et al. Effects of intermittent parathyroid hormone (PTH) administration on SOST mRNA and protein in rat bone. J Mol Histol 2007;38:261-9. [ Links ]
32. Delgado-Calle J, Arozamena J, Perez-Lopez J, Bolado-Carrancio A, Sanudo C, Agudo G, et al. Role of BMPs in the regulation of sclerostin as revealed by an epigenetic modifier of human bone cells. Mol Cell Endocrinol 2013;369:27-34. [ Links ]
33. Lin C, Jiang X, Dai Z, Guo X, Weng T, Wang J, et al. Sclerostin mediates bone response to mechanical unloading through antagonizing Wnt/beta-catenin signaling. J Bone Miner Res 2009;24:1651-61. [ Links ]
]]>34. Delgado-Calle J, Riancho JA, Klein-Nulend J. Nitric oxide is involved in the down-regulation of SOST expression induced by mechanical loading. Calcif Tissue Int 2014;94:414-22. [ Links ]
35. Estrada K, Styrkarsdottir U, Evangelou E, Hsu YH, Duncan EL, Ntzani EE, et al. Genome-wide meta-analysis identifies 56 bone mineral density loci and reveals 14 loci associated with risk of fracture. Nat Genet 2012;44:491-501. [ Links ]
36. Leupin O, Kramer I, Collette NM, Loots GG, Natt F, Kneissel M, et al. Control of the SOST bone enhancer by PTH using MEF2 transcription factors. J Bone Miner Res 2007;22:1957-67. [ Links ]
37. Loots GG, Kneissel M, Keller H, Baptist M, Chang J, Collette NM, et al. Genomic deletion of a long-range bone enhancer misregulates sclerostin in Van Buchem disease. Genome Res 2005;15:928-35. [ Links ]
38. McClung MR, Grauer A, boonen s, Bolognese MA, Brown JP, Diez-Perez A, et al. Romosozumab in postmenopausal women with low bone mineral density. N Engl J Med 2014;370:412-20. [ Links ]
]]>39. McColm J, Hu L, Womack T, Tang CC, Chiang AY. Single- and multiple-dose randomized studies of blosozumab, a monoclonal antibody against sclerostin, in healthy postmenopausal women. J Bone Miner Res 2014;29:935-43. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
José A. Riancho Moral
Departamento de Medicina Interna
Hospital U. Marqués de Valdecilla
39011 Santander (España)
Correo electrónico: jose.riancho@unican.es