Oxicodona
J. Sanz1
| Sanz Ortiz J. Oxycodone. Rev Soc Esp Dolor 2005; 12: 525-531.
| ||
| SUMMARY The present report makes a detailed revision and up date of a new pain killer recently included in Spanish handbook. It has oral route of administration and controlled liberation. Opioid analgesic mechanism and pharmacokinetic are described. The differences with other opioids are analysed. The incidence of side effects is studied and compared with other. Finally guidelines are described for being used. © 2005 Sociedad Española del Dolor. Published by Aran Ediciones S.L. Key words: Opioids. Oxycodone. Analgesic.
| RESUMEN ]]> En el presente trabajo se realiza una revisión y puesta al día de un nuevo analgésico opioide en forma de comprimidos de administración oral de liberación controlada. Se analiza su farmacocinética, su farmacodinamia así como sus interacciones medicamentosas. Se describe el nuevo mecanismo de liberación controlada y se comparan sus características y efectos secundarios con otros preparados opioides de administración por vía oral de liberación retardada. Finalmente se dan las pautas de utilización. © 2005 Sociedad Española del Dolor. Publicado por Arán Ediciones, S. L.Palabras clave: Opioides. Oxicodona. Analgésicos.
|
1Servicio de Oncología Médica y Cuidados Paliativos
Hospital Universitario Marqués de Valdecilla. Facultad de Medicina.
Universidad de Cantabria
Recibido: 27-06-05.
Aceptado: 02-09-05.
ÍNDICE ]]>
1. RESUMEN
2. INTRODUCCIÓN E HISTORIA
3. EL SER HUMANO COMO FUENTE IMPREDECIBLE DE COMPORTAMIENTO
4. FARMACOLOGÍA DE OXICODONA
5. INTERACCIONES FARMACOLÓGICAS Y COMBINACIONES DE FÁRMACOS
6. OXYCONTIN® (HIDROCLORURO DE OXICODONA): ¿COMPRIMIDOS DE LIBERACIÓN CONTROLADA O RETARDADA?
7. EFECTOS ADVERSOS DE OXICODONA
8. COMPARACIÓN ENTRE OXICODONA DE LIBERACIÓN CONTROLADA Y MORFINA DE LIBERACIÓN RETARDADA
9. UTILIZACIÓN EN LA PRÁCTICA CLÍNICA DE OXICODONA
10. OXICODONA: DOLOR NEUROPÁTICO Y OTRAS INDICACIONES MÉDICAS ]]>
1. RESUMEN
Recientemente, oxicodona (OxyContin®) se ha incorporado al abanico de opioides disponibles por vía oral en España, como alternativa en aquellos pacientes que presentan intolerancia a morfina.
Oxicodona (14-hidroxi-7,8-dihidrocodeinona) es un producto semisintético derivado de la tebaína (alcaloide del opio), agonista puro de receptores mu y kappa y sin techo terapéutico. El efecto terapéutico es principalmente analgésico, ansiolítico y sedante. Se ha demostrado que su combinación con morfina es sinérgica, con un perfil analgésico mejor y menor incidencia de emesis. Muestra una mayor biodisponibilidad que morfina, sin que se vea afectada por la ingesta de alimentos o la edad (ancianos): salvo en casos de insuficiencia hepática o renal grave, no es necesario reducir dosis. La metabolización hepática está mediada por el citocromo P450 2D6 (CYP2D6), por lo que puede interaccionar con sertralina y fluoxetina (inhibidores potentes de CYP2D6); asimismo, reduce la biodisponibilidad de ciclosporina y la rifampicina favorece su aclaramiento.
La formulación galénica de oxicodona de liberación controlada combina las características de un sistema de liberación inmediata y prolongada en un mismo comprimido por lo que, a pesar de ser de liberación retardada, tiene una fase inicial que hace innecesaria la administración simultánea del mismo fármaco en forma de comprimido de liberación inmediata, a diferencia de lo que ocurre con morfina. Los efectos secundarios son similares a los del resto de opioides. Los comprimidos de liberación prolongada no deben romperse, masticarse o triturarse ya que ello puede dar lugar a una sobredosis. Por otra parte, la ingestión masiva de oxicodona puede producir edema pulmonar no cardiogénico, depresión respiratoria y parada cardiaca que puede ser refractaria a la administración de naloxona.
Los tres ensayos fase III realizados con el objetivo de determinar la equivalencia analgésica y aceptabilidad entre oxicodona de liberación controlada y morfina de liberación retardada, han mostrado que oxicodona es más potente que morfina (relación 1:2), y produce menos náuseas, trastornos cognitivos (alucinaciones) y prurito.
En pacientes no expuestos a opioides previamente, debe comenzarse con la dosis más baja (10 mg/12 horas); si en 24 horas no hay mejoría, escalar dosis 50-100%; a partir de las 48 horas, los incrementos de dosis sucesivos son del 25-50% hasta el alivio eficaz. La mayoría de los pacientes no necesitan dosis superiores a 40 mg/12 horas.
]]> Además de en el tratamiento del dolor crónico oncológico, oxicodona ha demostrado ser eficaz en la neuralgia postherpética y en otras indicaciones médicas independientes de las analgésicas, tales como el síndrome de Tourette (en combinación con clonidina) o el síndrome idiopático de las piernas inquietas.En conclusión, oxicodona se presenta como el opioide oral de primera opción para el tratamiento del dolor intenso no controlado con morfina o en caso de intolerancia a esta. Es de liberación controlada bifásica (inmediata y retardada), de fácil titulación, de eficacia analgésica al menos similar a la morfina, mejor tolerado y con el valor añadido de ser eficaz en casos de dolores difíciles (dolor neuropático).
2. INTRODUCCIÓN E HISTORIA
Hasta 1988 en que se introduce en el vademécum español la primera morfina en forma de comprimidos orales de liberación retardada (MSTContinus®) no existía disponibilidad de fármacos opioides mayores por vía oral. En 1990 se incorporan los comprimidos de morfina oral de liberación inmediata (Sevredol®) Desde esa fecha hasta la actualidad se han ido sumando nuevos opioides (fentanilo y buprenorfina) con diferentes vías de administración como la mucosa oral (15 de febrero de 2002 Actiq®) o la piel (año 1998 Durogesic®‚ y 1 de noviembre de 2002 Transtec®) (1). El 15 de junio de 2004 oxicodona de liberación controlada (OxyContin®) se agrega al "menú" de opioides disponibles por vía oral en España. Esta sustancia no es nueva sino que se conoce en Europa desde 1915 tanto en administración por vía parenteral como oral. En EE.UU. está disponible en forma de comprimidos de liberación inmediata desde 1950, en combinación con Aspirina® o acetaminofeno porque estaba catalogada como congénere de la codeína en el 2º escalón de la OMS. Desde 1996 los comprimidos de liberación retardada (en forma de fármaco único) se añaden al portafolio analgésico opioide en EE.UU (2) para el tratamiento del dolor moderado-intenso (3er escalón). La primera revisión bibliográfica de oxicodona en España ha sido publicada en mayo de 2004 (3).
3. EL SER HUMANO COMO FUENTE IMPREDECIBLE DE COMPORTAMIENTO
La prescripción de opioides viene matizada por las variaciones existentes en cada persona en su bagaje enzimático, composición genética, cambios farmacocinéticos y sensibilidad específica para los efectos no deseados. Y por qué no, también por su personalidad y proyecto de vida. En otras palabras cada persona es un mundo y sus reacciones, tanto biológicas como psicológicas son imprevisibles. Esta es la razón de por qué es necesario titular la dosis de morfina oral individualmente: 10 mg/4 horas de morfina de liberación inmediata por vía oral tiene efectos distintos en personas diferentes. La mayoría de los pacientes con dolor relacionado con el cáncer pueden ser aliviados con la administración de morfina, no obstante, en algunos pacientes (10-15%) los efectos secundarios no deseados son limitantes de la dosis y comprometen su eficacia analgésica. En esta situación lo indicado es realizar un "cambio o sustitución de opioide" que mejora el perfil de efectos secundarios sin perder la eficacia analgésica. Esta variabilidad en el efecto analgésico y/o efectos adversos está relacionada con un fenómeno de tolerancia cruzada incompleta (4). La oxicodona amplía las posibilidades de cambio de opioide en estas situaciones mejorando la analgesia y reduciendo los efectos secundarios.
4. FARMACOLOGÍA DE OXICODONA
Lauretti y cols., en un estudio doble-ciego, aleatorizado y cruzado con 22 pacientes, evalúan la combinación de morfina con oxicodona en formulaciones de liberación retardada, para el tratamiento del dolor oncológico comparado con la administración de morfina sola. Comprueban que la combinación es sinérgica y que tiene un perfil analgésico mejor y con menor incidencia de emesis (11).
-Farmacocinética: oxicodona es más lipofílica que la morfina, por vía oral tiene un menor metabolismo hepático de "primer paso" y como resultado su biodisponibilidad es mayor (60-87%). La biodisponibilidad no se afecta por la ingesta de alimentos (12) o la edad (ancianos) (13) y, por tanto, sus concentraciones plasmáticas presentan menor variabilidad que las de morfina.
Se metaboliza en el hígado por el sistema enzimático citocromo P450 2D6 (CYP2D6) a noroxicodona (analgésico débil a concentraciones elevadas) y oximorfona (analgésico potente a concentraciones bajas), que no contribuyen al efecto farmacológico. En la insuficiencia hepática hay una alteración relevante del enzima que obliga a la reducción de la dosis. El gen CYP2D6 tiene tres mutaciones posibles, los pacientes que presenten alguna de ellas son más susceptibles a toxicidad por oxicodona (14).
La eliminación es por vía renal, el 8-14% en forma de oxicodona y el resto como noroxicodona y oximorfona. La eliminación renal del fármaco se reduce muy ligeramente en personas mayores de 65 años, por lo que no es necesario reducir dosis. Por estas razones puede sustituir a la morfina en casos de insuficiencia renal moderada (15). En presencia de insuficiencia hepática o renal grave es necesaria la reducción de la dosis. La vida media plasmática es el doble que la de morfina (3-5 horas) y alcanza niveles plasmáticos estacionarios en 24-36 horas (16), y su fijación a proteínas es del 38-45% (17).
5. INTERACCIONES FARMACOLÓGICAS Y COMBINACIONES DE FÁRMACOS
Oxicodona es metabolizada en el hígado por medio de una O-demetilación formando oximorfona, reacción catalizada por el citocromo P450 2D6 (CYP2D6). Este enzima puede ser bloqueado sin alterar los efectos farmacodinámicos de oxicodona (18). En la literatura hay descrito un caso de posible sinergismo en relación con la depresión del sistema nervioso central al combinar clonazepan y oxicodona, que pudo desencadenar la muerte del paciente por parada respiratoria y fallo cardiaco (19). En cuanto a otras interacciones farmacológicas la oxicodona puede interaccionar con la sertralina y la fluoxetina (inhibidores potentes de la enzima citocromo P450-2D6); reduce la biodisponibilidad de ciclosporina (20) y la rifampicina favorece su aclaramiento (21).
6. OXYCONTIN® (HIDROCLORURO DE OXICODONA): ¿COMPRIMIDOS DE LIBERACIÓN CONTROLADA O RETARDADA?
7. EFECTOS ADVERSOS DE OXICODONA
Son los típicos de los opioides y muchos de ellos responden a una disminución de dosis como ocurre con la morfina. Somnolencia 37%, náuseas 32%, vómitos 8%, mareo 12%, cefalea 7%, prurito 5% y ortostatismo 5% (23). Una sobredosis puede conducir a hipotensión, depresión respiratoria y parada cardiaca (24). Otros efectos secundarios de incidencia menor al 1% son: secreción inadecuada de ADH, alergia, palpitaciones, retención urinaria, amenorrea e impotencia (25).
8. COMPARACIÓN ENTRE OXICODONA DE LIBERACIÓN CONTROLADA Y MORFINA DE LIBERACION REATARDADA
Tres ensayos fase III aleatorizados doble-ciego determinan la equivalencia analgésica y aceptabilidad entre la oxicodona de liberación controlada y la morfina de liberación retardada (26-28). Ambos son opioides agonistas puros de liberación retardada o controlada. Oxicodona es más liposoluble que morfina (hidrosoluble). Oxicodona es más potente que morfina. La dosis equianalgésica a dosis única de 1 mg de oxicodona oral, corresponde a 2 mg de morfina oral (relación 1:2) (29), siendo adecuada esta estimación para el 70% de los pacientes (30).
Con respecto a los efectos adversos, oxicodona produce menos náuseas, trastornos cognitivos (alucinaciones) y prurito que morfina (31). El intervalo de la biodisponibilidad de morfina por vía oral es de 15-65%. Esta amplia variabilidad está en parte motivada por la modificación que la ingesta de alimentos con contenido graso, produce en la absorción de dicho fármaco (32). Esta circunstancia no se produce con oxicodona y su intervalo de biodisponibilidad es de 60-87% (33).
Tanto morfina como oxicodona no tienen techo terapéutico en actividad analgésica, pero en la práctica diaria sí existe un límite para su utilización que viene marcado por los efectos secundarios. Un estudio australiano señala que el 25% de los pacientes que reciben morfina y presentan delirio, mejoran al sustituir el opioide por oxicodona vía subcutánea (31). En este caso oxicodona presenta una neurotoxicidad menos intensa.
La vida media de oxicodona (3-5 horas) es superior a la de morfina oral (2,5-3 horas), su farmacocinética es predecible, no tiene metabolitos clínicamente activos, no necesita ajuste de dosis en ancianos, presenta menor metabolismo de primer paso y su biodisponibilidad es más estable y superior a la de morfina oral. En casos de insuficiencia renal se puede sustituir morfina por oxicodona ya que esta no acumula metabolitos activos (16). Al ser su forma galénica como un comprimido dual de liberación inmediata y retardada simultáneamente, permite una titulación más fácil. Actualmente oxicodona es el opioide alternativo a morfina como primera opción y en caso de efectos secundarios intolerables con morfina. Morfina tiene un claro efecto inmunosupresor (¿efecto antagonista kappa?) y oxicodona no ha mostrado efectos inmunosupresores en estudios realizados en animales (34). En la Tabla I se recogen resumidas las diferencias entre estos dos fármacos.
]]>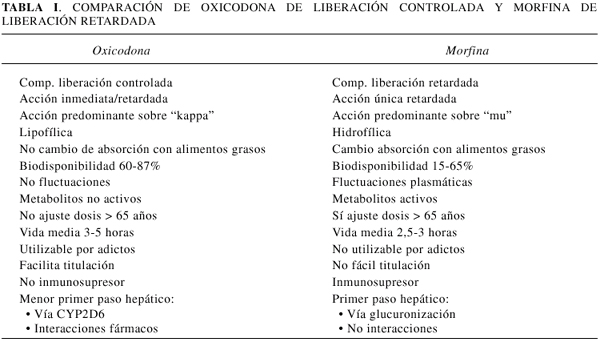
9. UTILIZACIÓN EN LA PRÁCTICA CLÍNICA DE OXICODONA
La indicación actual de oxicodona como fármaco único de liberación controlada por vía oral es el dolor intenso. El inicio de tratamiento puede ser desde exposición previa a opioides (2º escalón) a pacientes "vírgenes". En ambos casos la dosificación debe ser individualizada para cada paciente. En el primer caso la dosis viene marcada por la tabla de farmacoequivalencia analgésica correspondiente (oxicodona/morfina oral 1: 2). En pacientes no expuestos a opioides previamente, comenzar con la dosis más baja (10 mg/12 horas). Para conseguir la titulación individual adecuada proceder de la siguiente forma: si en la evaluación de 24 horas no hay mejoría, escalar dosis 50-100% según dosis de inicio. A partir de la evaluación de las 48 horas, los incrementos de dosis sucesivos son del 25-50% hasta el alivio eficaz.
Es importante remarcar que en pacientes mayores de 65 años no es necesario reducir la dosis en la mayoría de los casos, al contrario de lo que ocurre con la morfina. El alivio adecuado del dolor se obtiene con la dosis mínima eficaz de opioide ("domine") (35) y con menos efectos secundarios. Recordar que esta circunstancia no surge espontáneamente ni se improvisa, sino que hay que buscarla en el proceso continuo de titulación individual. La mayoría de los pacientes no necesitan dosis superiores a 40 mg/12 horas. Si fueran precisas dosis extra, de rescate o extraordinarias, debe utilizarse un opioide de liberación inmediata (preferentemente oxicodona si estuviera disponible). En su defecto, la alternativa es morfina de liberación inmediata o fentanilo transmucoso oral. Oxicodona no está aprobada en pacientes menores de 18 años.
10. OXICODONA: DOLOR NEUROPÁTICO Y OTRAS INDICACIONES MÉDICAS
-El dolor neuropático responde menos a opioides que el dolor nociceptivo (36). Existen cada vez más pruebas de que los opioides son eficaces en el dolor neuropático (37,38) en pacientes con neuralgia postherpética o neuropatía diabética. Algunos opioides que han demostrado su eficacia en estas situaciones son: morfina, fentanilo, tramadol, buprenorfina transdérmica y metadona. Oxicodona ha demostrado ser eficaz en la alodinia de la neuropatía postherpética (39). Una revisión sistemática del tratamiento de la neuralgia postherpética (40) comprueba que las terapias con eficacia probada (ensayos aleatorizados y controlados frente a placebo) en la actualidad son las siguientes: tramadol, altas dosis de dextrometorfano, oxicodona y gabapentina.
-Otras indicaciones médicas independientes de las analgésicas. El síndrome de Tourette (movimientos involuntarios motores, tics, comportamiento automutilatorio) mejora con la combinación de clonidina más 50 mg.día-1 de oxicodona. Esta respuesta demuestra la implicación del mecanismo de acción opioide y del sistema noradrenérgico (41). En pacientes afectados de síndrome idiopático de las piernas inquietas la oxicodona obtiene frente a placebo una mejoría sustancial de los síntomas (42).
]]> 11. PRECAUCIONES
Oxicodona tiene un perfil de abuso similar a la de otros agonistas opioides potentes, por lo que puede ser objeto de búsqueda y abuso por personas con alteraciones latentes o manifiestas de adicción. Los comprimidos de liberación prolongada no deben romperse, masticarse o triturarse ya que ello puede dar lugar a una sobredosis (25). Por otra parte, la ingestión masiva de oxicodona puede producir edema pulmonar no cardiogénico, depresión respiratoria y parada cardiaca que puede ser refractaria a la administración de naloxona (43).
12. RECOMENDACIONES
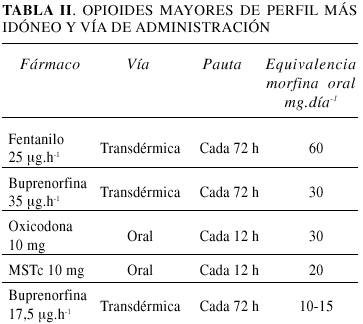
Una vez evaluado el dolor mediante la escala visual analógica (EVA) se aplican las medidas no farmacológicas y farmacológicas correspondientes. En las recomendaciones farmacológicas es importante recordar que las dosis analgésicas de opioides deben ser diseñadas de forma específica para cada paciente mediante el proceso de titulación. El tratamiento debe ser simple, con pauta horaria regular, no invasivo y si es posible, por vía oral. El objetivo es encontrar el opioide, que en su caso, obtenga el alivio necesario con la dosis mínima eficaz (dosis "domine"). Es decir, alivio estable con aceptable nivel de efectos secundarios. En la Tabla II se describen los opioides mayores de perfil más idóneo y su vía de administración.
13. CONCLUSIÓN
Disponemos de una alternativa más para el tratamiento del dolor intenso que amplía las posibilidades de analgesia eficaz en nuestros pacientes. Facilita el cambio de opioide en los casos que los efectos secundarios sean importantes. Cumple las características de poder ser administrada por vía oral, ser de liberación controlada bifásica (inmediata y retardada), de fácil titulación, y con una eficacia analgésica similar a la de morfina (patrón oro actual). Es de señalar que los trastornos cognitivos y el prurito son menos intensos que los observados con morfina. Tiene el valor añadido de ser eficaz en casos de dolores difíciles (dolor neuropático) (16).
| ]]>
|
BIBLIOGRAFÍA
1. Sanz Ortiz J. Situación actual del tratamiento del dolor. Rev Cáncer (Madrid) 2004; 18 (Supl. 1): 95-9. [ Links ]
2. Oxycodone and Oxycontin. The Medical Letter on Drugs and Therapeutics 2001; 43 (1113): 80-1. [ Links ]
3. Ordóñez Gallego A, González Barón M. Oxicodona: un nuevo opioide en España. Rev Oncol 2004; 6: 203-6. [ Links ]
4. Mercadante S. Opioid rotation for cancer pain: rationale and clinical aspects. Cancer 1999; 86: 1856-66. [ Links ]
5. Ross FB, Smith MT. The intrinsic antinociceptive effects or oxycodone appear to be kappa opioid receptor mediated. Pain 1997; 73: 151-7. [ Links ]
6. Saarialho-Kere U, Mattila MJ, Seppälä T. Psychomotor, respiratory and neuroendocrinological effects of a m-opioid receptor agonist (Oxycodone) in healthy volunteers. Pharmacol Toxicol 1989; 65: 252-7. [ Links ]
7. Shad SH, Hardy J. Oxycodone: a review of the literature. Eur J Palliative Care 2001; 8: 93-6. [ Links ]
8. Ripamonti C, Duke Dikerson E. Strategies for the treatment of cancer pain in the new millennium. Drugs 2001; 61: 955-77. [ Links ]
9. Davis MP, Varga J, Dickerson D, et al. Normal-release and contolled-release oxycodone: pharmacokinetics, pharmacodymamics, and controversy. Support Care Cancer 2003; 11: 84-92. [ Links ]
10. Ross FB, Wallis SC, Smith MT. Co-administration of sub-antinociceptive doses of oxycodone and morphine produces marked antinociceptive synergy with reduced CNS side-effects in rats. Pain 2000; 84: 421-8. [ Links ]
11. Lauretti GR, Oliveira GM, Pereira NL. Comparison of sustained-release morphine with sustained-release oxycodone in advanced cancer patients. Br J Cancer 2003; 89: 2027-30. [ Links ]
12. Benzinger DP, Kaiko Rf, Mohitto CB, et al. Differential effects of food on the bioavailability of controlled-release oxycodone tablets and immediate-release oxycodone solution. J Pharmac Sciences 1996; 85: 407-10. [ Links ]
13. Kaiko RF, Benziger DP, Fitzmartin RD, et al. Pharmacokinetic-pharmacodynamic relationship of controlled release oxycodone. Clin Pharmacol Ther 1996; 59: 52-61. [ Links ]
14. Jannetto PJ, Wong SH, Gock SB, et al. Pharmacogenomics as molecular autopsy for postmortem forensic toxicology: genotyping cytochrome P450 2D6 for oxycodone cases. J Anal Toxicol 2002; 26: 438-47. [ Links ]
15. Cairns R. The use of oxycodone in cancer-related pain: a literature review. Int J Palliat Nurs 2001; 7: 522-7. [ Links ]
16. Levy MH. Advancement of opioide analgesia with controlled-release oxycodone. Eur J Pain 2001; 5 (Supl. A): 113-6. [ Links ]
17. Leow KP, Wright AWE, Cramond T, et al. Determination of the serum protein binding of oxycodone and morphine using ultrafiltration. Ther Drug Monit 1993; 15: 440-7. [ Links ]
18. Heiskanen T, Olkkola KT, Kalso E. Effects of blocking CYP2D6 on the pharmacokinetics and pharmacodynamics of oxycodone. Clin Pharmacol Ther 1998; 64: 603-11. [ Links ]
19. Burrows DL, Hagardorn AN, Harlan GC, et al. A fatal drug interaction between oxycodone and clonazepam. J Forensic Sci 2003; 48: 1-4. [ Links ]
20. Lill J, Bauer LA, Horn JR, et al. Cyclosporine-drug interactions and the influence of patient age. Am J Health SystPharm 2000; 57: 1579-84. [ Links ]
21. Rifadin. PDR: Physicians' Desk Reference. 58 ed. 2004. p. 761-4. [ Links ]
22. Mandema JW, Kaiko RF, Oshlack B, et al. Characterization and validation of a pharmacokinetic model controlled-release oxycodone. Br J Clin Pharmacol 1996; 42: 747-56. [ Links ]
23. Curtis GB, Johnson GH, Clark P, et al. Relative potency of controlled-release oxycodone and controlled-release morphine in a postoperative pain model. Eur J Clin Pharmacol 1999; 55: 425-9. [ Links ]
24. Inturrisi ChE. Clinical pharmacology of opioids for pain. Clin J Pain 2002; 18: S3-S13. [ Links ]
25. Oxycontin® (hidrocloruro de oxicodona). Monografía de producto. Mundipharma, 2004. p. 35. [ Links ]
26. Mucci-LoRusso P, Berman BS, Silberstein PT, et al. Controlled release oxycodone compared with controlled release morphine in the treatment of cancer pain: a randomised, double-blind, parallel group study. Eur J Pain 1998; 2: 239-49. [ Links ]
27. Bruera E, Belzile M, Pituskin E, et al. Randomized, double-blind cross over trial comparing safety and efficacy of oral controlled release oxycodone with controlled release morphine in patients with cancer pain. J Clin Oncol 1998; 16: 3222-9. [ Links ]
28. Heiskanen T, Kalso E. Controlled release oxycodone and morphine in cancer related pain. Pain 1997; 73: 37-45. [ Links ]
29. Foley KM. The treatment of cancer pain. N Engl J Med 1985; 313: 84-95. [ Links ]
30. Kaplan R, C-V Parris W, Citron ML, et al. Comparison of controlled-release and immediate-release oxycodone tablets in patients with cancer pain. J Clin Oncol 1998; 16: 3230-7. [ Links ]
31. Maddocks I, Somogyi A, Abbott F, et al. Attenuation of morphine induced delirium in palliative care by substitution with infusion of oxycodone. J Pain Symptom Manage 1996; 12: 182-9. [ Links ]
32. Gourlay GK, Plummer JL, Cherry DA, et al. Influence of a high-fat meal on the absorption of morphine from oral solutions. Clin Pharmacol Ther 1989; 46: 463-8. [ Links ]
33. Poyhia R, Vainio A, Kalso E. A review of oxycodone's clinical pharmacokinetics and pharmacodynamics. J Pain Symptom Manage 1993; 8: 63-7. [ Links ]
34. Sacerdote P, Manfredi B, Mantegazza P, et al. Antinociceptive and immunosuppressive effects of opiate drugs: a structure-related activity study. Br J Pharmacol 1997; 121: 834-40. [ Links ]
35. Sanz-Ortiz J. Ancianidad y mundo opioide. Med Clin (Barc) 2004; 122: 227-30. [ Links ]
36. Cherny NI, Thaler HT, Friedlander-Klar H, et al. Opioid responsiveness of cancer pain syndromes caused by neuropathic pain or nociceptive mechanisms: a combined analysis of controlled single-dose studies. Neurology 1994; 44: 857-61. [ Links ]
37. Portenoy RK, Coyle N. Controversies in the long-term management of analgesic therapy in patients with advanced cancer. J Pain Symptom Manage 1990; 5: 307-19. [ Links ]
38. Rowbotham M, Reisner-Keller LA, Fields HL. Both intravenous lidocaine and morphine reduce pain of postherpetic neuralgia. Neurology 1991; 41: 102-28. [ Links ]
39. Watson CP, Babul N. Efficacy of oxicodone in neuropatic pain: a randomized trial in postherpetic neuralgia. Neurology 1998; 50: 1837-41. [ Links ]
40. Alper BS, Lewis PR. Treatment of postherpetic neuralgia: a systematic review of the literature. J Fami practice 2002; 51: 121-8. [ Links ]
41. Sandyk R. Tourette syndrome: successful treatment with clonidine and oxycodone. J Neurol 1986; 233: 178-9. [ Links ]
42. Walters AS, Wagner ML, Hening WA, et al. Successful treatment of the idiopathic restless legs syndrome in a randomized double-blind trial of oxycodone versus placebo. Sleep 1993; 16: 327-32. [ Links ]
43. Schneir AB, Vadeboncoeur TF, Offerman SR, et al. Massive OxyContin ingestion refractory to naloxone therapy. Ann Emerg Med 2002; 40: 425-8. [ Links ] ]]>