INTRODUCCIÓN
La trombocitopenia inducida por fármacos (TCPIF) es un efecto adverso (EA) poco común, pero potencialmente severo. Algunos antiinfecciosos se han relacionado más frecuentemente con su aparición1, pero en ficha técnica apenas se contempla la incidencia de trombocitopenia como EA, y solo se dispone de casos descritos en literatura. Se presentan dos casos con trombocitopenia asociada a ceftarolina y/o daptomicina durante el tratamiento de endocarditis infecciosa por Staphylococcus aureus meticilin resistente (SARM).
DESCRIPCIÓN DE LOS CASOS
Caso clínico 1
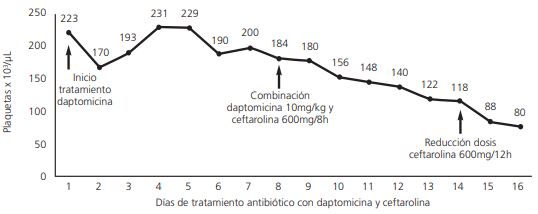
Paciente de 75 años con sospecha de sobreinfección del muñón tras amputación del dedo del pie. Ante broncoaspiración e inestabilidad hemodinámica con insuficiencia ventricular izquierda (IVI) ingresó en Unidad de Cuidados Intensivos (UCI). Se inició antibioterapia empírica con meropenem y daptomicina. Tras 72h de tratamiento, en hemocultivos y en herida creció SARM dirigiéndose antibioterapia con daptomicina 10mg/kg/día. Se realizó ecocardiograma transtorácico (ETT) confirmándose endocarditis por SARM, combinando daptomicina (día 8 de tratamiento) con ceftarolina 600mg/8h. Tras 48h, negativizaron hemocultivos. A la semana de la combinación se observó trombocitopenia progresiva (118.000 plaquetas/µL, figura 1) y se redujo ceftarolina (600mg/12h). El paciente sufrió empeoramiento de la amputación y síndrome de disfunción multiorgánica, falleciendo dos días después.
Caso clínico 2
Paciente de 79 años que ingresó en UCI por pancreatitis aguda, hipotensión y desaturación. Se extrajeron hemocultivos y se realizó una coronariografía con lesión en el tronco coronario izquierdo (TCI) que requiere revascularización quirúrgica trasladándose a nuestro hospital. Durante las primeras 12h en UCI, se informó de SARM en hemocultivos y catéter iniciándose daptomicina+cloxacilina. El tratamiento se suspendió tres días después, iniciando linezolid y piperacilina/tazobactam por pancreatitis. Tras 48h de ingreso, presentó sepsis e insuficiencia cardiaca, decidiendo realizar intervención coronaria percutánea implantándole 3 stents en TCI. Se confirmó bacteriemia por SARM y ante persistente crecimiento en hemocultivos, se realizó un ETE diagnosticándose endocarditis. Se suspendió linezolid y piperacilina/tazobactam, iniciándose daptomicina 10mg/kg/día y ceftarolina 600mg/8h. A las 72h, negativizaron hemocultivos.
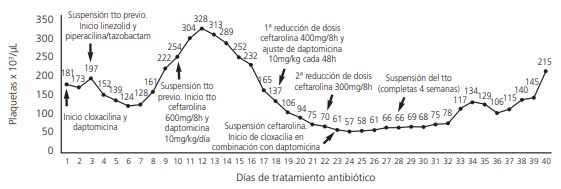
Tras 9 días con antibiótico, el paciente presentó fracaso renal agudo (creatinina: 1,61mg/dl) ajustándose ceftarolina 400mg/8h y daptomicina 700mg/48h. Cuatro días después, se reajustó ceftarolina 300mg/8h (creatinina: 1,8mg/dl). Se observó progresivo descenso de plaquetas apareciendo plaquetopenia a partir del 9º día de tratamiento (figura 2).
Ante la negativización, parámetros de infección negativos y 61.000 plaquetas/µL, el día 14 se cambió ceftarolina por cloxacilina. Al completar 4 semanas de tratamiento con hemocultivos negativos y sin signos de endocarditis, se suspendieron antibióticos. Se observó recuperación gradual de las plaquetas desde la suspensión de ceftarolina (figura 2).
Ambos casos fueron notificados al Servicio de Farmacovigilancia, y aplicando el algoritmo de Karch y Lasagna modificado por Naranjo et al., la relación de causalidad ceftarolinatrombocitopenia fue posible en el primer caso y probable en el segundo.
DISCUSIÓN
La trombocitopenia es un recuento de plaquetas en sangre <140.000 plaquetas/µL y como consecuencia aumenta el riesgo de sangrado.
En nuestros casos, se utilizó daptomicina y ceftarolina para tratar endocarditis por SARM, en indicación no aprobada en ficha técnica (IFFT) de ceftarolina para la que existe cierta evidencia en la literatura, avalando el uso combinado en bacteriemia persistente a pesar del tratamiento con daptomicina. En ficha técnica, ceftarolina se recomienda cada 12h pero en estos casos, se utiliza cada 8h2.
Ceftarolina es bactericida contra S.aureus manteniendo su actividad aunque pierda susceptibilidad a daptomicina/ vancomicina. Ho et al.3 describen 6 pacientes tratados con la combinación como tratamiento de rescate tras vancomicina. El régimen cada 8h produjo T>MIC libre del 100% y 92% con CMI 0,5mg/L y 1mg/L, respectivamente. Dada la gravedad de estas infecciones, se utilizan 600mg/8h para optimizar T>CMI. La duración de la bacteriemia al iniciar ceftarolina fue extremadamente corta, como en nuestros casos.
Los EA más notificados para ceftarolina en “vida real” han sido neutropenia y rash, asociándose a tratamientos prolongados y pautas cada 8h en IFFT4. En un estudio con 77 pacientes, la incidencia de neutropenia fue 10-14% con >2 semanas de tratamiento, y 21% con >34.
Sin embargo, la trombocitopenia ha sido menos descrita. En un estudio con 74 pacientes, se observaron 5 eventos de trombocitopenia. No observaron diferencias entre pacientes que recibieron dosificación cada 8h o cada 12h (p=0,4), pero presentaron más EA aquellos con tratamientos prolongados (17 días frente 6,5, p=0,002)5. En otro estudio en IFFT, con 84 pacientes, 2 sufrieron trombocitopenia6.
Britt et al.7, describen un caso de endocarditis con bacteriemia por SARM que no negativiza tras daptomicina por lo que inicia ceftarolina. Al 8º día observan trombocitopenia y suspenden ceftarolina con recuperación de plaquetas en una semana. Tras 15 días aparece una erupción, hipertransaminasemia y eosinofilia por lo que suspenden daptomicina y cambian a ceftarolina que produce de nuevo trombocitopenia (relación probable). Concluyen que la administración cada 8 horas pudiera haber aumentado el efecto.
En otro caso, paciente en hemodiálisis tras 6 semanas con daptomicina por SARM, desarrolló trombocitopenia al asociar ceftarolina. Se suspendió y al reintroducirla 10 días después volvió a aparecer, estableciéndose la relación causal ceftarolina-trombocitopenia como definitiva8.
Existen casos clínicos en la literatura de trombocitopenia por daptomicina. Grégoire et al.9 describen un caso de trombocitopenia grave (<10.000/µL) al 4º día de tratamiento. Leyra et al.10, describen un paciente con endocarditis tratada con daptomicina 10mg/kg/día y cefepime, que a los 28 días de tratamiento, desarrolló trombocitopenia retirándose cefepime, pero hasta suspensión de daptomicina las plaquetas no aumentaron. Según el algoritmo de Naranjo la relación fue probable.
En nuestros casos, ambos con daptomicina y ceftarolina; en el primero, se descartó trombocitopenia por daptomicina al haber estado 8 días en monoterapia sin plaquetopenia, mientras que en el segundo el paciente estuvo con daptomicina antes del tratamiento combinado sin objetivarse trombocitopenia.
Los estudios postautorización son importantes para detectar EA asociados a fármacos recientemente comercializados. Ceftarolina es eficaz en infecciones graves causadas por SARM, con pocas opciones de tratamiento por multirresistencia. La neutropenia está siendo asociada con cierta frecuencia con su uso prolongado y con altas dosis (10-21% según distintos autores) pero nuestros casos y otros descritos en literatura deben alertar sobre el riesgo de trombocitopenia y debería recomendarse la monitorización de los parámetros hematológicos, principalmente en IFFT con tratamientos prolongados.